Clear Sky Science · ar
إعادة تشكيل المناعة المستهدفة بواسطة ITK عززت فعالية علاج CAR‑T المضاد لـ CD19
جعل الخلايا المقاتلة للسرطان تدوم لفترة أطول
غيّر علاج خلايا CAR‑T مآل بعض سرطانات الدم بتحويل خلايا المناعة لدى المريض إلى صائدات موجهة للأورام. ومع ذلك، يعود المرض لدى العديد من المرضى لأن هذه الخلايا الهندسية تتعب وتضمحل بسرعة. تطرح هذه الدراسة سؤالاً بسيطاً لكنه ذو أثر كبير: هل يمكن تزويد خلايا CAR‑T بما يشبه «تعزيز قدرة التحمل المناعي» حتى تظل نشطة لفترة أطول وتقضي على مزيد من السرطان؟
لماذا تهم الخلايا التائية المعززة
خلايا CAR‑T هي خلايا دم بيضاء مخصصة تتعرف على علامات على خلايا السرطان، مثل CD19 في كثير من لمفومات وسرطانات الخلايا البائية. بعد هجوم أولي مبهر، تقل فعالية هذه الخلايا غالباً في البيئة العدائية حول الأورام. تدخل حالة متداعية تُعرف بالإنهاك، حيث تقل انقساماتها وتفرز جزيئات سامة أقل وتفقد قدرتها على قتل السرطان بفعالية. ركز الباحثون على مفصل داخلي مهم في الخلايا التائية، وهو بروتين يسمى ITK، الذي يساعد على نقل إشارات التنشيط. أشارت دراسات سابقة على الحيوانات إلى أن التحفيز المستمر لهذا المفتاح يساهم في الإرهاق. هنا اختبر الفريق ما إذا كان خفض نشاط ITK بدواء انتقائي للغاية، سوكليتينيب، يمكن أن يحافظ على خلايا CAR‑T قوية ومرنة في آن واحد.
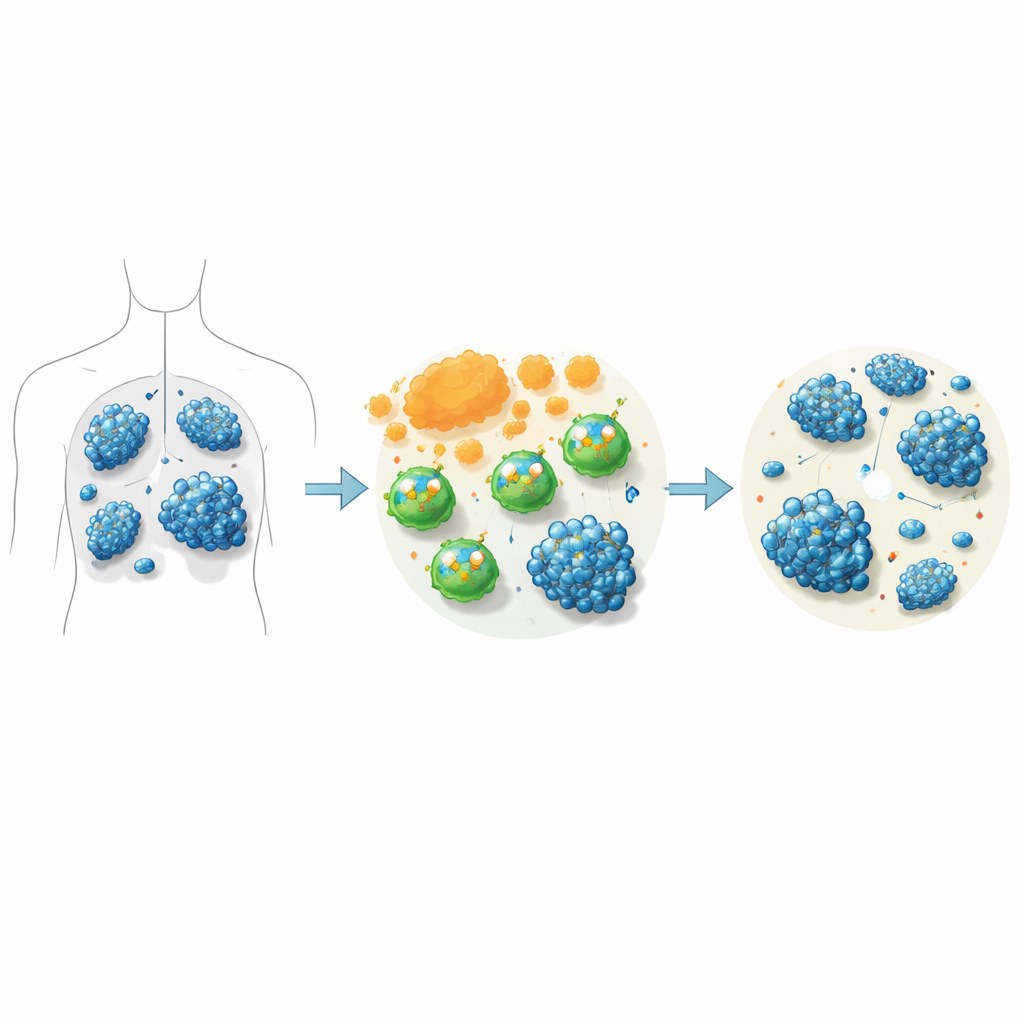
خفض إشارة لزيادة الهجوم
في تجارب مخبرية، قارن العلماء خلايا CAR‑T القياسية المستهدفة لـ CD19 مع خلايا CAR‑T التي تم حجب ITK فيها إما بطرق جينية أو بواسطة سوكليتينيب. عند مزج هذه الخلايا مع خلايا ليمفومة بشرية، دمرت خلايا CAR‑T المحجوبة فيها ITK عدداً أكبر من خلايا السرطان. كما أفرزت مستويات أعلى من جزيئات الهجوم الرئيسية مثل غرانزيم B وTNF‑alpha والإنترفيرون‑غاما، وأظهرت علامات أقوى على التنشيط. توسعت خلايا CAR‑T المعالجة بسوكليتينيب بشكل أفضل على مدى أسابيع في الثقافة، وماتت بنسبة أقل، وعززت خصوصاً نمو وقوة القتل لخلايا CD8 التائية، وهي الفئة «الجندية» الرئيسية المسؤولة عن القضاء المباشر على الخلايا الورمية.
إعادة توصيل إرهاق الخلايا التائية
تتمثل إسهامة كبيرة لهذه الدراسة في إظهار أن تثبيط ITK يفعل أكثر من مجرد تنشيط مؤقت لخلايا CAR‑T؛ إنه يعيد تشكيل البرامج التي تتحكم بالإنهاك والذاكرة. باستخدام تحليل دقيق لتوصيف الخلايا وتعبير الجينات، وجد الفريق أن سوكليتينيب خفّض مستويات عدة جزيئات «فرامل» على سطح خلايا CAR‑T وهدأ الدوائر الجينية الداخلية التي تقود الإرهاق المزمن. انخفضت علامات مثل PD‑1 وTIM3 وLAG3 وTIGIT وCD39، كلّها مرتبطة بالخلايا التائية المستنفدة، حتى بعد تعرض متكرر لخلايا الورم. في الوقت نفسه، ازدادت الجينات والبروتينات المرتبطة بالخلايا التائية طويلة العمر أو الشبيهة بالخلايا الجذعية أو الذاكرة—بما في ذلك TCF1 والجزيئات المتعلقة بالاستهداف والبقاء. بفعالية، دفع حجب ITK خلايا CAR‑T بعيداً عن حالة مُجهِدة ومفرطة التحفيز ونحو نمط قاتل أكثر توازناً وديمومة.
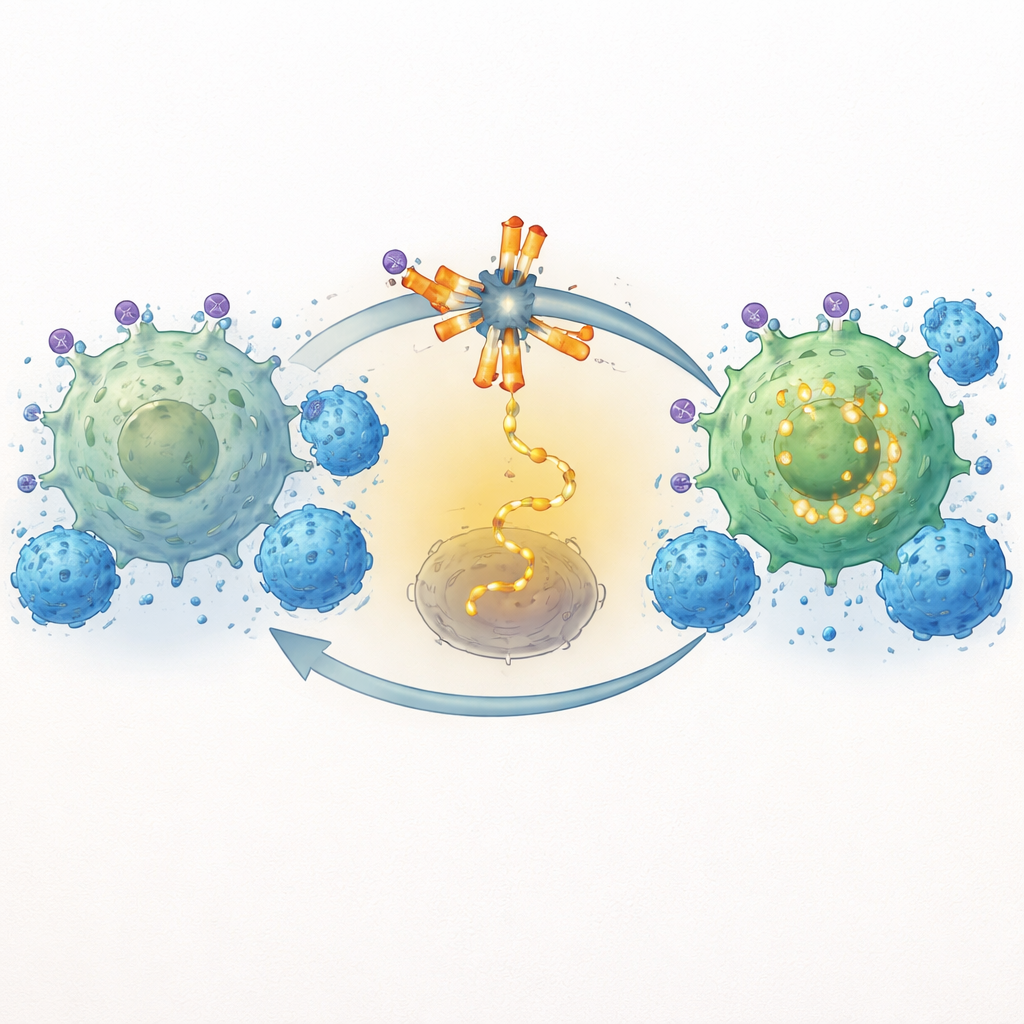
البرهان في نماذج حيوانية
لاختبار ما إذا كان هذا إعادة البرمجة مهمّة في كائنات حية، جرّب الباحثون التوليفة في فئران تحمل سرطان دم بشري عدواني. تلقت كل الحيوانات خلايا CAR‑T المستهدفة لـ CD19، لكن مجموعات فقط تلقت سوكليتينيب يومياً أيضاً. أظهرت مجموعة التوليفة انخفاضاً أكبر بكثير في عبء اللوكيميا، كما قيس بتصوير الجسم الكامل، وعاشت فترة أطول من الفئران المعالجة بخلايا CAR‑T وحدها. ومن المهم أن سوكليتينيب وحده لم يبطئ نمو الورم، مما يشير إلى أن فائدته ناتجة عن إعادة تشكيل الاستجابة المناعية بدلاً من عمله كدواء كيميائي تقليدي. تدعم هذه النتائج فكرة أن ضبط إشارات الخلايا التائية بدقة، بدلاً من دفعها بقوة أكبر فقط، يمكن أن يؤدي إلى هجوم مضاد للسرطان أكثر فعالية واستدامة.
ماذا قد يعني ذلك للمرضى
بالنسبة للأشخاص المصابين بلمفومات وسرطانات الخلايا البائية، وربما سرطانات أخرى، تشير هذه الدراسة إلى استراتيجية جديدة: إقران علاج CAR‑T بمثبط ITK لمنع إرهاق المناعة. من خلال تخفيف مسار إشارية واحد بشكل متواضع، يبدو أن سوكليتينيب يساعد خلايا CAR‑T على النمو، والبقاء وظيفية، ومقاومة الإنهاك، مما يؤدي إلى تحكم أقوى وأطول أمداً في الأورام في نماذج ما قبل السريرية. وبينما ستحتاج التجارب السريرية إلى تأكيد السلامة والمنفعة لدى المرضى، تقترح الدراسة أن «إعادة تشكيل» مناعية مستهدفة قد يجعل علاجات CAR‑T من الجيل التالي أكثر موثوقية وأكثر ديمومة، وربما قابلة للتوسيع إلى أورام صلبة قاومت هذه الصورة القوية من العلاج المناعي حتى الآن.
الاستشهاد: Li, Z., Lv, L., Yao, X. et al. ITK-targeted immune remodeling enhanced the efficacy of anti-CD19 CAR-T cell therapy. Cell Death Discov. 12, 131 (2026). https://doi.org/10.1038/s41420-026-03004-2
الكلمات المفتاحية: علاج خلايا CAR‑T, إنهاك الخلايا التائية, مثبط ITK, لمفوما الخلايا البائية, المناعة ضد السرطان