Clear Sky Science · es
La remodelación inmune dirigida a ITK mejoró la eficacia de la terapia CAR-T anti-CD19
Hacer que las células que combaten el cáncer duren más
La terapia CAR-T ha transformado el tratamiento de ciertos cánceres de la sangre al convertir las propias células inmunitarias del paciente en buscadoras de tumores dirigidas. Sin embargo, muchos pacientes recaen porque estas células modificadas se fatigan y desaparecen demasiado pronto. Este estudio plantea una pregunta sencilla pero potente: ¿podemos dar a las células CAR-T una especie de “impulso de resistencia inmune” para que permanezcan activas por más tiempo y eliminen más cáncer?
Por qué importan las células T supercargadas
Las células CAR-T son leucocitos personalizados que reconocen marcadores en las células cancerosas, como CD19 en muchos linfomas y leucemias de células B. Tras un ataque inicial impresionante, estas células con frecuencia disminuyen su actividad en el entorno hostil que rodea a los tumores. Entran en un estado de desgaste llamado agotamiento, en el que se dividen menos, liberan menos moléculas tóxicas y dejan de matar eficazmente al cáncer. Los investigadores se centraron en un interruptor interno clave en las células T, una proteína llamada ITK, que ayuda a transmitir señales de activación. Trabajos previos en animales sugirieron que la estimulación continua de este interruptor contribuye al desgaste. Aquí, el equipo probó si reducir la actividad de ITK con un fármaco muy selectivo, soquelitinib, podría mantener a las CAR-T tanto potentes como resistentes.
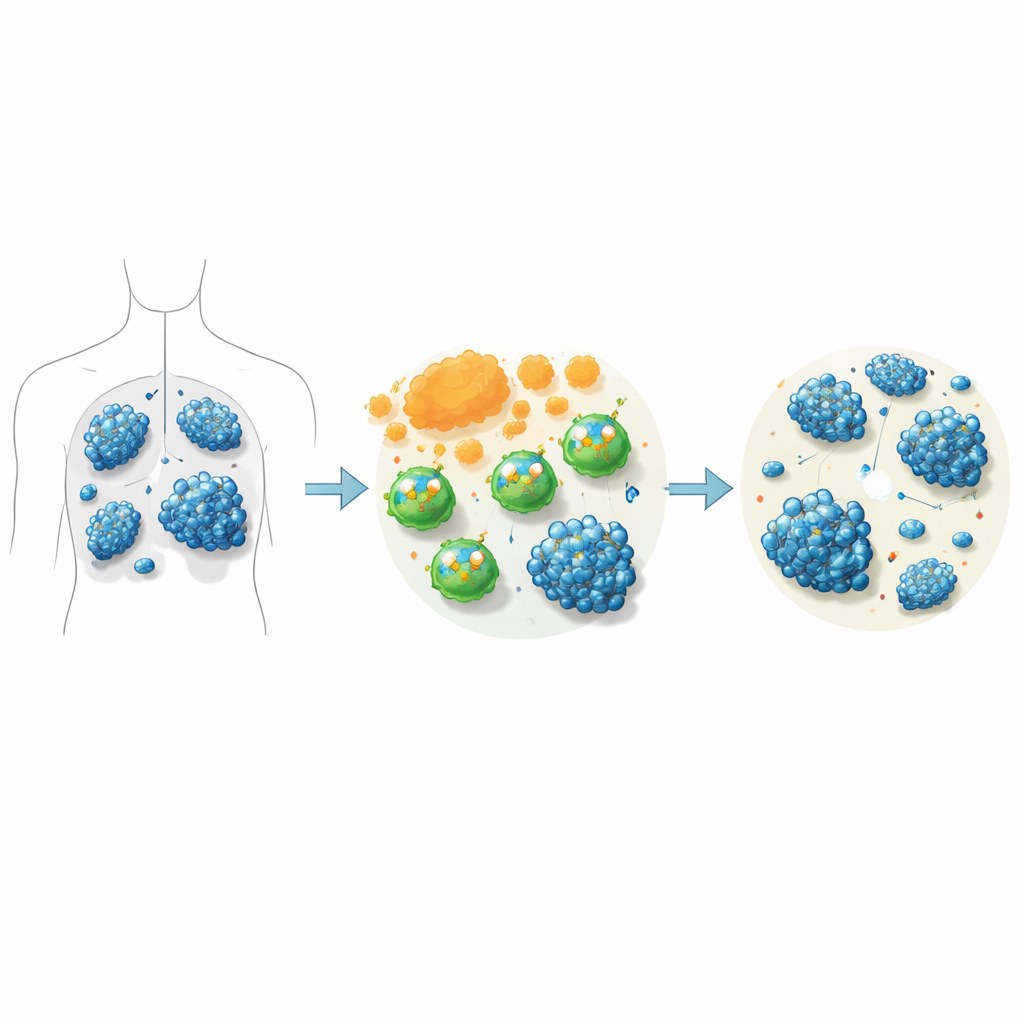
Bajar una señal para aumentar el ataque
En experimentos de laboratorio, los científicos compararon CAR-T estándar dirigidas a CD19 con CAR-T en las que ITK se bloqueó bien mediante métodos genéticos o bien con soquelitinib. Cuando estas células se mezclaron con células de linfoma humanas, las CAR-T con ITK bloqueado destruyeron más células cancerosas. También liberaron niveles más altos de moléculas clave de ataque como la granzima B, TNF-alfa e interferón gamma, y mostraron señales más fuertes de activación. Las CAR-T tratadas con soquelitinib se expandieron mejor durante semanas en cultivo, murieron con menos frecuencia y, en particular, aumentaron el crecimiento y el poder citotóxico de las células T CD8, el subconjunto principal “soldado” responsable de eliminar directamente las células tumorales.
Reconfigurando la fatiga de las células T
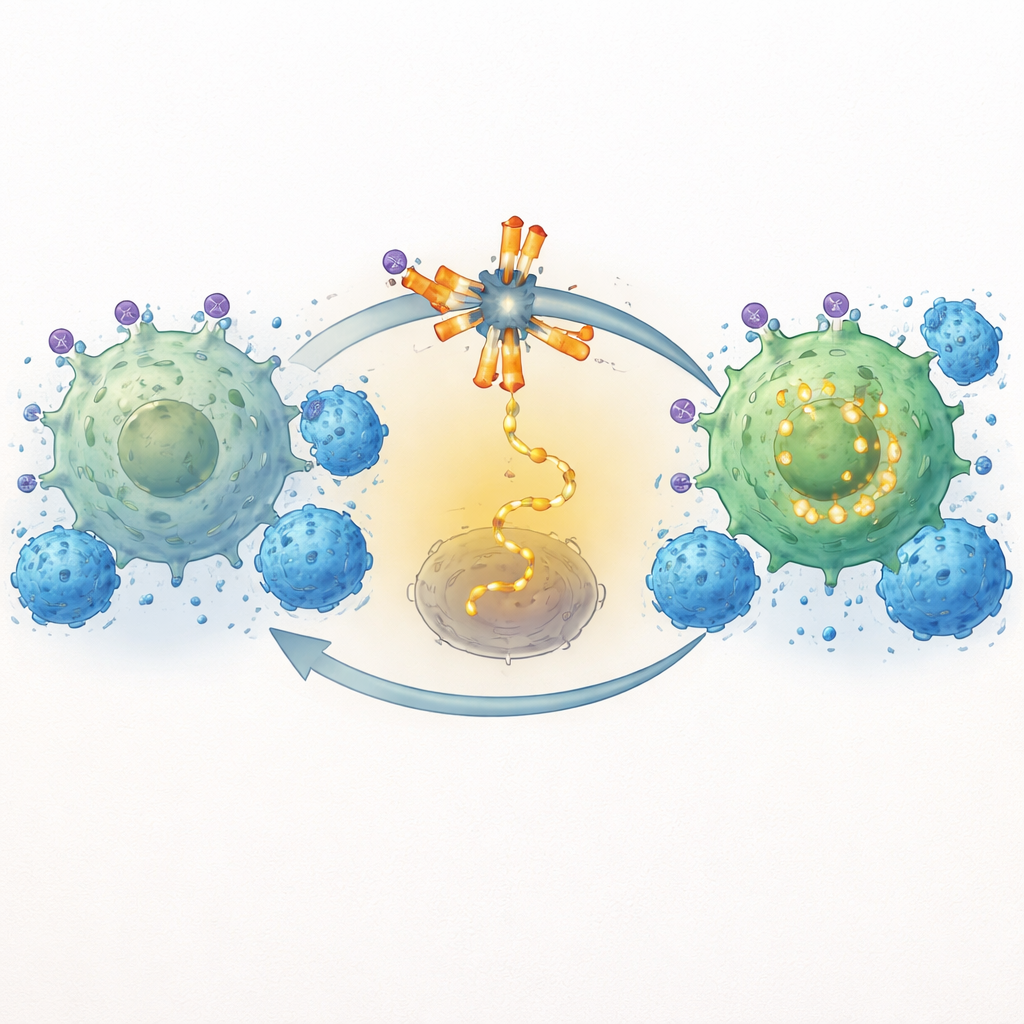
Un avance importante de este trabajo es mostrar que la inhibición de ITK hace más que activar temporalmente a las CAR-T; reconfigura los programas que controlan el agotamiento y la memoria. Mediante un perfilado celular detallado y análisis de expresión génica, el equipo encontró que el soquelitinib redujo múltiples moléculas “de freno” en la superficie de las CAR-T y atenuó los circuitos genéticos internos que impulsan la fatiga crónica. Marcadores como PD-1, TIM3, LAG3, TIGIT y CD39, todos asociados con células T agotadas, se redujeron incluso tras exposiciones repetidas a células tumorales. Al mismo tiempo, aumentaron genes y proteínas asociados con células T de larga vida, con características de tipo progenitor o memoria —incluyendo TCF1 y moléculas relacionadas con la migración y la supervivencia. En efecto, el bloqueo de ITK empujó a las CAR-T lejos de un estado agotado y sobreestimulado hacia un perfil de asesino más equilibrado y durable.
Prueba en modelos animales
Para ver si esta reprogramación tenía impacto en organismos vivos, los investigadores probaron la combinación en ratones portadores de leucemia humana agresiva. Todos los animales recibieron CAR-T contra CD19, pero solo algunos también recibieron soquelitinib diariamente. El grupo combinado mostró una caída mucho mayor en la carga de leucemia, medida por imagen corporal total, y vivió más tiempo que los ratones tratados solo con CAR-T. Es importante señalar que el soquelitinib por sí solo no ralentizó el crecimiento tumoral, lo que indica que su beneficio proviene de remodelar la respuesta inmune más que de actuar como un fármaco quimioterápico convencional. Estos hallazgos apoyan la idea de que ajustar con precisión la señalización de las células T, en lugar de simplemente potenciarla, puede generar un ataque contra el cáncer más eficaz y sostenible.
Qué podría significar esto para los pacientes
Para las personas con linfomas y leucemias de células B, y potencialmente otros cánceres, este estudio apunta a una nueva estrategia: combinar la terapia CAR-T con un inhibidor de ITK para prevenir el desgaste inmune. Mediante la atenuación moderada de una vía de señalización, el soquelitinib parece ayudar a las CAR-T a proliferar, mantenerse funcionales y resistir el agotamiento, lo que conduce a un control tumoral más fuerte y duradero en modelos preclínicos. Aunque serán necesarios ensayos clínicos para confirmar seguridad y beneficio en pacientes, el trabajo sugiere que la “remodelación” inmune dirigida podría hacer que las terapias CAR-T de próxima generación sean más fiables, más duraderas y quizá extensibles a tumores sólidos que hasta ahora han resistido esta potente forma de inmunoterapia.
Cita: Li, Z., Lv, L., Yao, X. et al. ITK-targeted immune remodeling enhanced the efficacy of anti-CD19 CAR-T cell therapy. Cell Death Discov. 12, 131 (2026). https://doi.org/10.1038/s41420-026-03004-2
Palabras clave: Terapia con células CAR-T, Agotamiento de células T, Inhibición de ITK, Linfoma de células B, Inmunoterapia contra el cáncer