Clear Sky Science · it
Il rimodellamento immunitario mirato a ITK ha potenziato l’efficacia della terapia con CAR-T anti-CD19
Far durare più a lungo le cellule che combattono il cancro
La terapia con cellule CAR-T ha trasformato il trattamento di alcuni tumori del sangue convertendo le cellule immunitarie del paziente in cacciatori mirati dei tumori. Tuttavia molti pazienti recidivano perché queste cellule ingegnerizzate si affaticano e scompaiono troppo presto. Questo studio pone una domanda semplice ma potente: possiamo fornire alle CAR-T una sorta di “potenziamento dell’endurance immunitaria” affinché rimangano attive più a lungo e annihilino più tumore?
Perché le cellule T potenziate sono importanti
Le CAR-T sono globuli bianchi personalizzati che riconoscono marcatori sulle cellule tumorali, come il CD19 in molti linfomi e leucemie delle cellule B. Dopo un attacco iniziale impressionante, queste cellule spesso rallentano nell’ambiente ostile intorno ai tumori. Entrano in uno stato di logoramento chiamato esaurimento, in cui si dividono meno, rilasciano meno molecole tossiche e smettono di uccidere efficacemente il cancro. I ricercatori si sono concentrati su un interruttore interno chiave nelle cellule T, una proteina chiamata ITK, che aiuta a trasmettere i segnali di attivazione. Studi precedenti su animali suggerivano che la spinta costante di questo interruttore contribuisce al burnout. Qui il gruppo ha testato se attenuare ITK con un farmaco altamente selettivo, lo soquelitinib, potesse mantenere le CAR-T potenti e resilienti.
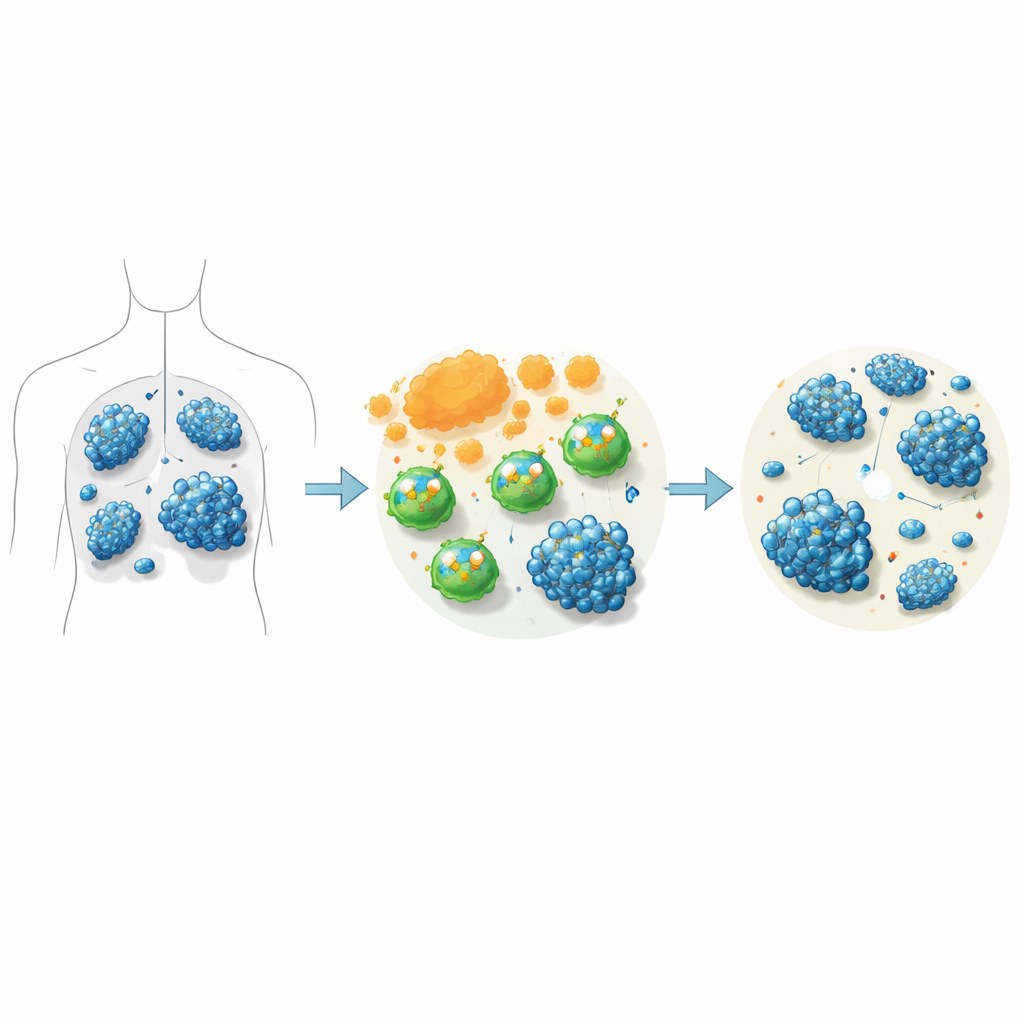
Abbassare un segnale per alzare l’attacco
Negli esperimenti in laboratorio, gli scienziati hanno confrontato CAR-T standard mirate a CD19 con CAR-T in cui ITK era bloccata sia con metodi genetici sia con lo soquelitinib. Quando queste cellule sono state mescolate con cellule linfomatose umane, le CAR-T con ITK bloccata hanno distrutto più cellule tumorali. Hanno inoltre rilasciato livelli più elevati di molecole chiave d’attacco come granzima B, TNF-alfa e interferone-gamma, e hanno mostrato segni più forti di attivazione. Le CAR-T trattate con soquelitinib si sono anche espanse meglio nel corso di settimane in coltura, sono morte meno frequentemente e in particolare hanno aumentato la crescita e il potere citotossico delle cellule T CD8, il sottogruppo “soldato” principale responsabile dell’eliminazione diretta delle cellule tumorali.
Riprogrammare l’affaticamento delle cellule T
Un avanzamento rilevante di questo lavoro è dimostrare che l’inibizione di ITK fa più che risvegliare temporaneamente le CAR-T; rimodella i programmi che controllano l’esaurimento e la memoria. Usando un profilo dettagliato delle cellule e l’analisi dell’espressione genica, il gruppo ha rilevato che lo soquelitinib ha sia abbassato molteplici molecole “freno” sulla superficie delle CAR-T sia attenuato i circuiti genetici interni che guidano la fatica cronica. Marcatori come PD-1, TIM3, LAG3, TIGIT e CD39, tutti associati alle cellule T logorate, sono risultati ridotti anche dopo esposizioni ripetute alle cellule tumorali. Allo stesso tempo, geni e proteine associati a cellule T di lunga durata, con caratteristiche staminali o di memoria — tra cui TCF1 e molecole legate al trafficking e alla sopravvivenza — sono aumentati. Di fatto, il blocco di ITK ha spinto le CAR-T lontano da uno stato esaurito e sovra-stimolato verso un profilo di killer più equilibrato e durevole.
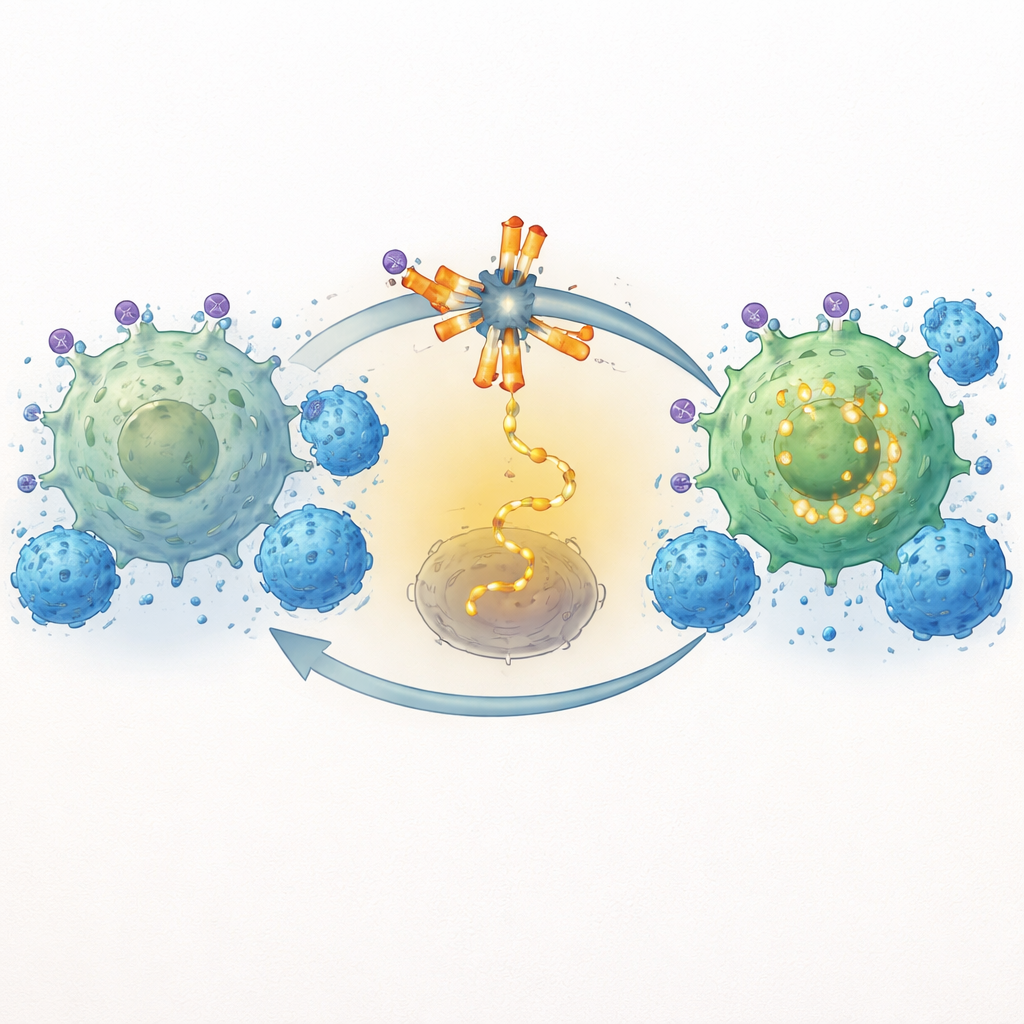
Prova nei modelli animali
Per verificare se questa riprogrammazione avesse effetto negli organismi viventi, i ricercatori hanno testato la combinazione in topi portatori di una leucemia umana aggressiva. Tutti gli animali hanno ricevuto CAR-T anti-CD19, ma solo alcuni hanno ricevuto quotidianamente anche lo soquelitinib. Il gruppo trattato con la combinazione ha mostrato una riduzione molto maggiore del carico leucemico, misurata con imaging dell’intero corpo, e ha vissuto più a lungo rispetto ai topi trattati solo con CAR-T. Importante, lo soquelitinib da solo non ha rallentato la crescita tumorale, indicando che il suo beneficio deriva dal rimodellare la risposta immunitaria piuttosto che dall’agire come un chemioterapico convenzionale. Questi risultati supportano l’idea che regolare con precisione il segnalamento delle cellule T, anziché semplicemente potenziarlo, può generare un attacco contro il cancro più efficace e sostenibile.
Cosa potrebbe significare per i pazienti
Per le persone con linfomi o leucemie delle cellule B, e potenzialmente altri tumori, questo studio indica una nuova strategia: abbinare la terapia CAR-T con un inibitore di ITK per prevenire il burnout immunitario. Attenuando modestamente una via di segnalazione, lo soquelitinib sembra aiutare le CAR-T a proliferare, rimanere funzionali e resistere all’esaurimento, portando a un controllo tumorale più forte e duraturo nei modelli preclinici. Pur richiedendo studi clinici per confermare sicurezza e beneficio nei pazienti, il lavoro suggerisce che il “rimodellamento” mirato del sistema immunitario potrebbe rendere le terapie CAR-T di nuova generazione più affidabili, più durature e forse estendibili anche ai tumori solidi che finora hanno resistito a questa potente forma di immunoterapia.
Citazione: Li, Z., Lv, L., Yao, X. et al. ITK-targeted immune remodeling enhanced the efficacy of anti-CD19 CAR-T cell therapy. Cell Death Discov. 12, 131 (2026). https://doi.org/10.1038/s41420-026-03004-2
Parole chiave: Terapia con cellule CAR-T, Esaurimento delle cellule T, Inibizione di ITK, Linfoma delle cellule B, Immunoterapia del cancro