Clear Sky Science · he
שדרוג ממוקד של המערכת החיסונית נגד ITK שיפור את היעילות של טיפול CAR‑T נגד CD19
להאריך את חיי התאים הנלחמים בסרטן
טיפול תאי CAR‑T חולל מהפיכה בטיפול בסוגים מסוימים של סרטן הדם על‑ידי הפיכת תאי החיסון של החולה לציידים ממוקדים של הגידול. עם זאת, עדיין רבים מהחולים עוברים הישנות כי התאים המהונדסים מתעייפים ונעלמים מוקדם מדי. המחקר הזה שואל שאלה פשוטה אך חזקה: האם ניתן לתת לתאי CAR‑T סוג של "חיזוק סיבולת חיסונית" כדי שהם יישארו פעילים זמן רב יותר וייכלו יותר מהסרטן?
למה חשובות תאי T משודרגות
תאי CAR‑T הם תאי דם לבנים מותאמים שמזהים סמנים על תאי סרטן, כגון CD19 ברבות מהלימפומות והלוקמיות של תאי B. לאחר מתקפה ראשונית מרשימה, תאים אלה לעתים מקרטעים בסביבה העוינת סביב הגידול. הם נכנסים למצב של שחיקה הנקרא התשה, שבו הם מתחלקים פחות, משחררים פחות מולקולות טוקסיות ועוצרים מלהשמיד את הסרטן ביעילות. החוקרים התמקדו במתג פנימי מרכזי בתאי T, חלבון שנקרא ITK, שעוזר לשדר אותות הפעלה. עבודות חיות קודמות הצביעו על כך שהפעלת מתג זה בעקביות תורמת לשחיקה. כאן, הצוות בחן האם הקטנת פעילות ITK בעזרת תרופה סלקטיבית מאוד, סוקלטיניב, יכולה לשמור על תאי CAR‑T חזקים ועמידים.
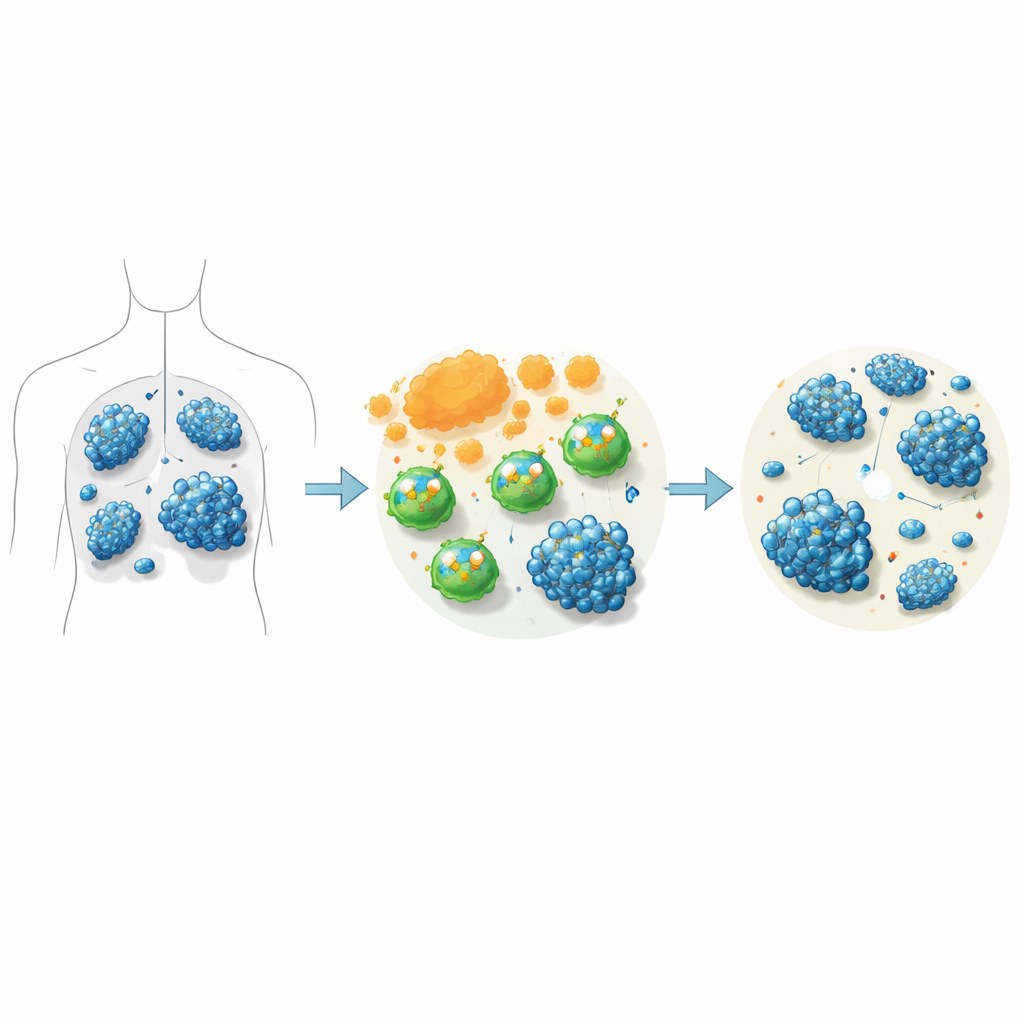
להדביר אות כדי להגביר את המתקפה
בניסויים במעבדה השוו המדענים בין תאי CAR‑T סטנדרטיים המכוונים ל‑CD19 לבין תאי CAR‑T שבהם הושתק ITK על‑ידי שיטות גנטיות או על‑ידי סוקלטיניב. כאשר תאים אלה נערבבו עם תאי לימפומה אנושיים, תאי CAR‑T בעלי עיכוב ITK השמידו יותר תאי סרטן. הם גם שחררו רמות גבוהות יותר של מולקולות התקפה מרכזיות כמו גרנצ'ים B, TNF‑alpha ואינטרפרון‑גמא, והציגו סימנים חזקים יותר של הפעלה. תאי CAR‑T שטופלו בסוקלטיניב התרחבו טוב יותר במהלך שבועות של תרבות, מתו פחות, ובמיוחד הגדילו את הצמיחה וכוח ההריגה של תאי CD8, תת‑הקבוצה ה"חיילת" העיקרית האחראית לחיסול ישיר של תאי הגידול.
לתכנת מחדש את עייפות תאי T
הישג מרכזי של עבודה זו הוא ההדגמה שעיכוב ITK עושה יותר מאשר להגביר זמנית את פעילות תאי CAR‑T; הוא משנים את התוכניות השולטות בהתשה ובזיכרון. באמצעות פרופילינג תאי מפורט וניתוח ביטוי גנים, הצוות מצא שסוקלטיניב גם הפחית מספר מולקולות "בלם" על פני השטח של CAR‑T וגם השתק את המעגלים הגנטיים הפנימיים שמניעים עייפות כרונית. סמנים כמו PD‑1, TIM3, LAG3, TIGIT ו‑CD39, כולם מקושרים לתאי T מותשים, פחתו אפילו לאחר חשיפות חוזרות לתאי גידול. במקביל, גנים וחלבונים המשויכים לתאי זיכרון או בעלי תכונות דמויות‑גזע וארוכי‑חי, כולל TCF1 ומולקולות הקשורות לנווט והישרדות, עלו ברמותיהם. במובן זה, חסימת ITK הטתה את תאי CAR‑T ממצב מותש ומוגבר מידות לכיוון פרופיל קוטל יותר מאוזן ועמיד.
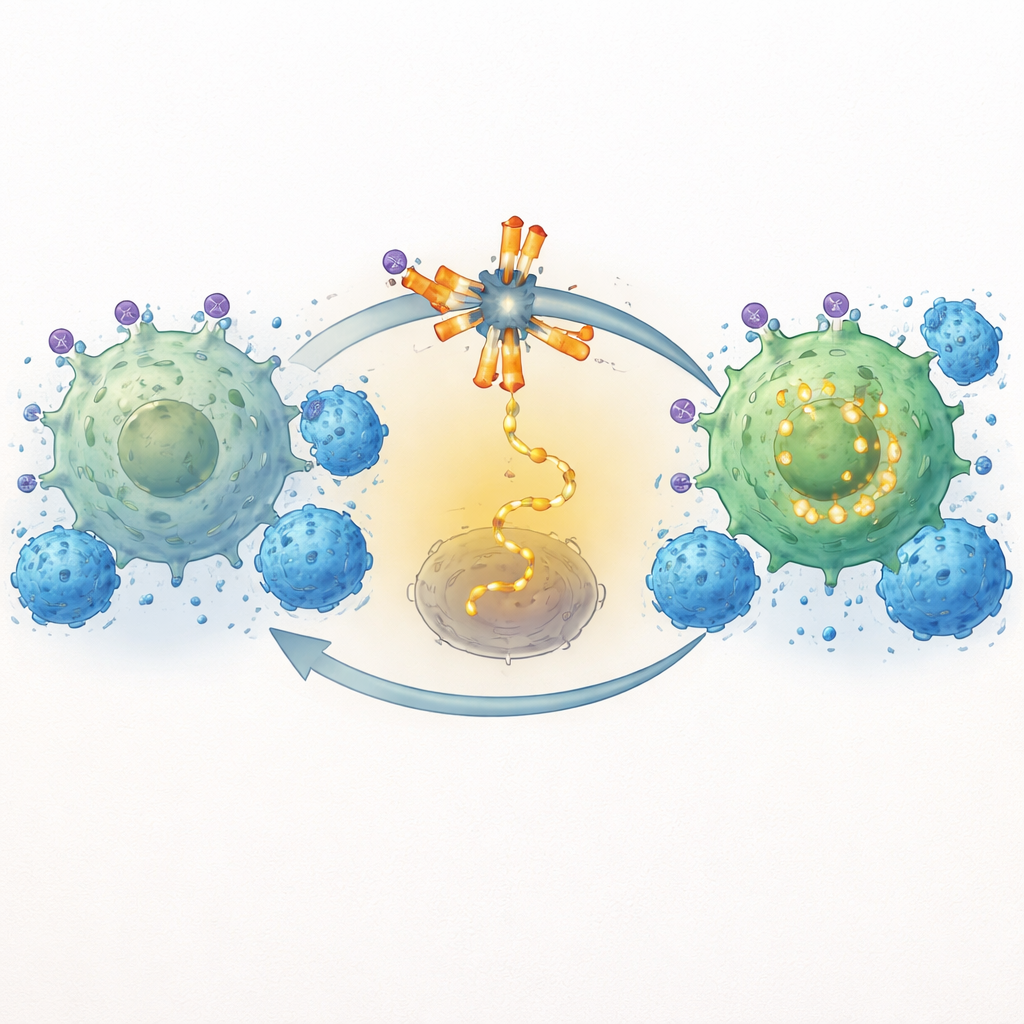
הוכחה במודלים חייים
כדי לבדוק האם תכנות מחדש זה חשוב באורגניזמים חיים, החוקרים בחנו את השילוב בעכברים הנשאים לוקמיה אנושית אגרסיבית. כל החיות קיבלו תאי CAR‑T נגד CD19, אך רק חלק מהן קיבלו גם סוקלטיניב יומי. קבוצת השילוב הראתה ירידה משמעותית יותר בעומס הלוקמיה, כפי שנמדד בהדמיה של כל הגוף, וחיה זמן רב יותר מהעכברים שטופלו בתאי CAR‑T בלבד. חשוב לציין שסוקלטיניב לבדו לא האט את צמיחת הגידול, מה שמעיד שהתועלת שלו נובעת מעיצוב תגובת המערכת החיסונית ולא מפעולה כטיפול כימותרפי קונבנציונלי. הממצאים תומכים ברעיון שבעיצוב מדויק של איתות בתאי T, במקום פשוט להגבירו, יכול להניב מתקפה על הסרטן יעילה וברת‑קיימא יותר.
מה זה עשוי להצביע לחולים
עבור אנשים המתמודדים עם לימפומות ולוקמיות של תאי B, וייתכן שגם סוגי סרטן אחרים, המחקר מצביע על אסטרטגיה חדשה: לשלב טיפול CAR‑T עם מעכב ITK כדי למנוע שחיקת מערכת החיסון. על‑ידי השתקת נתיב איתות אחד במידה מתונה, נראה שסוקלטיניב מסייע לתאי CAR‑T לגדול, להישאר תפקודיים ולסבול פחות התשה, מה שמוביל לשליטה חזקה וארוכת‑טווח יותר בגידול במודלים פרה‑קליניים. אמנם יידרשו ניסויים קליניים כדי לאשר בטיחות ותועלת בחולים, העבודה מצביעה על כך ש"שיפוץ" חיסוני ממוקד עשוי להפוך טיפולי CAR‑T בדור הבא לאמינים ועמידים יותר, ואולי להרחיבם גם לגידולים מוצקים שהתנגדו עד כה לצורה חזקה זו של אימונותרפיה.
ציטוט: Li, Z., Lv, L., Yao, X. et al. ITK-targeted immune remodeling enhanced the efficacy of anti-CD19 CAR-T cell therapy. Cell Death Discov. 12, 131 (2026). https://doi.org/10.1038/s41420-026-03004-2
מילות מפתח: טיפול תאי CAR‑T, התשה של תאים T, עיכוב ITK, לימפומה של תאי B, אימונותרפיה נגד סרטן