Clear Sky Science · pl
Onkogenny GPRIN1 podtrzymuje proliferację i homeostazę mitochondrialną poprzez dwuwarstwowe sygnalizowanie CDK1-PI3K/Akt w raku pęcherzyka żółciowego
Dlaczego te badania mają znaczenie
Rak pęcherzyka żółciowego jest rzadki, ale wyjątkowo śmiertelny — często wykrywany zbyt późno, by możliwe było skuteczne leczenie chirurgiczne. W badaniu odkryto wcześniej nieznany „przełącznik główny”, białko nazwane GPRIN1, które pomaga komórkom raka pęcherzyka żółciowego szybko się mnożyć, jednocześnie utrzymując w dobrym stanie ich małe elektrownie — mitochondria. Zrozumienie tego przełącznika może otworzyć drogę do bardziej precyzyjnych, mniej toksycznych terapii dla nowotworu, dla którego obecnie dostępnych jest niewiele opcji.
Ukryty czynnik napędowy w śmiertelnym nowotworze
Naukowcy zaczęli od analizy próbek guzów od 100 pacjentów z rakiem pęcherzyka żółciowego. Stwierdzili, że poziomy GPRIN1 były znacznie wyższe w guzach niż w sąsiadującej zdrowej tkance. Pacjenci, których guzy wykazywały najwyższe stężenie GPRIN1, mieli bardziej zaawansowaną chorobę i krótsze przeżycie, co sugeruje silny związek tego białka z agresywnością nowotworu. W modelach mysich guzy zaprogramowane do produkcji dodatkowego GPRIN1 rosły szybciej, wzmacniając przekonanie, że ta cząsteczka nie jest jedynie towarzyszem, lecz aktywnym promotorem wzrostu guza.
Łączenie podziału komórkowego z zasilaniem komórki
Szybko rosnące komórki nowotworowe muszą jednocześnie przeskoczyć przez cykl komórkowy i zapewnić wystarczającą ilość energii na wspieranie ekspansji. Zespół wykazał, że GPRIN1 znajduje się w centrum tej koordynacji. Po zmniejszeniu poziomu GPRIN1 w liniach komórkowych raka pęcherzyka żółciowego komórki traciły energię, produkowały mniej ATP i gromadziły szkodliwe reaktywne formy tlenu. Pod mikroskopem mitochondria wyglądały na spuchnięte i uszkodzone. Jednocześnie zastał normalny system oczyszczania — mitofagia, odpowiedzialna za usuwanie wadliwych mitochondriów. Kluczowe białka uruchamiające ten proces, PINK1 i PARKIN, spadły, a uszkodzone mitochondria gromadziły się. Zarówno w komórkach hodowlanych, jak i w guzach mysich, GPRIN1 okazał się niezbędny do utrzymania funkcjonalności mitochondriów na tyle, by zasilać nieustanny wzrost.
Podwójny przełącznik kontroli aparatu cyklu komórkowego
Pogłębiając badania, naukowcy wykorzystali wielkoskalowe ekrany białkowe i fosforylacyjne, by poszukać molekuł zmieniających się po stłumieniu GPRIN1. Jeden czynnik wyróżniał się: CDK1, centralny silnik napędzający komórki przez końcowe etapy podziału. GPRIN1 zwiększał zarówno ilość, jak i aktywność CDK1. W jądrze komórkowym GPRIN1 fizycznie wiązał się z innym białkiem, E2F1, i stabilizował je, co pozwalało E2F1 silniej włączać gen CDK1. Poza jądrem GPRIN1 przekształcał otoczenie białkowe CDK1, odciągając go od naturalnych hamulców i kierując ku aktywatorom. Ta „dwuwarstwowa” kontrola — na poziomie genu i białka — tworzy nadaktywne „silnik” CDK1, który popycha komórki szybko do podziału.
Od sygnałów molekularnych do równowagi mitochondrialnej
Historia nie skończyła się na CDK1. Zespół odkrył, że nadaktywne CDK1 z kolei włącza dobrze znaną ścieżkę przetrwania PI3K/Akt, która pomaga komórkom nowotworowym opierać się stresowi i śmierci. Gdy CDK1 zostało zablokowane, GPRIN1 nie mogło już uruchomić tej ścieżki. A gdy badacze zastosowali inhibitor PI3K o nazwie Buparlisib, zlikwidował on korzyści wynikające z obecności GPRIN1: podział komórek zwolnił, produkcja ATP powróciła do normy, stres oksydacyjny wzrósł, a mechanizmy mitofagii zostały zakłócone. W istocie GPRIN1 używa CDK1 do włączenia PI3K/Akt, które następnie koordynuje zarówno szybki wzrost komórek, jak i dokładne utrzymanie mitochondriów, dając komórkom raka pęcherzyka żółciowego potężną przewagę przetrwania.
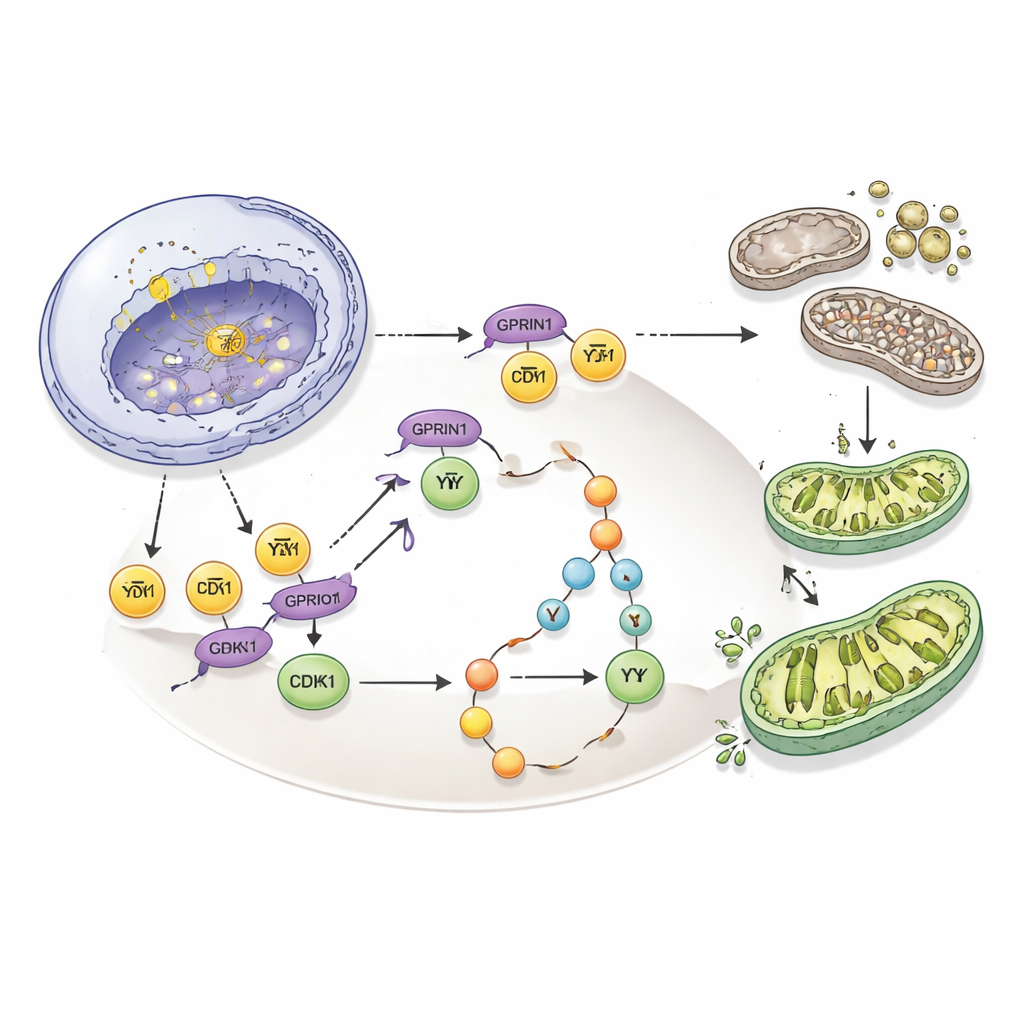
Przekształcenie słabości w możliwości terapeutyczne
Podsumowując, wyniki wskazują na GPRIN1 jako centralnego konduktora łączącego tempo podziału komórek raka pęcherzyka żółciowego z efektywnością utrzymania ich mitochondriów. Stabilizując E2F1, wzmacniając CDK1 i angażując PI3K/Akt, GPRIN1 buduje samowzmacniającą się pętlę napędzającą agresywny wzrost guza. Co ważne, przerwanie tej pętli — poprzez zmniejszenie GPRIN1, wyciszenie CDK1 lub zablokowanie PI3K — znacząco spowolniło, a nawet zatrzymało powstawanie guzów w komórkach i u myszy. Dla pacjentów sugeruje to, że pomiar poziomu GPRIN1 mógłby pomóc przewidywać rokowanie, a leki celujące w oś GPRIN1–CDK1–PI3K/Akt mogą dostarczyć bardziej ukierunkowanej opcji leczenia jednego z najbardziej wymagających nowotworów układu pokarmowego.
Cytowanie: Xu, C., Gong, Z., Ni, X. et al. Oncogenic GPRIN1 sustains proliferation and mitochondrial homeostasis via dual‑layer CDK1-PI3K/Akt signalling in gallbladder cancer. Cell Death Dis 17, 333 (2026). https://doi.org/10.1038/s41419-026-08550-2
Słowa kluczowe: rak pęcherzyka żółciowego, GPRIN1, CDK1, homeostaza mitochondrialna, sygnalizacja PI3K Akt