Clear Sky Science · de
Onkogenes GPRIN1 erhält Proliferation und mitochondriale Homöostase durch zweischichtige CDK1‑PI3K/Akt‑Signalgebung beim Gallenblasenkrebs
Warum diese Forschung wichtig ist
Gallenblasenkrebs ist selten, aber äußerst tödlich und wird häufig zu spät für eine Operation oder wirksame Therapie entdeckt. Diese Studie enthüllt ein bislang unbekanntes „Hauptschalter“-Protein namens GPRIN1, das Gallenblasenkrebszellen hilft, sich schnell zu vermehren, während es gleichzeitig ihre kleinen Kraftwerke — die Mitochondrien — funktionsfähig hält. Das Verständnis dieses Schalters könnte den Weg zu präziseren, weniger toxischen Therapien für eine Krebsform ebnen, für die derzeit sehr wenige Optionen bestehen.
Ein verborgener Treiber eines tödlichen Krebses
Die Forschenden begannen mit der Untersuchung von Tumorproben von 100 Patientinnen und Patienten mit Gallenblasenkrebs. Sie fanden heraus, dass die GPRIN1‑Spiegel in Tumoren deutlich höher waren als im umliegenden gesunden Gewebe. Patientinnen und Patienten, deren Tumoren am meisten GPRIN1 aufwiesen, hatten weiter fortgeschrittene Erkrankungen und eine kürzere Überlebenszeit, was darauf hindeutet, dass dieses Protein eng mit der Aggressivität des Tumors verknüpft ist. In Mausmodellen wuchsen Tumoren, die genetisch so verändert wurden, dass sie zusätzliches GPRIN1 produzierten, schneller — ein Befund, der die These stützt, dass dieses Molekül kein blinder Passagier, sondern ein aktiver Treiber des Tumorwachstums ist.
Verknüpfung von Zellteilung und zellulärer Energieversorgung
Schnell wachsende Krebszellen müssen gleichzeitig den Zellzyklus vorantreiben und ausreichend Energie für ihre Expansion bereitstellen. Das Team zeigte, dass GPRIN1 im Zentrum dieser Koordination steht. Wenn sie GPRIN1 in Gallenblasenkrebs‑Zelllinien reduzierten, verloren die Zellen Energie, produzierten weniger ATP und sammelten schädliche reaktive Sauerstoffspezies an. Unter dem Mikroskop wirkten ihre Mitochondrien geschwollen und beschädigt. Gleichzeitig kam das normale Aufräumsystem — die Mitophagie, die defekte Mitochondrien entfernt — zum Erliegen. Schlüsselproteine, die diese Reinigung starten, PINK1 und PARKIN, gingen zurück, und beschädigte Mitochondrien häuften sich an. Sowohl in kultivierten Zellen als auch in Maus‑Tumoren erwies sich GPRIN1 als wesentlich, um die Mitochondrien so funktionsfähig zu halten, dass sie das unablässige Wachstum antreiben können.
Der doppelte Kontrollschalter der Zellzyklusmaschinerie
Bei tiefergehenden Untersuchungen nutzten die Wissenschaftler groß angelegte Protein‑ und Phosphorylierungs‑Screenings, um Moleküle zu finden, die sich ändern, wenn GPRIN1 heruntergeregelt wird. Eines stach hervor: CDK1, ein zentrales Aggregat, das Zellen durch die finalen Phasen der Teilung treibt. GPRIN1 erhöhte sowohl die Menge als auch die Aktivität von CDK1. Im Zellkern band GPRIN1 physisch an ein anderes Protein, E2F1, und stabilisierte es, wodurch E2F1 stärker das CDK1‑Gen aktivieren konnte. Außerhalb des Zellkerns veränderte GPRIN1 die Proteinpartner von CDK1, lenkte es weg von seinen natürlichen Bremsen und hin zu seinen Aktivatoren. Diese „zweischichtige“ Steuerung — auf Gen‑ und Protein‑Ebene — schafft einen hyperaktiven CDK1‑Motor, der Zellen rasch in die Teilung treibt.
Von molekularen Signalen zum mitochondrialen Gleichgewicht
Die Geschichte endete nicht bei CDK1. Das Team entdeckte, dass dieser überaktive CDK1 wiederum einen bekannten Überlebensweg, PI3K/Akt, einschaltete, der Krebszellen hilft, Stress und Zelltod zu widerstehen. Wenn CDK1 blockiert wurde, konnte GPRIN1 diesen Weg nicht mehr aktivieren. Und als die Forschenden ein PI3K‑Inhibitor‑Medikament namens Buparlisib einsetzten, beseitigte es die Vorteile von GPRIN1: Die Zellteilung verlangsamte sich, die ATP‑Produktion fiel wieder auf Normalniveau, der oxidative Stress stieg und die Mitophagie‑Maschinerie wurde gestört. Im Kern nutzt GPRIN1 CDK1, um PI3K/Akt zu aktivieren, das dann sowohl schnelles Zellwachstum als auch die sorgfältige Erhaltung der Mitochondrien koordiniert und den Gallenblasenkrebszellen einen starken Überlebensvorteil verschafft.
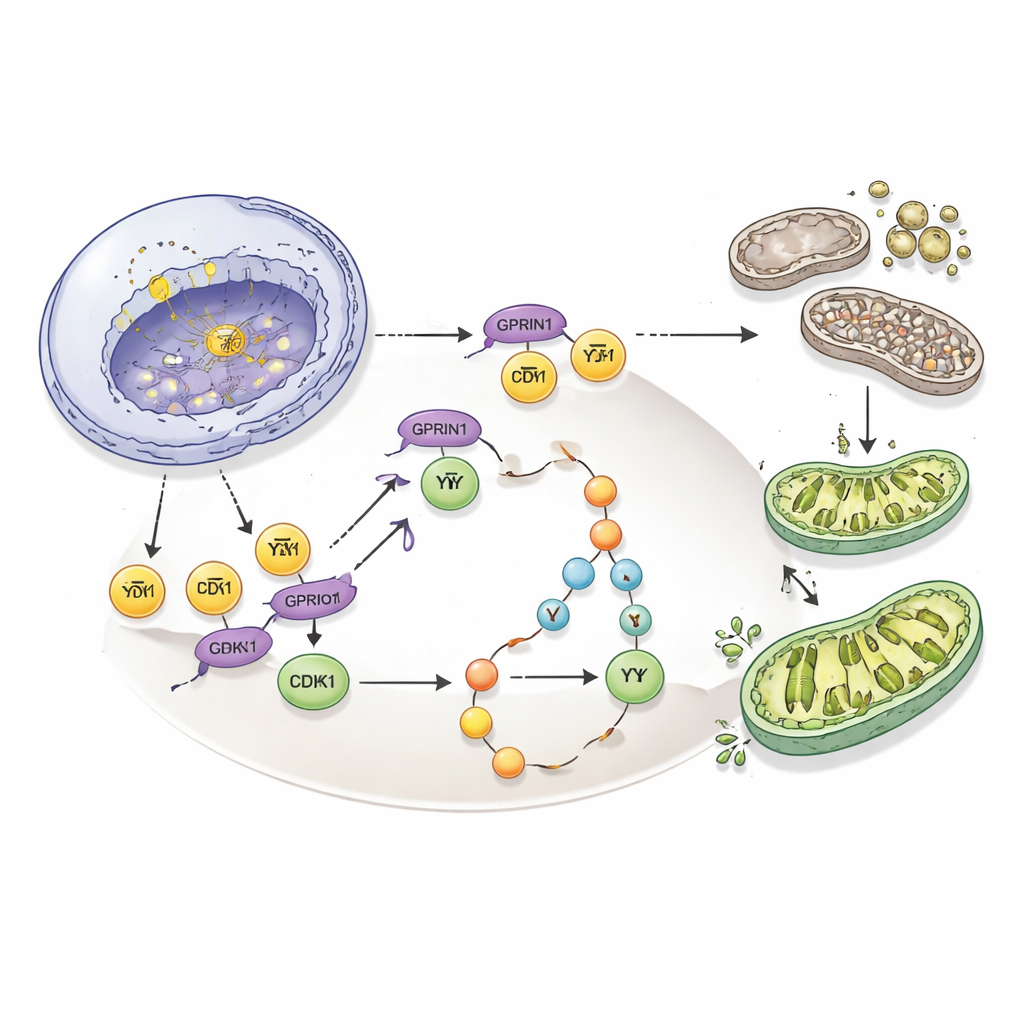
Eine Schwäche in eine Behandlungschance verwandeln
Zusammengefasst zeigen die Ergebnisse, dass GPRIN1 als zentraler Dirigent fungiert, der die Teilungsrate von Gallenblasenkrebszellen mit dem Zustand ihrer Mitochondrien verbindet. Durch die Stabilisierung von E2F1, die Verstärkung von CDK1 und die Aktivierung von PI3K/Akt baut GPRIN1 eine sich selbst verstärkende Schleife auf, die aggressives Tumorwachstum antreibt. Wichtig ist: Das Durchbrechen dieser Schleife — entweder durch Reduktion von GPRIN1, Silencing von CDK1 oder Blockade von PI3K — verlangsamte oder stoppte die Tumorbildung in Zellen und in Mäusen erheblich. Für Patientinnen und Patienten legt das nahe, dass die Messung von GPRIN1‑Spiegeln bei der Prognose helfen könnte und dass Medikamente, die auf die GPRIN1–CDK1–PI3K/Akt‑Achse zielen, eine gezieltere Behandlungsoption für eine der herausforderndsten Krebsarten des Verdauungssystems bieten könnten.
Zitation: Xu, C., Gong, Z., Ni, X. et al. Oncogenic GPRIN1 sustains proliferation and mitochondrial homeostasis via dual‑layer CDK1-PI3K/Akt signalling in gallbladder cancer. Cell Death Dis 17, 333 (2026). https://doi.org/10.1038/s41419-026-08550-2
Schlüsselwörter: Gallenblasenkrebs, GPRIN1, CDK1, mitochondriale Homöostase, PI3K Akt Signalgebung