Clear Sky Science · nl
Oncogene GPRIN1 onderhoudt proliferatie en mitochondriale homeostase via dubbele CDK1-PI3K/Akt-signaallaag bij galblaaskanker
Waarom dit onderzoek ertoe doet
Galblaaskanker is zeldzaam maar buitengewoon dodelijk, vaak pas ontdekt wanneer chirurgie of effectieve behandeling niet meer mogelijk is. Deze studie onthult een tot nu toe onbekend “master‑schakelaar”-eiwit, GPRIN1 genoemd, dat galblaaskankercellen helpt snel te vermenigvuldigen terwijl hun kleine energiecentrales — de mitochondriën — goed blijven functioneren. Het begrijpen van deze schakelaar kan de weg openen naar meer precieze, minder toxische therapieën voor een kanker waarvoor momenteel maar weinig opties bestaan.
Een verborgen drijver in een dodelijke kanker
De onderzoekers begonnen met het onderzoeken van tumorproeven van 100 patiënten met galblaaskanker. Ze vonden dat GPRIN1-niveaus veel hoger waren in tumoren dan in nabijgelegen gezond weefsel. Patiënten van wie de tumoren de meeste GPRIN1 vertoonden, hadden meer gevorderde ziekte en een kortere overleving, wat suggereert dat dit eiwit sterk samenhangt met hoe agressief de kanker wordt. In muismodellen groeiden tumoren die extra GPRIN1 produceerden sneller, wat het idee versterkt dat dit molecuul geen toeschouwer is maar een actieve motor van tumorgroei.
Cellulaire deling verbinden met cellulaire energie
Snelgroeiende kankercellen moeten tegelijk door de celcyclus heen en voldoende energie veiligstellen om hun expansie te ondersteunen. Het team toonde aan dat GPRIN1 centraal staat in deze coördinatie. Wanneer ze GPRIN1 verminderden in galblaaskankercellijnen, raakten de cellen energiearm, produceerden minder ATP en stapelden zich schadelijke reactieve zuurstofmoleculen op. Onder de microscoop leken hun mitochondriën opgezwollen en beschadigd. Tegelijkertijd stokte het normale opruimsysteem — mitofagie, dat defecte mitochondriën verwijdert. Sleutelproteïnen die deze opruiming starten, PINK1 en PARKIN, daalden, en beschadigde mitochondriën hoopten zich op. In zowel gekweekte cellen als muistumoren bleek GPRIN1 essentieel om de mitochondriën voldoende functioneel te houden om onophoudelijke groei mogelijk te maken.
De dubbele regelschakelaar op de celcyclusmachine
Dieper graven, gebruikten de wetenschappers grootschalige eiwit- en fosforyleringsschermen om te zoeken naar moleculen die veranderen wanneer GPRIN1 wordt verlaagd. Één viel op: CDK1, een centraal mechanisme dat cellen door de laatste stadia van deling duwt. GPRIN1 verhoogde zowel de hoeveelheid als de activiteit van CDK1. In de celkern bond GPRIN1 fysiek aan een ander eiwit, E2F1, en stabiliseerde het, waardoor E2F1 sterker het CDK1-gen kon aanzetten. Buiten de kern herschikte GPRIN1 de eiwitpartners rond CDK1, waardoor het werd weggestuurd van zijn natuurlijke remmen en richting zijn activatoren geleid. Deze “dubbele laag” van controle — op het gen en op het eiwit — creëert een hyperactieve CDK1‑motor die cellen snel de deling in jaagt.
Van moleculaire signalen naar mitochondriale balans
Het verhaal eindigde niet bij CDK1. Het team ontdekte dat dit overactieve CDK1 op zijn beurt een bekende overlevingsweg, PI3K/Akt, activeerde, die kankercellen helpt stress en celdood te weerstaan. Wanneer CDK1 werd geblokkeerd, kon GPRIN1 deze signaalweg niet langer inschakelen. En toen de onderzoekers een PI3K-remmer gebruikten, Buparlisib geheten, werd het voordeel van GPRIN1 tenietgedaan: celdeling vertraagde, ATP‑productie daalde naar normale waarden, oxidatieve stress nam toe en de mitofagie‑machinerie raakte verstoord. In wezen gebruikt GPRIN1 CDK1 om PI3K/Akt aan te zetten, die vervolgens zowel snelle celgroei als zorgvuldige instandhouding van mitochondriën coördineert, waardoor galblaaskankercellen een sterk overwicht in overleving krijgen.
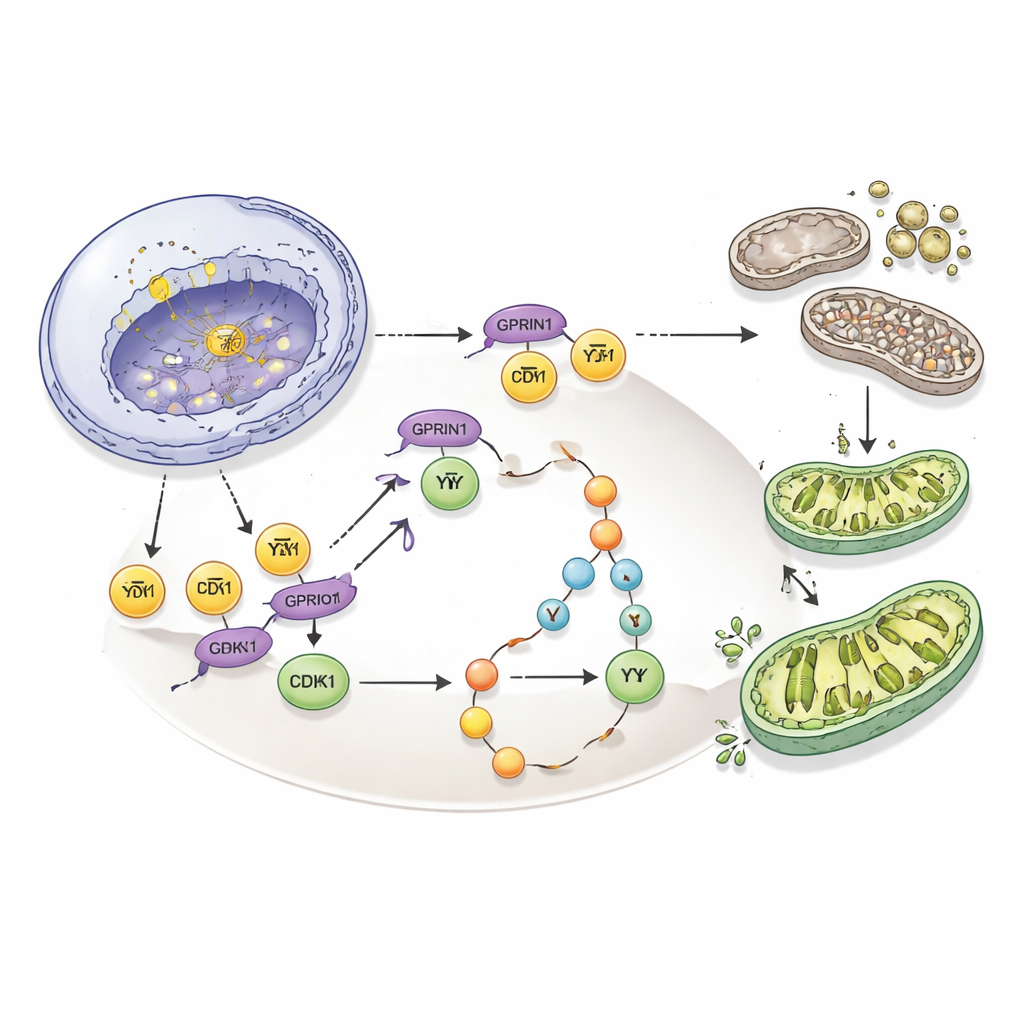
Een zwakte omzetten in een behandelingskans
Alles bij elkaar onthullen de bevindingen GPRIN1 als een centrale dirigent die koppelt hoe snel galblaaskankercellen delen aan hoe goed hun mitochondriën worden onderhouden. Door E2F1 te stabiliseren, CDK1 te versterken en PI3K/Akt in te schakelen, bouwt GPRIN1 een zichzelf versterkende lus die agressieve tumorgroei voedt. Belangrijk is dat het doorbreken van deze lus — hetzij door GPRIN1 te verminderen, CDK1 stil te leggen of PI3K te blokkeren — de tumorvorming in cellen en in muizen sterk vertraagde of zelfs stopzette. Voor patiënten suggereert dit dat het meten van GPRIN1‑niveaus kan helpen bij prognose, en dat medicijnen gericht op deze GPRIN1–CDK1–PI3K/Akt‑as mogelijk een meer gerichte manier bieden om een van de meest uitdagende kankers van het spijsverteringsstelsel te behandelen.
Bronvermelding: Xu, C., Gong, Z., Ni, X. et al. Oncogenic GPRIN1 sustains proliferation and mitochondrial homeostasis via dual‑layer CDK1-PI3K/Akt signalling in gallbladder cancer. Cell Death Dis 17, 333 (2026). https://doi.org/10.1038/s41419-026-08550-2
Trefwoorden: galblaaskanker, GPRIN1, CDK1, mitochondriale homeostase, PI3K Akt-signaalweg