Clear Sky Science · it
GPRIN1 oncogenico sostiene la proliferazione e l’omeostasi mitocondriale tramite una doppia regolazione CDK1-PI3K/Akt nel tumore della cistifellea
Perché questa ricerca è importante
Il carcinoma della cistifellea è raro ma estremamente letale, spesso scoperto troppo tardi per interventi chirurgici o terapie efficaci. Questo studio identifica una proteina finora sconosciuta che funge da “interruttore maestro”, chiamata GPRIN1, che permette alle cellule del tumore della cistifellea di moltiplicarsi rapidamente mantenendo allo stesso tempo operativi i loro piccoli impianti energetici — i mitocondri. Comprendere questo interruttore potrebbe aprire la strada a terapie più mirate e meno tossiche per un cancro che attualmente ha poche opzioni.
Un driver nascosto in un cancro letale
I ricercatori hanno cominciato analizzando campioni tumorali di 100 pazienti con carcinoma della cistifellea. Hanno riscontrato che i livelli di GPRIN1 erano molto più alti nei tumori rispetto ai tessuti sani circostanti. I pazienti i cui tumori mostravano la massima espressione di GPRIN1 avevano una malattia più avanzata e una sopravvivenza più breve, suggerendo che questa proteina sia strettamente legata all’aggressività del tumore. In modelli murini, i tumori ingegnerizzati per esprimere quantità aggiuntive di GPRIN1 crescevano più rapidamente, confermando che questa molecola non è un semplice spettatore ma un driver attivo della crescita tumorale.
Collegare la divisione cellulare al motore energetico
Le cellule tumorali in rapida crescita devono contemporaneamente procedere nel ciclo cellulare e garantirsi energia sufficiente per sostenere l’espansione. Il gruppo ha dimostrato che GPRIN1 è al centro di questa coordinazione. Quando hanno ridotto GPRIN1 in linee cellulari del tumore della cistifellea, le cellule hanno perso energia, prodotto meno ATP e accumulato molecole reattive dannose. Al microscopio i loro mitocondri apparivano rigonfi e danneggiati. Allo stesso tempo, il normale sistema di pulizia — la mitofagia, che rimuove mitocondri difettosi — si è bloccato. Proteine chiave che avviano questa pulizia, come PINK1 e PARKIN, sono diminuite e i mitocondri danneggiati si sono accumulati. Sia nelle cellule in coltura sia nei tumori nei topi, GPRIN1 si è rivelato essenziale per mantenere i mitocondri sufficientemente funzionali da alimentare una crescita incessante.
Il doppio interruttore sulla macchina del ciclo cellulare
Approfondendo, gli scienziati hanno usato schermaggi proteici e di fosforilazione su larga scala per cercare molecole che cambiavano quando GPRIN1 veniva ridotto. Una ha attirato l’attenzione: CDK1, un motore centrale che spinge le cellule attraverso le fasi finali della divisione. GPRIN1 aumentava sia la quantità sia l’attività di CDK1. Nel nucleo, GPRIN1 si legava fisicamente a un’altra proteina, E2F1, stabilizzandola e permettendo a E2F1 di attivare più efficacemente il gene CDK1. Fuori dal nucleo, GPRIN1 rimodellava i partner proteici intorno a CDK1, spingendolo lontano dai suoi freni naturali e verso i suoi attivatori. Questo controllo “a doppio strato” — sul gene e sulla proteina — crea un motore CDK1 iperattivo che spinge rapidamente le cellule alla divisione.
Dai segnali molecolari all’equilibrio mitocondriale
La storia non si è fermata a CDK1. Il gruppo ha scoperto che questo CDK1 iperattivo, a sua volta, attivava una via di sopravvivenza ben nota, PI3K/Akt, che aiuta le cellule tumorali a resistere allo stress e alla morte. Quando CDK1 veniva bloccato, GPRIN1 non riusciva più ad attivare questa via. E quando i ricercatori hanno usato un farmaco inibitore della PI3K chiamato Buparlisib, hanno annullato i vantaggi conferiti da GPRIN1: la divisione cellulare rallentava, la produzione di ATP tornava a livelli normali, lo stress ossidativo aumentava e il macchinario della mitofagia veniva perturbato. In sostanza, GPRIN1 utilizza CDK1 per accendere PI3K/Akt, che poi coordina sia la rapida crescita cellulare sia la manutenzione dei mitocondri, dando alle cellule del carcinoma della cistifellea un forte vantaggio di sopravvivenza.
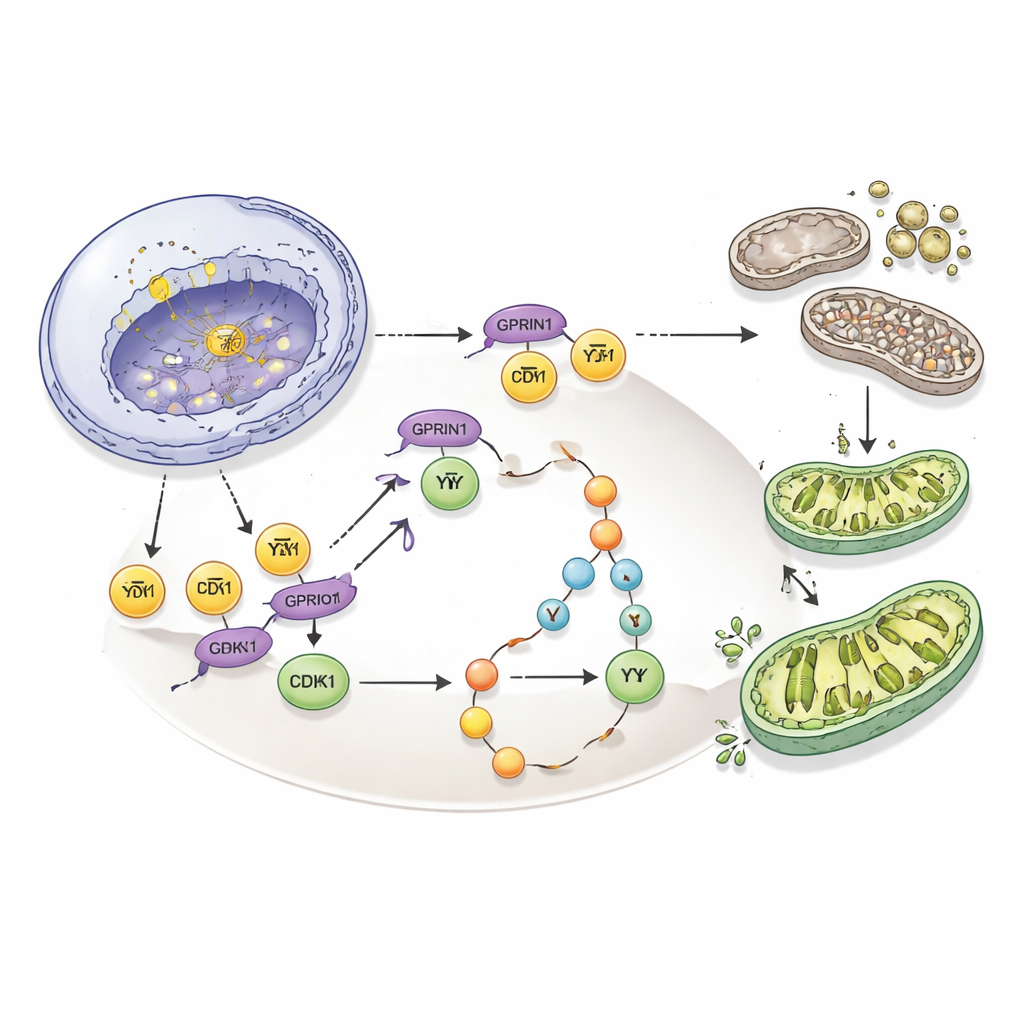
Trasformare una debolezza in un’opportunità terapeutica
Nel complesso, i risultati rivelano GPRIN1 come un conduttore centrale che collega la velocità di divisione delle cellule del carcinoma della cistifellea con l’efficacia della manutenzione mitocondriale. Stabilizzando E2F1, amplificando CDK1 e attivando PI3K/Akt, GPRIN1 costruisce un circuito auto‑alimentante che sostiene la crescita tumorale aggressiva. Importante, interrompere questo circuito — riducendo GPRIN1, silenziando CDK1 o bloccando PI3K — ha rallentato notevolmente o addirittura arrestato la formazione del tumore in cellule e nei topi. Per i pazienti, ciò suggerisce che misurare i livelli di GPRIN1 potrebbe aiutare a prevedere la prognosi e che farmaci mirati sull’asse GPRIN1–CDK1–PI3K/Akt potrebbero offrire un modo più selettivo per trattare uno dei tumori digestivi più difficili da affrontare.
Citazione: Xu, C., Gong, Z., Ni, X. et al. Oncogenic GPRIN1 sustains proliferation and mitochondrial homeostasis via dual‑layer CDK1-PI3K/Akt signalling in gallbladder cancer. Cell Death Dis 17, 333 (2026). https://doi.org/10.1038/s41419-026-08550-2
Parole chiave: cancro della cistifellea, GPRIN1, CDK1, omeostasi mitocondriale, segnalazione PI3K Akt