Clear Sky Science · ar
البروتين المسرطن GPRIN1 يدعم التكاثر والتوازن الميتوكوندري عبر إشارة مزدوجة المستوى CDK1-PI3K/Akt في سرطان المرارة
لماذا يهم هذا البحث
سرطان المرارة نادر لكنه قاتل للغاية، وغالبًا ما يُكتشف متأخرًا بحيث لا تكون الجراحة أو العلاجات الفعالة ممكنة. تكشف هذه الدراسة عن بروتين «مفتاح رئيسي» لم يُعرف سابقًا يُدعى GPRIN1، يساعد خلايا سرطان المرارة على التكاثر بسرعة مع الحفاظ على تشغيل محطات الطاقة الصغيرة داخل الخلايا — الميتوكوندريا — بشكل سليم. فهم هذا المفتاح قد يفتح الباب أمام علاجات أكثر دقة وأقل سمية لسرطان تفتقر حاليًا لخيارات كثيرة.
محرك خفي في سرطان قاتل
بدأ الباحثون بفحص عينات أورام من 100 مريض بسرطان المرارة. وجدوا أن مستويات GPRIN1 أعلى بكثير في الأورام مقارنة بالنسيج السليم المجاور. المرضى الذين أظهرت أورامهم أعلى مستويات GPRIN1 كان لديهم مرض أكثر تقدماً وبقياة أقصر، مما يشير إلى ارتباط هذا البروتين بشدة العدوانية السرطانية. في نماذج الفئران، نمت الأورام المصممة لإنتاج GPRIN1 إضافي بسرعة أكبر، مما يعزز فكرة أن هذه الجزيئة ليست مجرد مرافق بل سائق نشط لنمو الورم.
ربط انقسام الخلية بطاقة الخلية
تحتاج الخلايا السرطانية سريعة النمو إلى دفع دورة الخلية وتأمين طاقة كافية لدعم توسعها في الوقت نفسه. أظهر الفريق أن GPRIN1 يقع في مركز هذا التنسيق. عندما خفضوا مستوى GPRIN1 في خطوط خلايا سرطان المرارة، فقدت الخلايا طاقتها، أنتجت ATP أقل، وتراكمت فيها جزيئات تفاعل أكسجيني ضارة. تحت المجهر ظهرت ميتوكوندريا منتفخة ومتضررة. في الوقت نفسه، تعطل نظام التنظيف الطبيعي — الميتوفاجي الذي يزيل الميتوكوندريا المعطلة. انخفضت البروتينات الأساسية التي تطلق هذا التنظيف، PINK1 وPARKIN، وتراكمت الميتوكوندريا التالفة. في كل من الخلايا المستزرعة وأورام الفئران، برهن GPRIN1 على ضرورته للحفاظ على وظيفة الميتوكوندريا بما يكفي لتغذية النمو المتواصل.
مفتاح التحكم المزدوج في آلية دورة الخلية
بالغوص أعمق، استخدم العلماء شاشات واسعة النطاق للبروتين والفوسفوريلة للبحث عن جزيئات تتغير عند خفض GPRIN1. برز أحدها: CDK1، المحرك المركزي الذي يدفع الخلايا خلال المراحل النهائية من الانقسام. عزز GPRIN1 كلاً من كمية ونشاط CDK1. في نواة الخلية، ارتبط GPRIN1 جسديًا ببروتين آخر، E2F1، وقام بتثبيته، ما أتاح لـ E2F1 أن ينشط جين CDK1 بقوة أكبر. خارج النواة، أعاد GPRIN1 تشكيل شركاء البروتين حول CDK1، موجهًا إياه بعيدًا عن فراملها الطبيعية ونحو منشطاته. يؤدي هذا التحكم «ثنائي الطبقة» — على مستوى الجين والمستوى البروتيني — إلى محرك CDK1 مفرط النشاط يدفع الخلايا بسرعة نحو الانقسام.
من الإشارات الجزيئية إلى توازن الميتوكوندريا
لم تتوقف القصة عند CDK1. اكتشف الفريق أن هذا CDK1 المفرط النشاط بدوره فعّل مسار بقاء معروفًا، PI3K/Akt، الذي يساعد الخلايا السرطانية على مقاومة الإجهاد والموت. عندما تم حظر CDK1، لم يعد GPRIN1 قادرًا على تفعيل هذا المسار. وعندما استخدم الباحثون دواءً مثبطًا لـ PI3K يُدعى Buparlisib، أزال مزايا GPRIN1: تباطأ انقسام الخلايا، وعاد إنتاج ATP إلى المستويات الطبيعية، وازداد الإجهاد التأكسدي، وتعطلت آلية الميتوفاجي. باختصار، يستخدم GPRIN1 CDK1 لتشغيل PI3K/Akt، والذي ينسق بدوره النمو الخلوي السريع مع صيانة متأنية للميتوكوندريا، مما يمنح خلايا سرطان المرارة ميزة بقاء قوية.
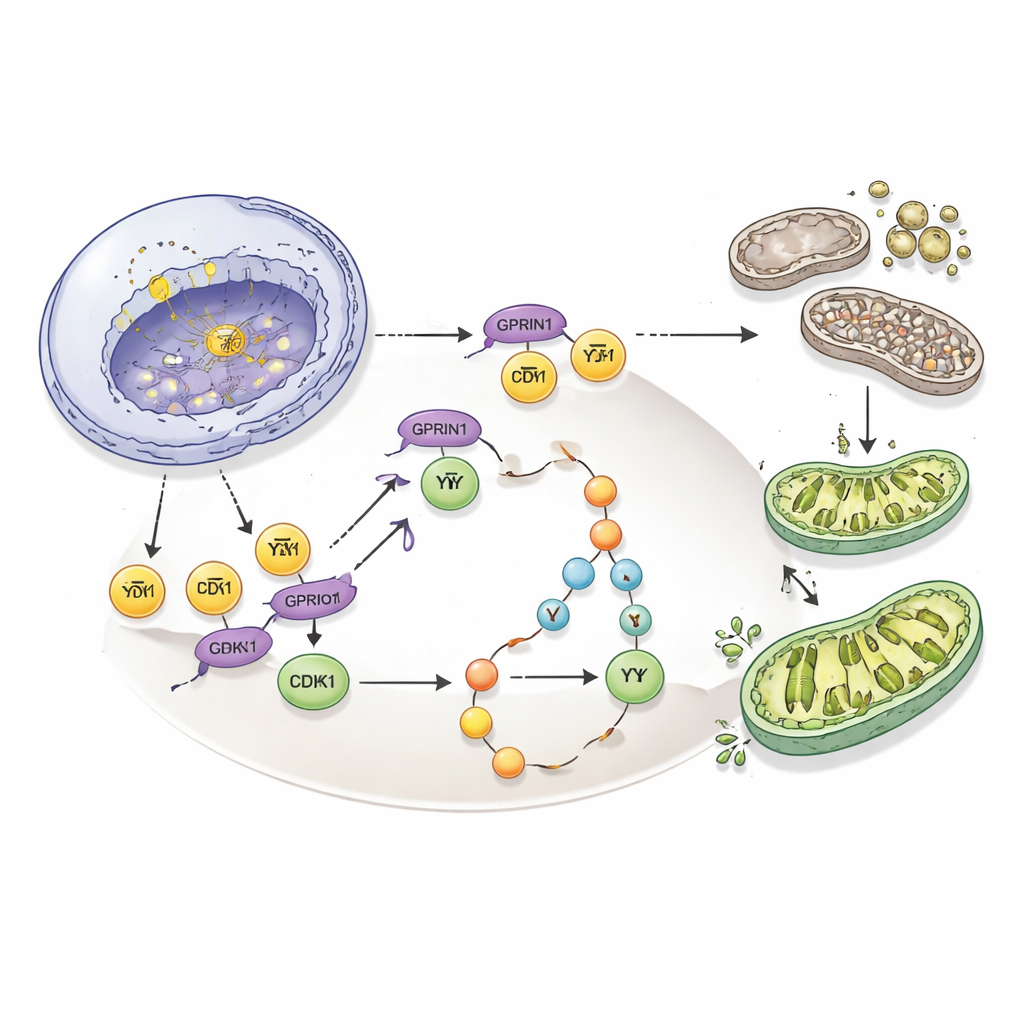
تحويل نقطة ضعف إلى فرصة علاجية
تظهر النتائج مجتمعة أن GPRIN1 يعمل كقائد مركزي يربط بين سرعة انقسام خلايا سرطان المرارة وجودة صيانة ميتوكوندرياتها. من خلال تثبيت E2F1، وتضخيم CDK1، وتفعيل PI3K/Akt، يبني GPRIN1 حلقة تعزيز ذاتي تغذي نمو الورم العدواني. والأهم من ذلك، أن كسر هذه الحلقة — سواء بتقليل GPRIN1، أو إسكات CDK1، أو حجب PI3K — أبطأ أو حتى أوقف تكوين الأورام في الخلايا والفئران. للمرضى، يشير ذلك إلى أن قياس مستويات GPRIN1 قد يساعد في توقع سير المرض، وأن الأدوية المستهدفة لمحور GPRIN1–CDK1–PI3K/Akt قد توفر طريقة أكثر توجيهًا لعلاج أحد أصعب سرطانات الجهاز الهضمي.
الاستشهاد: Xu, C., Gong, Z., Ni, X. et al. Oncogenic GPRIN1 sustains proliferation and mitochondrial homeostasis via dual‑layer CDK1-PI3K/Akt signalling in gallbladder cancer. Cell Death Dis 17, 333 (2026). https://doi.org/10.1038/s41419-026-08550-2
الكلمات المفتاحية: سرطان المرارة, GPRIN1, CDK1, التوازن الميتوكوندري, إشارة PI3K Akt