Clear Sky Science · pl
Hamowanie c‑FLIP wraz z leczeniem TRAIL hamuje aktywność komórek macierzystych raka prostaty
Dlaczego to badanie ma znaczenie dla mężczyzn i ich rodzin
Rak prostaty jest jednym z najczęstszych nowotworów u mężczyzn; choć wiele przypadków jest uleczalnych, agresywne postaci często nawrotują po standardowym leczeniu i mogą być śmiertelne. Głównym winowajcą bywa niewielka pula odporniejszych komórek, nazywanych czasem komórkami macierzystymi nowotworu, które potrafią przetrwać terapię i odbudować guz. W tym badaniu zbadano nowe podejście pozwalające zaatakować zarówno masę guza, jak i jego odporną „rdzeń” — poprzez wyłączenie kluczowego przełącznika przeżycia w komórkach nowotworowych i skojarzenie tego z istniejącymi lekami wywołującymi śmierć komórki.
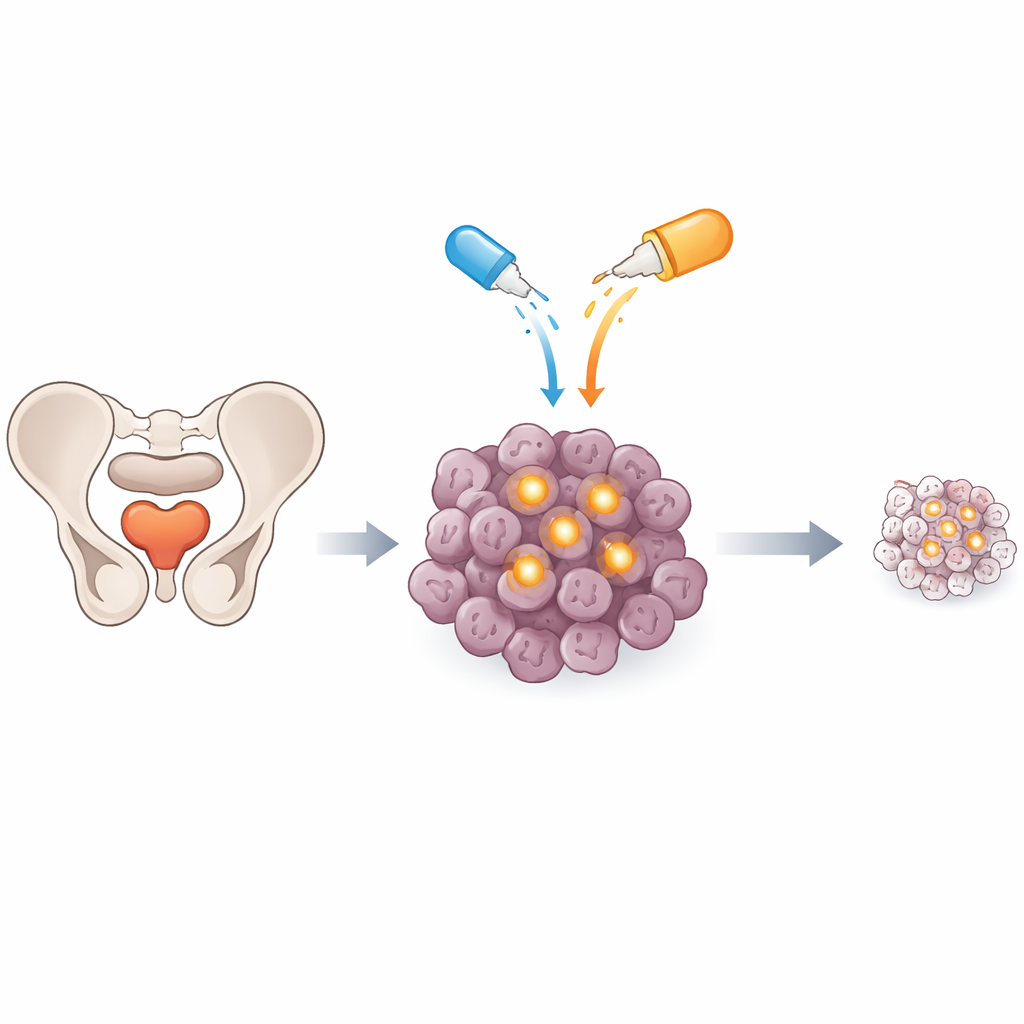
Ukryty przełącznik bezpieczeństwa w komórkach guza
Komórki nowotworowe często przetrwają, przebudowując normalne mechanizmy, które w przeciwnym razie prowadziłyby uszkodzone komórki do samozniszczenia. Ważnym elementem tej machiny jest białko zwane c‑FLIP, które działa w szlaku zwykle uruchamiającym „programowaną śmierć komórki”, gdy na powierzchnię komórki trafia sygnał zagrożenia. W rakach prostaty, zwłaszcza w zaawansowanej, opornej na leczenie postaci, poziomy c‑FLIP są często podwyższone i pełnią rolę blokującego sygnały śmierci przełącznika bezpieczeństwa. Naukowcy sprawdzili, czy wyłączenie tego przełącznika małym cząsteczkom, oznaczonym jako OH14, może uczynić komórki raka prostaty bardziej wrażliwymi na naturalne białko wywołujące śmierć — TRAIL — lub na chemioterapeutyk docetaksel.
Testowanie nowego połączenia leków w laboratorium
Początkowo zespół pracował na ustalonych liniach komórek raka prostaty hodowanych in vitro, w tym na komórkach normalnie opornych na TRAIL. Samodzielnie zarówno OH14, jak i TRAIL miały ograniczony wpływ na śmierć komórek. Jednak przy krótkiej ekspozycji na OH14, a następnie leczeniu TRAIL, obserwowano silną falę programowanej śmierci komórki, którą dało się zablokować inhibitorem kaspaz, co potwierdza, że ścieżka samobójcza komórki została rzeczywiście uruchomiona. Przeżywające komórki zaszczepiono następnie w bardzo niskich liczbach, aby sprawdzić, ile z nich jest w stanie utworzyć kolonie — co stanowi przybliżenie aktywności komórek macierzystych lub progenitorowych. Kombinacja OH14 i TRAIL wyraźnie zmniejszyła tworzenie kolonii w porównaniu z każdym leczeniem osobno, sugerując, że podejście to uderza nie tylko w zwykłe komórki guza, lecz także w bardziej niebezpieczne, przypominające komórki macierzyste.
Włączenie guzów pacjentów i modeli zwierzęcych
Następnie badacze wyszli poza standardowe linie komórkowe i pracowali z komórkami wyizolowanymi bezpośrednio z tkanek prostaty mężczyzn, obejmującymi zarówno łagodne rozrosty, jak i guzy o różnym stopniu zaawansowania. Również tutaj OH14 skuteczniej zmniejszał przeżywalność komórek nowotworowych niż sam TRAIL, a połączenie obu czynników dodatkowo obniżało żywotność i wzrost kolonii, szczególnie w guzach wyższej złośliwości. Aby sprawdzić, czy ma to znaczenie in vivo, użyto myszy niosących guzy pochodzące od pacjentów, które odzwierciedlają zaawansowaną, oporną na hormony chorobę. Komórki guzowe pobrano, potraktowano poza organizmem OH14, TRAIL lub oboma jednocześnie, a potem przeszczepiono do nowych myszy w różnych dawkach komórek. Tylko leczenie skojarzone znacząco ograniczyło zdolność tych komórek do zapoczątkowania nowych guzów, wskazując na utratę komórek inicjujących nowotwór o charakterze macierzystym.
Celowanie w zaawansowanego i opornego na leki raka prostaty
Analiza dużych zbiorów danych genetycznych wykazała, że w miarę postępu raka prostaty do bardziej agresywnych, opornych na kastrację postaci, następuje przesunięcie równowagi między c‑FLIP a TRAIL: poziomy c‑FLIP zwykle rosną, a TRAIL maleje, szczególnie w najtrudniejszych do leczenia podtypach pozbawionych standardowych celów hormonalnych. Wzorzec ten zgadza się z koncepcją, że te guzy coraz bardziej zależą od przełącznika bezpieczeństwa c‑FLIP, aby przetrwać. W eksperymentach na zwierzętach połączenie OH14 z chemioterapeutykiem docetaksel zmniejszało guzy oporne na kastrację znacznie bardziej niż sam docetaksel, bez widocznego wzrostu toksyczności. W modelach komórkowych, które już stały się oporne na docetaksel, blokada c‑FLIP nadal osłabiała komórki i w pewnym stopniu przywracała wrażliwość na TRAIL, choć oporność nie została całkowicie odwrócona.
Co to może oznaczać dla przyszłych terapii
Podsumowując, badanie sugeruje, że leki wyłączające c‑FLIP mogłyby zwiększyć skuteczność istniejących terapii, takich jak preparaty oparte na TRAIL czy docetaksel, szczególnie wobec agresywnych, zaawansowanych raków prostaty, dla których obecnie dostępnych jest niewiele skutecznych opcji. Atakując zarówno masę guza, jak i mniejszą pulę komórek o cechach macierzystych napędzających nawrót, ta strategia ma na celu nie tylko zmniejszenie rozmiaru guzów, lecz także zapobieganie ich powrotom. Choć sam OH14 będzie wymagał dalszego udoskonalenia i badań bezpieczeństwa przed zastosowaniem w klinice, praca ta daje wyraźny plan dla terapii skojarzonych, które mogłyby w przyszłości zapewnić mężczyznom z zaawansowanym rakiem prostaty dłuższą kontrolę nad chorobą.
Cytowanie: Turnham, D.J., French, R., Frame, F.M. et al. Inhibition of c-FLIP alongside TRAIL treatment suppresses prostate cancer stem cell activity. Br J Cancer 134, 1300–1310 (2026). https://doi.org/10.1038/s41416-026-03359-4
Słowa kluczowe: rak prostaty, inhibicja c‑FLIP, terapia TRAIL, komórki macierzyste nowotworu, oporność na docetaksel