Clear Sky Science · fr
Inhibition de c-FLIP associée au traitement par TRAIL supprime l'activité des cellules souches du cancer de la prostate
Pourquoi cette recherche est importante pour les hommes et leurs familles
Le cancer de la prostate est l’un des cancers les plus fréquents chez l’homme et, si de nombreux cas sont traitables, les formes agressives réapparaissent souvent après les traitements standards et peuvent être mortelles. Un des responsables principaux est une petite réserve de cellules plus résistantes, parfois appelées cellules souches cancéreuses, qui survivent aux traitements et reconstruisent la tumeur. Cette étude explore une nouvelle façon d’attaquer à la fois la masse tumorale et ce noyau résilient en désactivant un commutateur de survie clé à l’intérieur des cellules cancéreuses et en l’associant à des médicaments existants qui déclenchent la mort cellulaire.
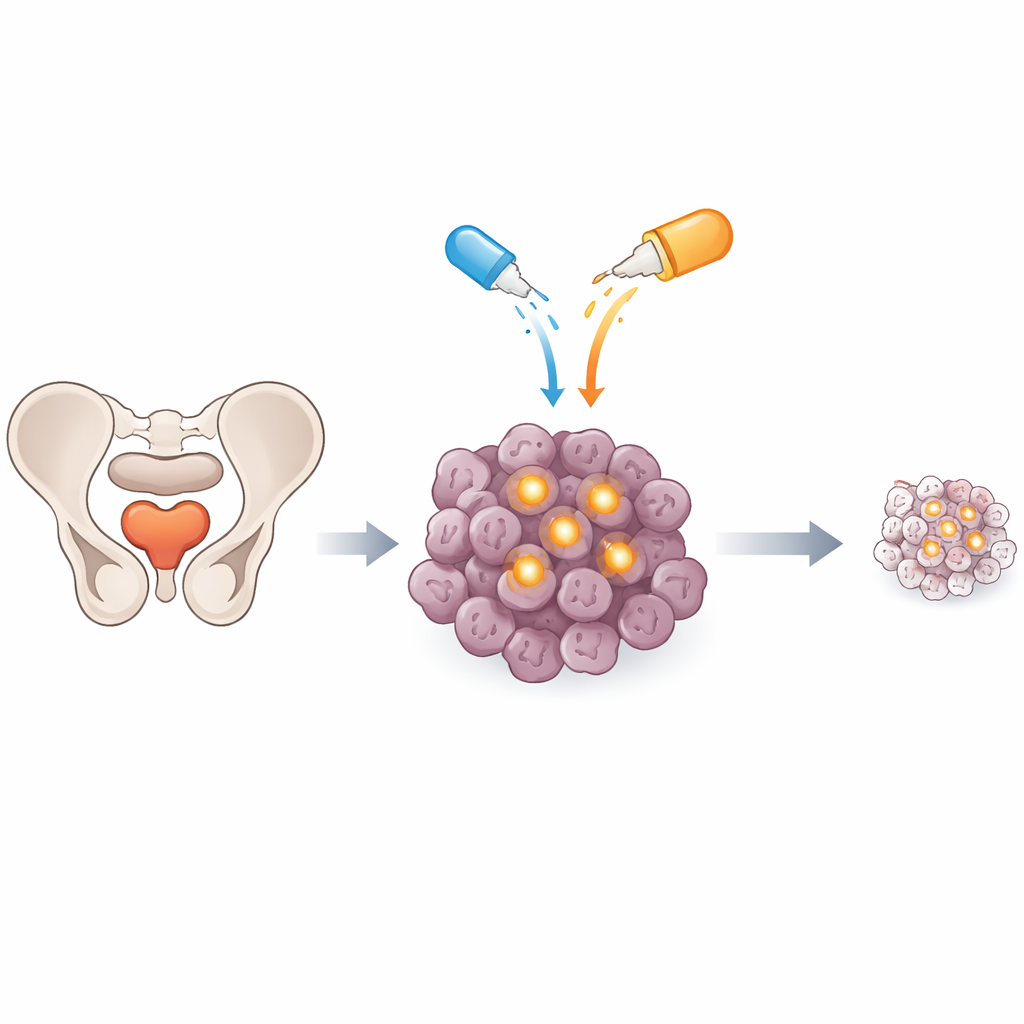
Un commutateur de sécurité caché dans les cellules tumorales
Les cellules cancéreuses survivent souvent en réorientant la machinerie normale qui conduirait autrement les cellules endommagées à s’autodétruire. Une composante importante de cette machinerie est une protéine appelée c‑FLIP, qui intervient dans une voie qui active normalement la « mort cellulaire programmée » lorsqu’un signal de danger arrive à la surface cellulaire. Dans les tumeurs prostatiques, en particulier dans les maladies avancées résistantes au traitement, c‑FLIP a tendance à être élevé et agit comme un interrupteur de sécurité qui bloque les signaux de mort. Les chercheurs ont cherché à savoir si désactiver cet interrupteur avec une petite molécule, nommée OH14, pouvait rendre les cellules du cancer de la prostate beaucoup plus vulnérables à une protéine signal naturelle induisant la mort connue sous le nom de TRAIL ou au médicament de chimiothérapie docétaxel.
Tester la nouvelle combinaison médicamenteuse en laboratoire
D’abord, l’équipe a travaillé avec des lignées cellulaires établies de cancer de la prostate cultivées en boîte, y compris des cellules normalement résistantes à TRAIL. Pris séparément, OH14 ou TRAIL avaient un impact limité sur la mort cellulaire. Mais lorsque les cellules ont été brièvement exposées à OH14 puis traitées par TRAIL, une forte vague de mort cellulaire programmée a été observée, bloquée par un inhibiteur de caspases, confirmant que la voie d’autodestruction était bien activée. Les cellules survivantes ont ensuite été ensemencées à très faible densité pour évaluer combien pouvaient former des colonies, un proxy de l’activité des cellules souches ou progénitrices cancéreuses. La combinaison OH14 + TRAIL a fortement réduit la formation de colonies comparée à chaque traitement pris isolément, suggérant que l’approche frappe non seulement les cellules tumorales ordinaires mais aussi les cellules de type souches plus dangereuses.
Intégrer des tumeurs de patients et des modèles animaux
Les chercheurs sont ensuite allés au‑delà des lignées cellulaires standards pour travailler sur des cellules issues directement de tissus prostatiques d’hommes, incluant des hyperplasies bénignes et des cancers de gravité variable. Là encore, OH14 a réduit la survie des cellules cancéreuses plus efficacement que TRAIL seul, et la combinaison des deux a encore diminué la viabilité et la croissance des colonies, en particulier dans les tumeurs de grade plus élevé. Pour savoir si cela avait un impact in vivo, ils ont utilisé des souris porteuses de tumeurs prostatiques dérivées de patients, mimant une maladie avancée résistante aux hormones. Les cellules tumorales ont été prélevées, traitées hors du corps par OH14, TRAIL ou les deux, puis transplantées dans de nouvelles souris à différentes doses cellulaires. Seul le traitement combiné a nettement réduit la capacité de ces cellules à initier de nouvelles tumeurs, indiquant une perte importante des cellules initiatrices de tumeur de type souches.
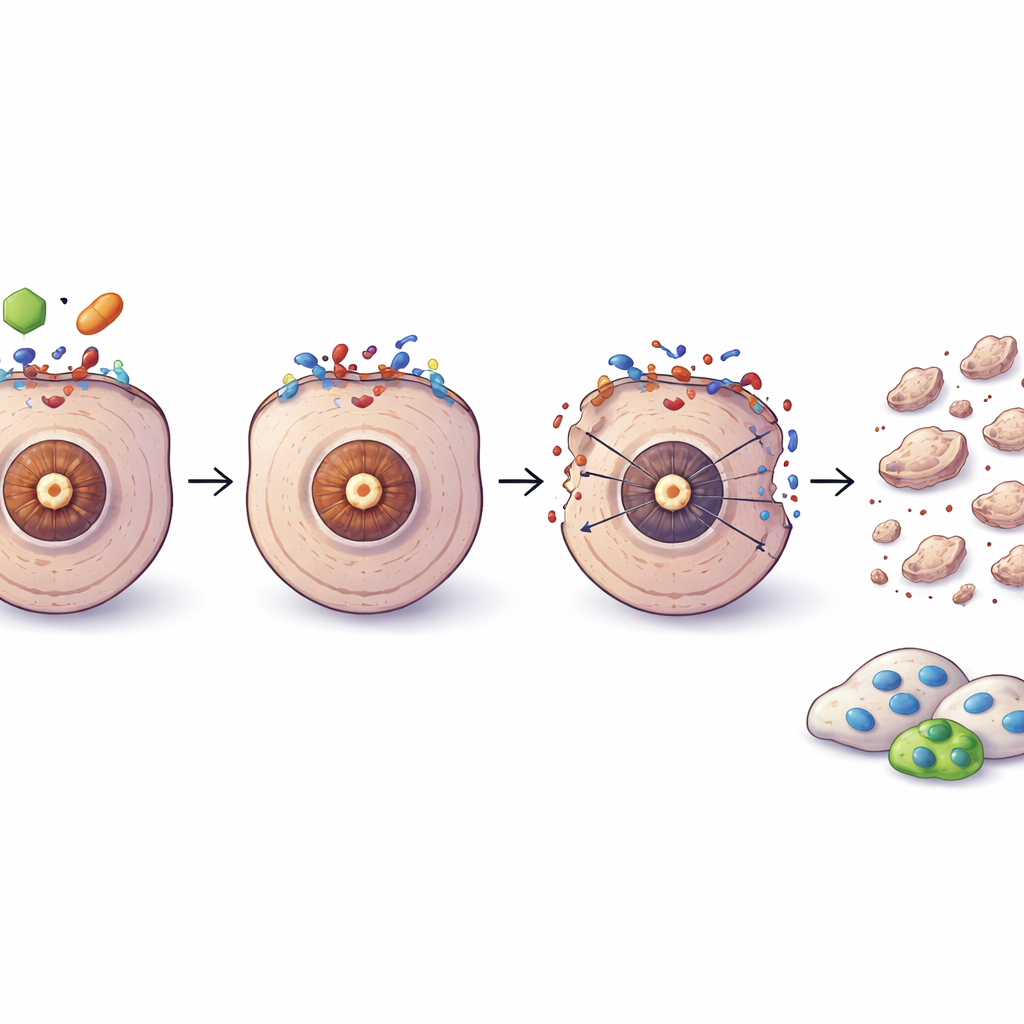
Viser les cancers de la prostate avancés et résistants aux médicaments
L’analyse de larges jeux de données génétiques a montré qu’à mesure que le cancer de la prostate progresse vers des formes plus agressives et résistantes à la castration, l’équilibre entre c‑FLIP et TRAIL se modifie : les niveaux de c‑FLIP ont tendance à augmenter tandis que ceux de TRAIL diminuent, notamment dans les sous‑types les plus difficiles à traiter qui manquent de cibles hormonales standards. Ce schéma s’accorde avec l’idée que ces tumeurs deviennent de plus en plus dépendantes du commutateur de sécurité c‑FLIP pour survivre. Dans des expériences animales, la combinaison d’OH14 avec le docétaxel a réduit des tumeurs résistantes à la castration bien plus que le docétaxel seul, sans toxicité ajoutée évidente. Dans des modèles cellulaires déjà résistants au docétaxel, le blocage de c‑FLIP a tout de même affaibli les cellules et restauré modestement la sensibilité à TRAIL, bien que la résistance n’ait pas été complètement inversée.
Ce que cela pourrait signifier pour les traitements futurs
Globalement, l’étude suggère que des médicaments désactivant c‑FLIP pourraient rendre les traitements existants comme les agents basés sur TRAIL et le docétaxel beaucoup plus efficaces, en particulier contre les cancers de la prostate agressifs et avancés qui disposent aujourd’hui de peu d’options. En visant à la fois les cellules tumorales majoritaires et la petite population de cellules de type souches qui provoquent les récidives, cette stratégie vise non seulement à réduire les tumeurs, mais aussi à empêcher leur retour. Si OH14 lui‑même nécessitera encore des optimisations et des tests de sécurité avant d’atteindre la clinique, ce travail fournit une feuille de route claire pour des thérapies combinatoires qui pourraient un jour offrir aux hommes atteints d’un cancer de la prostate avancé un contrôle durable de leur maladie.
Citation: Turnham, D.J., French, R., Frame, F.M. et al. Inhibition of c-FLIP alongside TRAIL treatment suppresses prostate cancer stem cell activity. Br J Cancer 134, 1300–1310 (2026). https://doi.org/10.1038/s41416-026-03359-4
Mots-clés: cancer de la prostate, inhibition de c-FLIP, thérapie TRAIL, cellules souches cancéreuses, résistance au docétaxel