Clear Sky Science · ar
تثبيط c-FLIP إلى جانب علاج TRAIL يكبح نشاط خلايا جذع سرطان البروستاتا
لماذا تهم هذه الدراسة الرجال وعائلاتهم
يعد سرطان البروستاتا من أكثر أنواع السرطان شيوعًا بين الرجال، وعلى الرغم من أن العديد من الحالات قابلة للعلاج، فإن الأشكال الشديدة غالبًا ما تعاود الظهور بعد العلاجات القياسية وقد تكون مميتة. سبب رئيسي لذلك هو احتياطي صغير من الخلايا الأقوى، التي يُطلق عليها أحيانًا خلايا جذع السرطان، والتي يمكن أن تبقى على قيد الحياة بعد العلاج وتعيد بناء الورم. تستكشف هذه الدراسة طريقة جديدة لمهاجمة كل من كتلة الورم ونواته المقاومة عن طريق تعطيل مفتاح بقاء رئيسي داخل خلايا السرطان ومزج ذلك مع أدوية محفزة للموت المتاحة حاليًا.
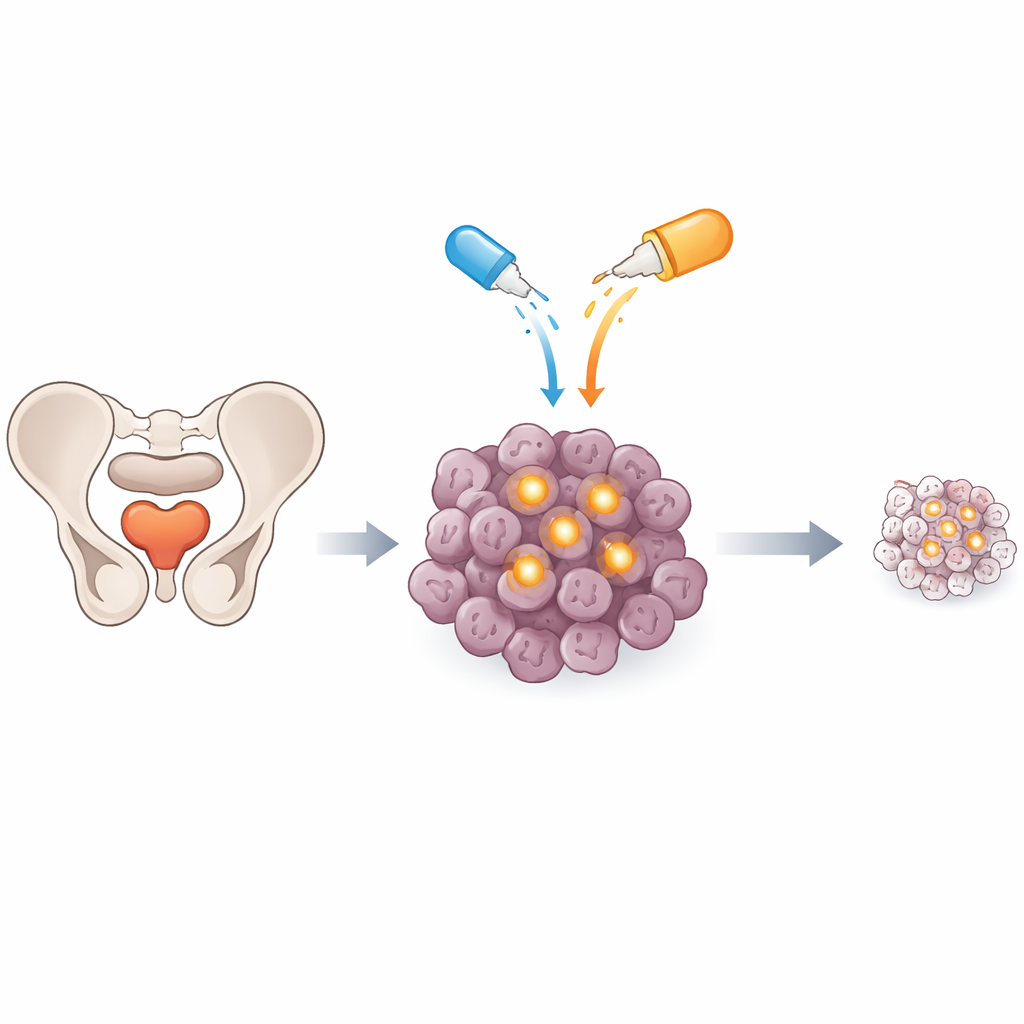
مفتاح أمان مخفي داخل خلايا الورم
غالبًا ما تبقى خلايا السرطان على قيد الحياة عبر إعادة توصيل الآليات الطبيعية التي كانت ستجعل الخلايا التالفة تنتحر. جزء مهم من هذه الآلية هو بروتين يُدعى c-FLIP، الذي يعمل في مسار عادةً ما يشغّل "الموت المبرمج للخلايا" عند وصول إشارة خطر إلى سطح الخلية. في أورام البروستاتا، خصوصًا في المرض المتقدم المقاوم للعلاج، يرتفع مستوى c-FLIP ويعمل كمفتاح أمان يمنع إشارات الموت. تساءل الباحثون عما إذا كان إيقاف هذا المفتاح بمركب جزيئي صغير يسمى OH14 يمكن أن يجعل خلايا سرطان البروستاتا أكثر عرضة بكثير لإشارة موت طبيعية تُدعى TRAIL أو لمادة العلاج الكيميائي دوسيتاكسيل.
اختبار مزيج الدواء الجديد في المختبر
أولاً، عمل الفريق على خطوط خلايا سرطان البروستاتا المزروعة في أطباق، بما في ذلك خلايا كانت مقاومة عادةً لـTRAIL. بمفردها، كان لكل من OH14 أو TRAIL تأثير محدود على موت الخلايا. لكن عندما عُرضت الخلايا لفترة وجيزة لـOH14 ثم عُولجت بـTRAIL، حدثت موجة قوية من الموت المبرمج للخلايا، ويمكن حجبها بمثبط الكاسباز، مما يؤكد أن مسار الانتحار الخلوي قد تم تفعيله فعلاً. ثم بُذرت الخلايا الناجية بأعداد منخفضة جدًا لمعرفة عددها الذي يمكن أن ينمو إلى مستعمرات، وهو مقياس لنشاط خلايا الجذع أو الخلايا الأولية السرطانية. قلل مزيج OH14 وTRAIL تشكيل المستعمرات بشكل حاد مقارنة بكل علاج على حدة، ما يشير إلى أن النهج يؤثر ليس فقط على الخلايا الورمية الاعتيادية بل أيضًا على الخلايا الشبيهة بالجذع الأكثر خطورة.
إدخال أورام المرضى والنماذج الحيوانية في الصورة
انتقل الباحثون بعد ذلك إلى ما هو أبعد من خطوط الخلايا القياسية إلى خلايا نُمت مباشرة من أنسجة بروستاتا بشرية، بما في ذلك أورام حميدة وسرطانات بمستويات شدّة مختلفة. هنا أيضًا، قلّل OH14 بقاء الخلايا السرطانية بفاعلية أكبر من TRAIL بمفرده، وأدى الجمع بينهما إلى خفض إضافي في القابلية للبقاء ونمو المستعمرات، لا سيما في الأورام عالية الدرجة. لرؤية ما إذا كان لذلك أثر في كائن حي، استخدموا فئرانًا حاملة لأورام مستمدة من مرضى تحاكي المرض المتقدم المقاوم للهرمونات. جُمعت خلايا الورم، وعُولجت خارج الجسم بـOH14 أو TRAIL أو كليهما، ثم نُقلت إلى فئران جديدة بأعداد خلوية مختلفة. فقط العلاج المركب خفّض بشكل ملحوظ قدرة هذه الخلايا على بدء أورام جديدة، مما يدل على فقدان كبير للخلايا ذات القدرة على بدء الورم والمشبَّهة بالجذع.
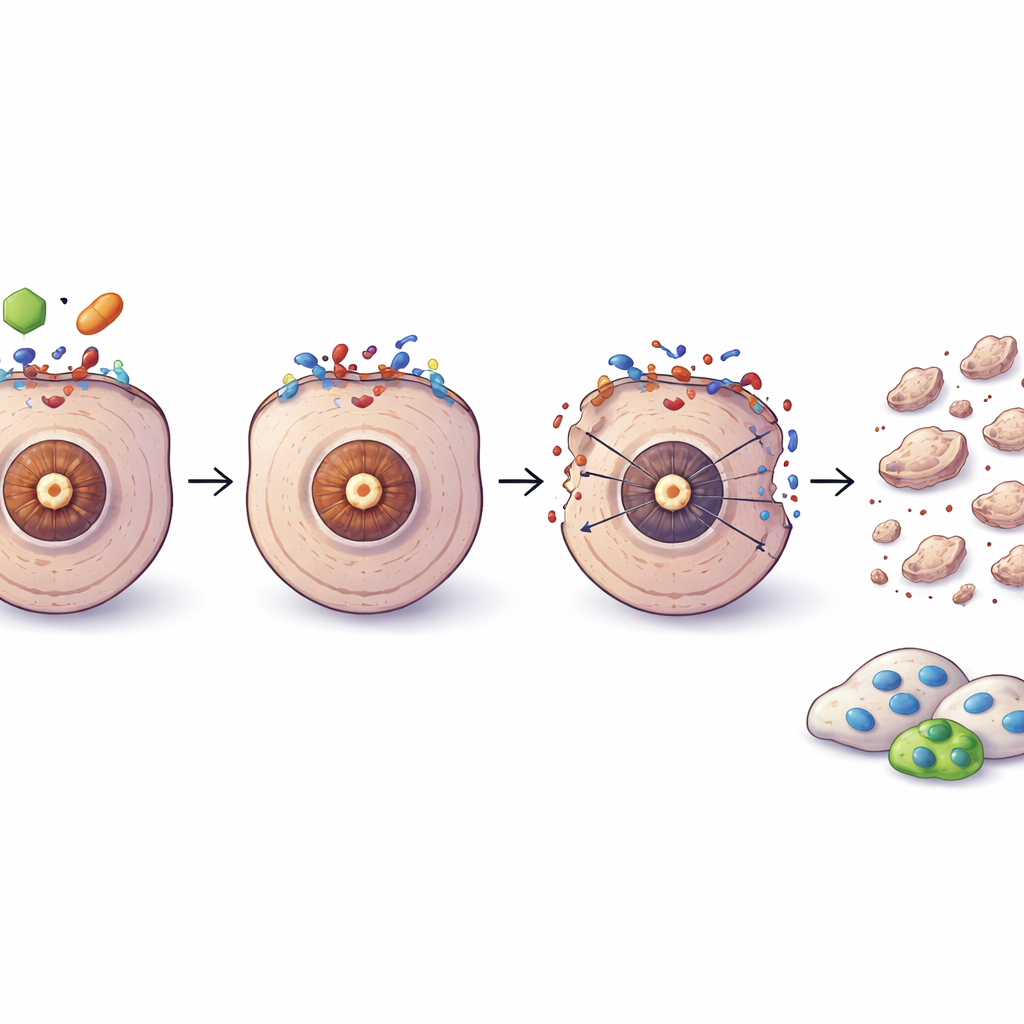
استهداف سرطان البروستاتا المتقدم والمقاوم للأدوية
أظهر تحليل مجموعات بيانات جينية كبيرة أنه مع تقدم سرطان البروستاتا إلى أشكال أكثر عدوانية ومقاومة للخصي، يتغير التوازن بين c-FLIP وTRAIL: تميل مستويات c-FLIP للارتفاع بينما تنخفض مستويات TRAIL، خصوصًا في الأنماط الأصعب علاجًا التي تفتقر إلى أهداف هرمونية قياسية. يتوافق هذا النمط مع فكرة أن هذه الأورام تصبح أكثر اعتمادًا على مفتاح الأمان c-FLIP للبقاء. في تجارب حيوانية، أدى الجمع بين OH14 ودواء العلاج الكيميائي دوسيتاكسيل إلى انكماش أورام مقاومة للخصي أكثر بكثير من دوسيتاكسيل بمفرده، دون سميّة ظاهرة إضافية. في نماذج خلوية أصبحت مقاومة مسبقًا للدوسيتاكسيل، استمر حجب c-FLIP في إضعاف الخلايا وأعاد بشكل طفيف الحساسية تجاه TRAIL، رغم أن المقاومة لم تُعكس تمامًا.
ماذا قد يعني هذا للعلاجات المستقبلية
بشكل عام، تشير الدراسة إلى أن الأدوية التي تعطل c-FLIP قد تجعل العلاجات الحالية مثل العوامل المعتمدة على TRAIL والدوسيتاكسيل أكثر فعالية، لا سيما ضد سرطانات البروستاتا المتقدمة التي لا تملك حاليًا خيارات جيدة كثيرة. من خلال استهداف كل من خلايا الورم الكتلية والمجموعة الأصغر من الخلايا الشبيهة بالجذع التي تقود الانتكاس، يهدف هذا الاستراتيجية ليس فقط إلى تصغير الأورام، بل إلى منع عودتها. بينما سيحتاج OH14 نفسه إلى مزيد من التحسين واختبارات السلامة قبل الوصول إلى العيادة، توفّر هذه العمل خطة واضحة للعلاجات المركبة التي قد تمنح يومًا ما الرجال المصابين بسرطان البروستاتا المتقدم سيطرة أطول أمدًا على مرضهم.
الاستشهاد: Turnham, D.J., French, R., Frame, F.M. et al. Inhibition of c-FLIP alongside TRAIL treatment suppresses prostate cancer stem cell activity. Br J Cancer 134, 1300–1310 (2026). https://doi.org/10.1038/s41416-026-03359-4
الكلمات المفتاحية: سرطان البروستاتا, تثبيط c-FLIP, علاج TRAIL, خلايا جذع السرطان, مقاومة الدوسيتاكسيل