Clear Sky Science · nl
Remming van c-FLIP samen met TRAIL-behandeling onderdrukt stamcelactiviteit bij prostaatkanker
Waarom dit onderzoek ertoe doet voor mannen en hun families
Prostaatkanker is een van de meest voorkomende kankers bij mannen. Hoewel veel gevallen behandelbaar zijn, treden bij agressieve vormen vaak terugvallen op na standaardtherapieën en kunnen ze dodelijk zijn. Een belangrijke boosdoener is een kleine voorraad hardere cellen, vaak aangeduid als kankerstamcellen, die een behandeling kunnen overleven en de tumor kunnen heropbouwen. Deze studie onderzoekt een nieuwe manier om zowel de bulk van de tumor als deze veerkrachtige kern aan te pakken door een sleutelschakelaar voor overleving in de kankercellen uit te schakelen en dat te combineren met bestaande middelen die celdood opwekken.
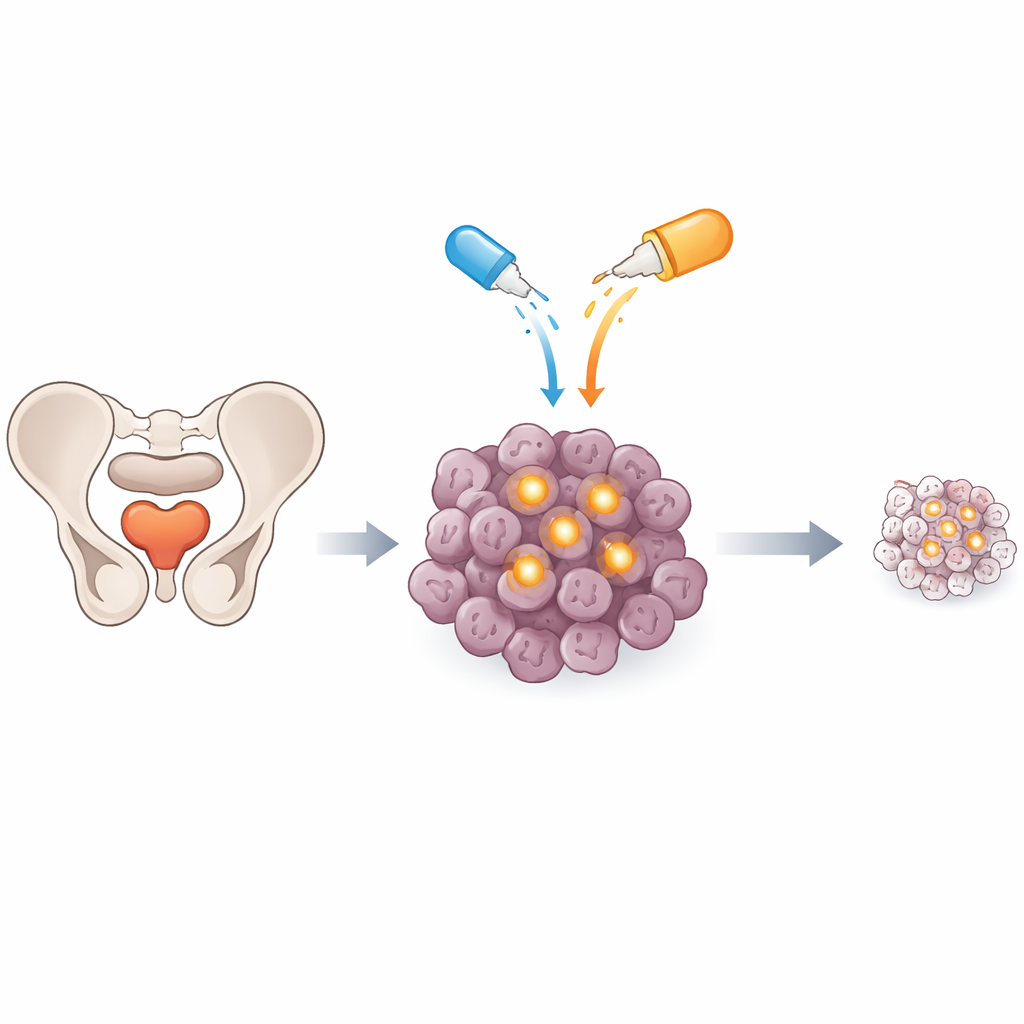
Een verborgen veiligheidsschakelaar in tumorcellen
Kankercellen blijven vaak in leven door de normale mechanismen zodanig te herschakelen dat beschadigde cellen niet zelfdestructief worden. Een belangrijk onderdeel van dit mechanisme is een eiwit genaamd c‑FLIP, dat in een route zit die normaal gesproken "geprogrammeerde celdood" activeert wanneer een alarmsignaal het celoppervlak bereikt. In prostaattumoren, vooral in gevorderde, therapieresistente ziektes, is c‑FLIP vaak verhoogd en fungeert het als een veiligheidsschakelaar die doodssignalen blokkeert. De onderzoekers vroegen zich af of het uitschakelen van deze schakelaar met een kleinmolecuulmedicijn, genoemd OH14, prostaatkankercellen veel kwetsbaarder kon maken voor een natuurlijk doodssignaleiwit dat TRAIL heet of voor het chemotherapiemiddel docetaxel.
Het nieuwe medicijncombinatie in het laboratorium testen
Eerst werkte het team met gevestigde prostaatkankercellijnen gekweekt in schaaltjes, inclusief cellen die normaal gesproken resistent waren tegen TRAIL. Op zichzelf hadden OH14 of TRAIL beperkt effect op celdood. Maar wanneer cellen kort werden blootgesteld aan OH14 en vervolgens aan TRAIL, trad er een sterke golf van geprogrammeerde celdood op, die geblokkeerd kon worden door een caspase-remmer, wat bevestigt dat de zelfmoordroute echt werd geactiveerd. Overlevende cellen werden daarna bij zeer lage aantallen uitgezaaid om te zien hoeveel kunnen uitgroeien tot kolonies, een proxy voor kankerstam- of voorlopercelactiviteit. De combinatie van OH14 en TRAIL verminderde de kolonievorming sterk vergeleken met een van beide behandelingen alleen, wat suggereert dat de aanpak niet alleen gewone tumorcellen treft maar ook de gevaarlijkere stamachtige cellen.
Patienttumoren en diermodellen in beeld brengen
Vervolgens gingen de onderzoekers verder dan standaard cellijnen en gebruikten cellen die rechtstreeks uit prostaatweefsel van mannen waren gekweekt, inclusief goedaardige vergrotingen en kankers van verschillende ernst. Ook hier verlaagde OH14 het overleven van kankercellen effectiever dan TRAIL alleen, en de combinatie van de twee verlaagde de levensvatbaarheid en koloniegroei nog verder, met name in hooggradige tumoren. Om te onderzoeken of dit in een levend lichaam relevant kon zijn, gebruikten ze muizen met patiënt-afgeleide prostaattumoren die gevorderde, hormoonresistente ziekte nabootsen. Tumorcellen werden geoogst, buiten het lichaam behandeld met OH14, TRAIL of beide, en vervolgens opnieuw getransplanteerd in nieuwe muizen bij verschillende celbelastingen. Alleen de combinatiebehandeling verminderde sterk het vermogen van deze cellen om nieuwe tumoren te starten, wat wijst op een groot verlies van tumor-initierende, stamachtige cellen.
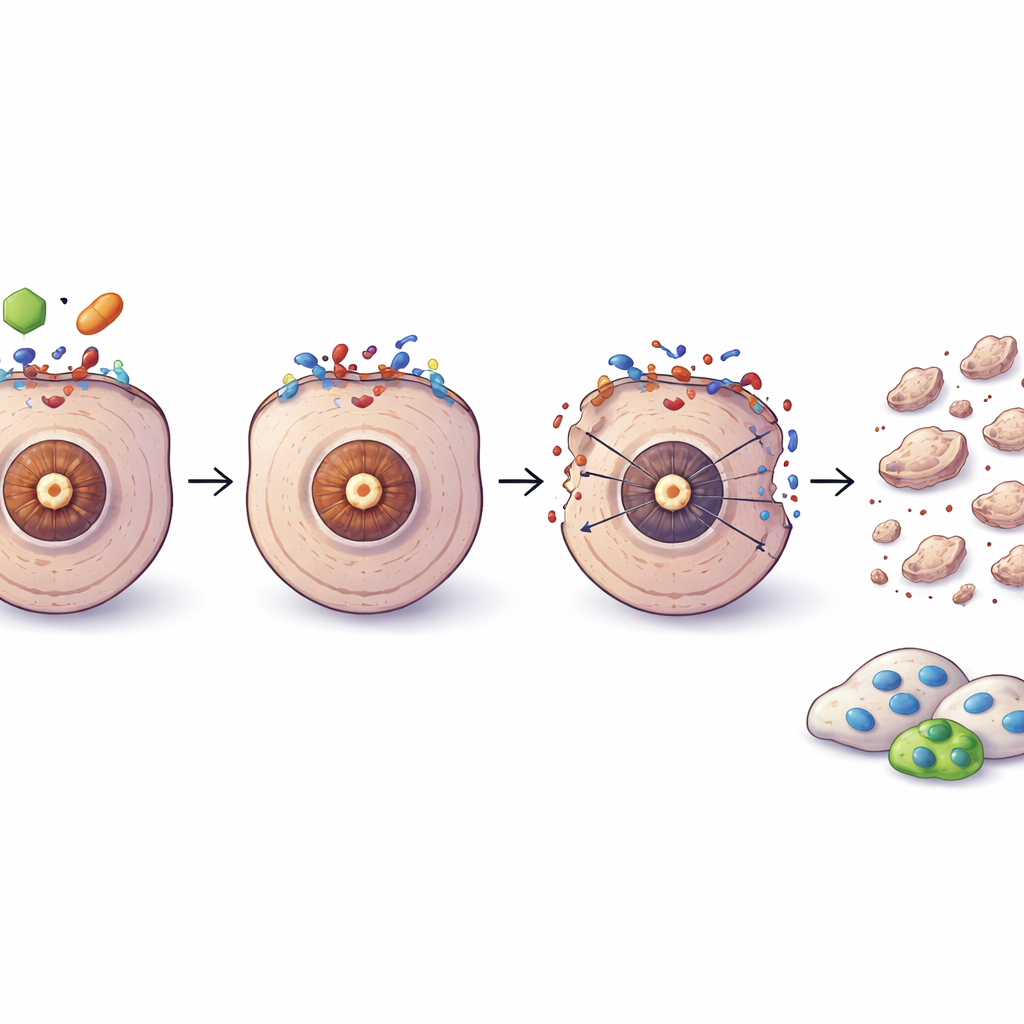
Richten op gevorderde en medicijnresistente prostaatkanker
Analyse van grote genetische datasets toonde aan dat naarmate prostaatkanker vordert naar agressievere, castratieresistente vormen, het evenwicht tussen c‑FLIP en TRAIL verandert: c‑FLIP-niveaus hebben de neiging te stijgen terwijl TRAIL-niveaus dalen, vooral in de lastigst te behandelen subtypes die standaard hormoontargets missen. Dit patroon past bij het idee dat deze tumoren steeds afhankelijker worden van de c‑FLIP-veiligheidsschakelaar voor overleving. In proefdierexperimenten krompen castratieresistente tumoren veel sterker wanneer OH14 werd gecombineerd met het chemotherapiemiddel docetaxel dan bij docetaxel alleen, zonder duidelijke toegenomen toxiciteit. In celmodellen die al resistent waren geworden tegen docetaxel verzwakte het blokkeren van c‑FLIP de cellen nog steeds en herstelde het in beperkte mate de gevoeligheid voor TRAIL, hoewel resistentie niet volledig werd opgeheven.
Wat dit kan betekenen voor toekomstige behandelingen
Samengevat suggereert de studie dat middelen die c‑FLIP uitschakelen bestaande behandelingen zoals TRAIL-gebaseerde agentia en docetaxel veel effectiever kunnen maken, vooral tegen agressieve, laat‑stadium prostaatkankers waarvoor momenteel weinig goede opties bestaan. Door zowel de bulk tumorcellen als de kleinere populatie stamachtige cellen aan te pakken die terugval aandrijven, is het doel van deze strategie niet alleen tumoren te verkleinen, maar ook te voorkomen dat ze terugkomen. Hoewel OH14 zelf verdere verfijning en veiligheidstesten nodig heeft voordat het de kliniek bereikt, levert dit werk een duidelijke blauwdruk voor combinatietherapieën die mannen met gevorderde prostaatkanker mogelijk langduriger onder controle zouden kunnen houden.
Bronvermelding: Turnham, D.J., French, R., Frame, F.M. et al. Inhibition of c-FLIP alongside TRAIL treatment suppresses prostate cancer stem cell activity. Br J Cancer 134, 1300–1310 (2026). https://doi.org/10.1038/s41416-026-03359-4
Trefwoorden: prostaatkanker, remming van c-FLIP, TRAIL-therapie, kankerstamcellen, docetaxelresistentie