Clear Sky Science · de
Hemmung von c-FLIP zusammen mit TRAIL-Behandlung unterdrückt die Aktivität von Prostatakrebs-Stammzellen
Warum diese Forschung für Männer und ihre Familien wichtig ist
Prostatakrebs gehört zu den häufigsten Krebserkrankungen bei Männern. Viele Fälle lassen sich behandeln, doch aggressive Formen treten nach Standardtherapien oft wieder auf und können tödlich verlaufen. Ein wesentlicher Grund dafür ist eine kleine Reserve widerstandsfähiger Zellen, oft als Krebsstammzellen bezeichnet, die Behandlungen überleben und den Tumor wiederaufbauen können. Diese Studie untersucht einen neuen Ansatz, bei dem sowohl die Masse des Tumors als auch dieser resistente Kern angegriffen werden, indem ein zentraler Überlebensschalter in den Krebszellen ausgeschaltet und mit bereits vorhandenen zell‑tötenden Wirkstoffen kombiniert wird.
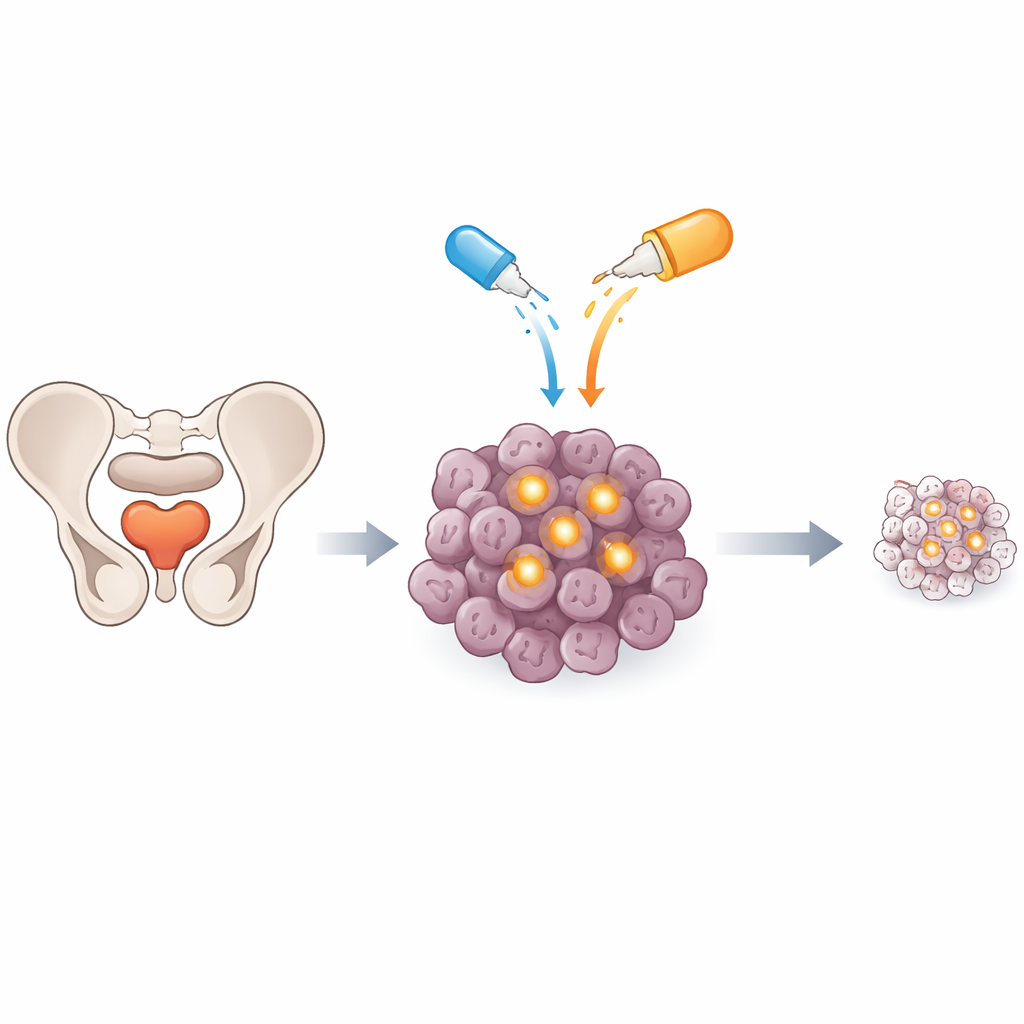
Ein versteckter Sicherheitsschalter in Tumorzellen
Krebszellen überleben häufig, indem sie die normale Maschinerie so umprogrammieren, dass beschädigte Zellen nicht wie vorgesehen Selbstmord begehen. Ein wichtiger Bestandteil dieser Maschinerie ist ein Protein namens c‑FLIP, das in einem Signalweg sitzt, der normalerweise den programmierten Zelltod aktiviert, wenn ein Gefahrensignal an der Zelloberfläche ankommt. In Prostatatumoren, insbesondere in fortgeschrittenen, therapieresistenten Formen, ist c‑FLIP häufig hochreguliert und wirkt wie ein Sicherheitsschalter, der Todesignale blockiert. Die Forschenden fragten, ob das Ausschalten dieses Schalters mit einem kleinen Molekülwirkstoff namens OH14 Prostatakrebszellen deutlich anfälliger für ein natürliches Todesignalprotein namens TRAIL oder für das Chemotherapeutikum Docetaxel machen könnte.
Prüfung der neuen Wirkstoffkombination im Labor
Zunächst arbeiteten die Forschenden mit etablierten Prostatakrebszelllinien, die in Kultur gezüchtet wurden, einschließlich Zellen, die normalerweise gegenüber TRAIL resistent sind. Allein hatten weder OH14 noch TRAIL einen starken Effekt auf den Zelltod. Wurden die Zellen jedoch kurz OH14 ausgesetzt und anschließend mit TRAIL behandelt, löste das eine ausgeprägte Welle programmierten Zelltods aus, die durch einen Caspase-Inhibitor blockiert werden konnte — ein Hinweis darauf, dass der Selbstmordweg tatsächlich aktiviert wurde. Überlebende Zellen wurden dann in sehr geringer Zahl ausgesät, um zu prüfen, wie viele Kolonien entstehen konnten; das dient als Indikator für die Aktivität von Krebsstamm‑ oder Vorläuferzellen. Die Kombination aus OH14 und TRAIL reduzierte die Koloniebildung deutlich stärker als jede Einzelbehandlung, was darauf hindeutet, dass der Ansatz nicht nur gewöhnliche Tumorzellen, sondern auch die gefährlicheren, stammzellähnlichen Zellen trifft.
Patiententumoren und Tiermodelle im Blick
Die Forschenden gingen über Standardzelllinien hinaus und verwendeten Zellen, die direkt aus Prostatagewebe von Männern gewonnen wurden, einschließlich gutartiger Wucherungen und Tumoren unterschiedlicher Schweregrade. Auch hier verringerte OH14 das Überleben von Krebszellen effektiver als TRAIL allein, und die Kombination beider Wirkstoffe senkte Überlebensrate und Koloniewachstum weiter, besonders in höhergradigen Tumoren. Um zu prüfen, ob das in einem lebenden Organismus relevant ist, nutzten sie Mäuse mit patientenabgeleiteten Prostatatumoren, die fortgeschrittene, hormonresistente Erkrankungen nachbilden. Tumorzellen wurden entnommen, außerhalb des Körpers mit OH14, TRAIL oder beiden behandelt und dann in unterschiedlichen Zellzahlen in neue Mäuse transplantiert. Nur die Kombinationstherapie verringerte deutlich die Fähigkeit dieser Zellen, neue Tumoren zu bilden, was auf einen erheblichen Verlust tumorinitiierender, stammzellähnlicher Zellen hindeutet.
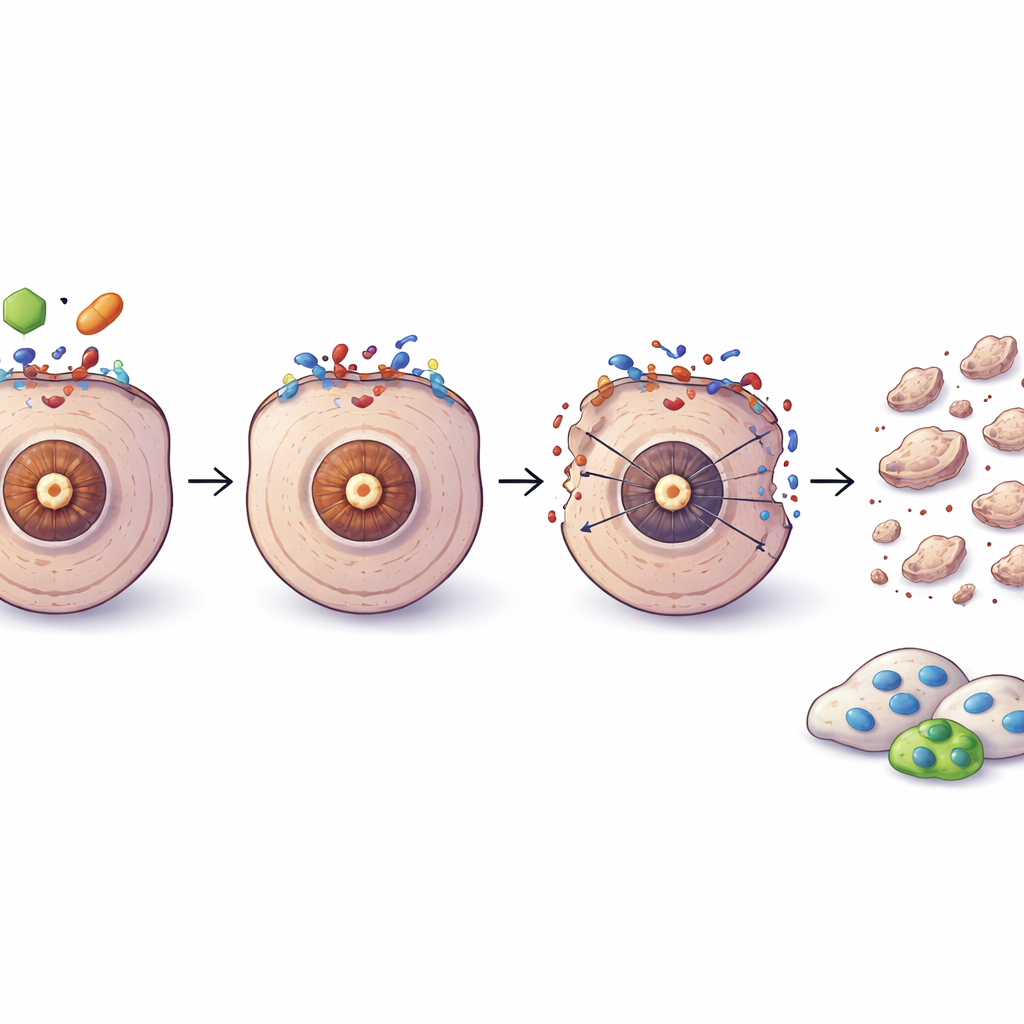
Gezielter Angriff auf fortgeschrittenen und medikamentenresistenten Prostatakrebs
Analysen großer genetischer Datensätze zeigten, dass mit dem Fortschreiten des Prostatakrebses zu aggressiveren, kastrationsresistenten Formen das Gleichgewicht zwischen c‑FLIP und TRAIL kippt: c‑FLIP-Spiegel steigen tendenziell an, während TRAIL‑Spiegel abnehmen, besonders in den schwer behandelbaren Subtypen ohne gängige Hormonziele. Dieses Muster passt zur Idee, dass diese Tumoren zunehmend von dem c‑FLIP‑Sicherheitsschalter abhängig werden. In Tierexperimenten schrumpften kastrationsresistente Tumoren durch die Kombination von OH14 mit dem Chemotherapeutikum Docetaxel deutlich stärker als durch Docetaxel allein, ohne offensichtliche zusätzliche Toxizität. In Zellmodellen, die bereits Docetaxel-resistent geworden waren, schwächte die Blockade von c‑FLIP die Zellen weiterhin und stellte die Empfindlichkeit gegenüber TRAIL teilweise wieder her, obwohl die Resistenz nicht vollständig aufgehoben wurde.
Was das für künftige Behandlungen bedeuten könnte
Insgesamt legt die Studie nahe, dass Wirkstoffe, die c‑FLIP deaktivieren, vorhandene Behandlungen wie TRAIL-basierte Agenzien und Docetaxel deutlich wirksamer machen könnten, insbesondere gegen aggressive, späte Stadien des Prostatakrebses, für die es derzeit wenige gute Optionen gibt. Indem sowohl die massiven Tumorzellen als auch der kleinere Pool stammzellähnlicher Zellen, die Rückfälle antreiben, angegriffen werden, zielt diese Strategie nicht nur auf die Verkleinerung von Tumoren, sondern darauf, ihr Wiederauftreten zu verhindern. OH14 selbst wird zwar noch weiter verfeinert und sicherheitstechnisch geprüft werden müssen, bevor es in die Klinik kommt, doch die Arbeit liefert eine klare Blaupause für Kombinationstherapien, die Männern mit fortgeschrittenem Prostatakrebs eines Tages eine länger anhaltende Kontrolle ihrer Erkrankung bieten könnten.
Zitation: Turnham, D.J., French, R., Frame, F.M. et al. Inhibition of c-FLIP alongside TRAIL treatment suppresses prostate cancer stem cell activity. Br J Cancer 134, 1300–1310 (2026). https://doi.org/10.1038/s41416-026-03359-4
Schlüsselwörter: Prostatakrebs, c-FLIP-Hemmung, TRAIL-Therapie, Krebsstammzellen, Docetaxel-Resistenz