Clear Sky Science · pl
Utrata sygnalizacji receptora PTH1R w komórkach periodontium powoduje dysfunkcję cementu i zesztywnienie trzonowców u myszy
Dlaczego podpora zęba ma znaczenie wykraczające poza próchnicę
Większość z nas myśli o zdrowiu jamy ustnej w kategoriach ubytków i chorób dziąseł, ale istnieje jeszcze jedna ukryta struktura, która cicho trzyma każdy ząb na miejscu: cienka, żywa poduszka oddzielająca korzeń zęba od otaczającej kości szczęki. Gdy ten system podparcia zawodzi, zęby mogą dosłownie zrosnąć się z kością, stając się nieruchome i bardzo trudne do leczenia. Badanie na myszach ujawnia, jak pojedynczy receptor hormonalny w komórkach periodontium działa jako zabezpieczenie przed tego typu szkodliwym zespoleniem korzenia z kością.
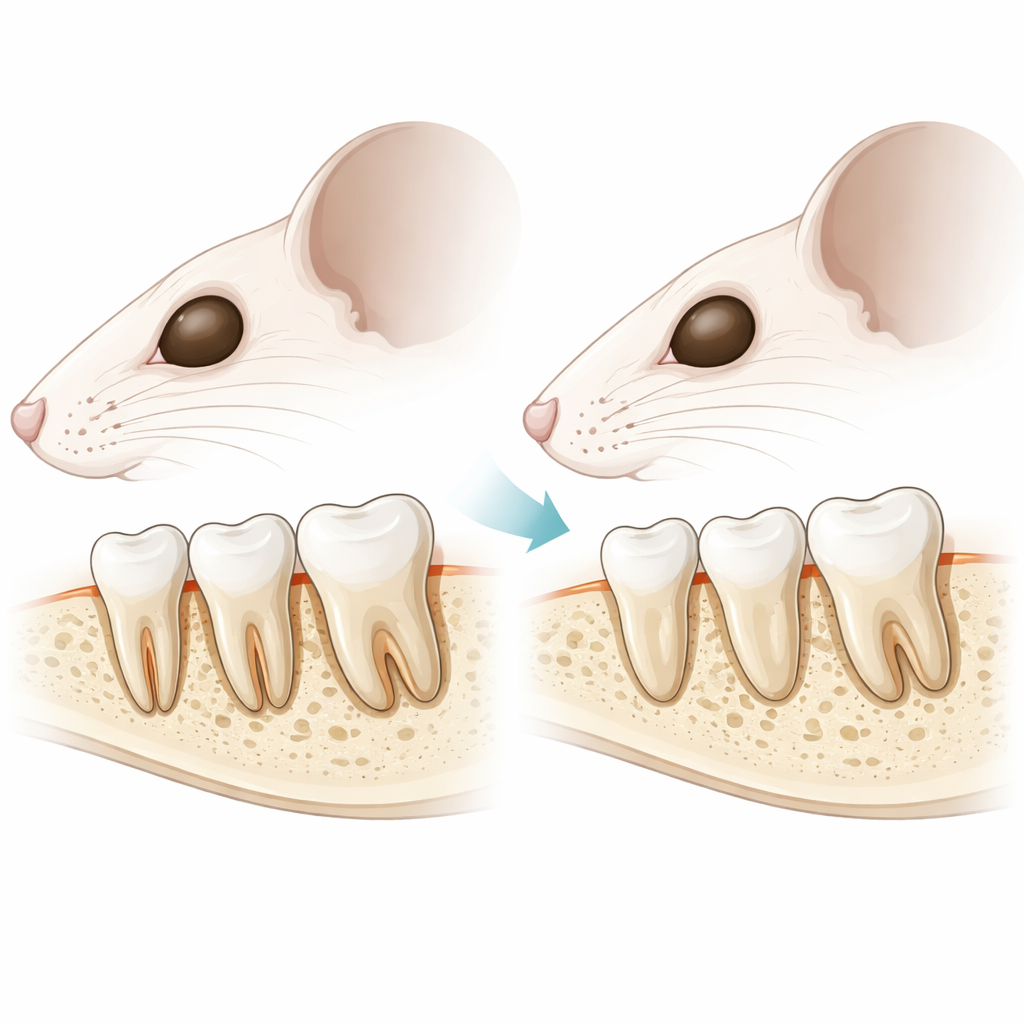
Ciche tkanki utrzymujące zęby na miejscu
Każdy ząb jest osadzony w zębodole przez niewielki ekosystem tkanek zwany periodontium. Obejmuje ono kość otaczającą korzeń, cienką mineralną powłokę na korzeniu zwaną cementem oraz miękką, włóknistą warstwę pośrednią — więzadło ozębnej. To więzadło działa jak mikroskopijny most wiszący, pozwalając zębom wytrzymywać siły żucia przy zachowaniu niewielkiej elastyczności. Badacze skoncentrowali się na receptorze hormonalnym PTH1R, znanym z roli w zdrowiu kości i wyrzynaniu zębów w dzieciństwie, i zapytali, jaką pełni funkcję później w życiu w dojrzałych komórkach obecnych w cemencie i kości wokół korzeni.
Celowana zmiana genetyczna o zaskakujących skutkach dla szczęki
Aby to zbadać, zespół stworzył myszy, u których PTH1R usunięto tylko z określonych mineralizowanych komórek w kości szczęki i cemencie, używając narzędzia genetycznego DMP1‑Cre. Zaawansowane trójwymiarowe skany mikro‑CT wykazały, że te zwierzęta rozwinęły krótsze szczęki górne i cieńszą kość pod trzonowcami w porównaniu z normalnymi rodzeństwem. Ich korzenie trzonowców były także krótsze, a kość, która normalnie unosi się wokół nich, miała zmniejszoną wysokość. Ważne jednak, że zęby wyrżnęły się do jamy ustnej, a zęby sieczne wyglądały normalnie, co pozwoliło naukowcom badać, jak późna utrata PTH1R wpływa na już uformowany system periodontium, a nie na wczesny rozwój zęba.
Gdy poduszka zęba znika
Szczegółowa analiza mikroskopowa ujawniła dramatyczny rozpad przestrzeni więzadła w rejonie trzonowców. U zdrowych myszy korzeń zęba i kość szczęki były wyraźnie rozdzielone uporządkowanym pasmem włókien bogatych w białka strukturalne, takie jak periostyna, dekoryna i kolagen. U mutantów ta szczelina była często zastępowana przez zwartą zmineralizowaną tkankę bezpośrednio łączącą korzeń z kością — stan znany jako ankyloza. Macierz włóknista była pofragmentowana lub nieobecna, jej włókna kolagenowe rozchwiane, a kluczowe białka więzadła wyraźnie zredukowane. W wielu miejscach pozostałe więzadło wydawało się odsunięte od powierzchni korzenia, sugerując, że coś wyrastające z samego korzenia wypełniało przestrzeń, gdzie powinno być więzadło.
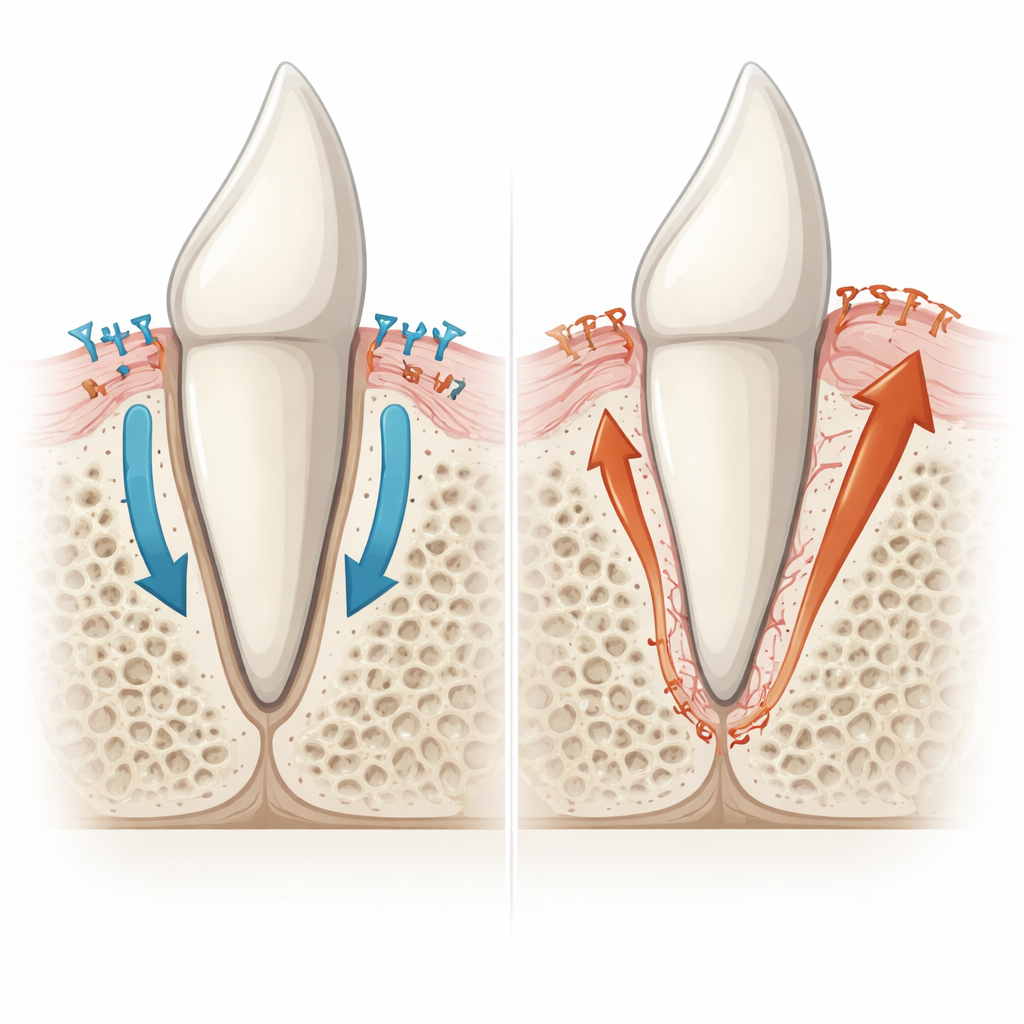
Powłoka korzenia wymykająca się spod kontroli
Bliższa inspekcja wykazała, że sprawcą nie była przerostowa kość szczęki, lecz nieprawidłowe rozrosty własnej mineralnej powłoki korzenia — cementu. Zazwyczaj cienka, bezkomórkowa warstwa cementu pokrywa dużą część korzenia, zapewniając gładką powierzchnię do przyczepu włókien więzadła. Pod wierzchołkiem korzenia tworzy się grubszy, komórkowy typ cementu zawierający zatopione żywe komórki. U myszy mutantów obszary, które powinny mieć jedynie cienką bezkomórkową warstwę, zamiast tego gromadziły grubszy cement o cechach komórkowych, który łączył się bezpośrednio z kością. Maleńkie przestrzenie mieszczące komórki w tej tkance wyglądały bardziej jak cement niż kość i nie przyciągały komórek resorbujących kość, które zwykle przebudowują tkankę kostną szczęki. Markery molekularne potwierdziły, że te zrośnięte obszary nosiły sygnaturę cementu, a nie kości, wskazując na nadaktywnych komórek tworzących cement jako główny czynnik ankylozy.
Sygnały przechylające równowagę w stronę zrostu
Aby zrozumieć, co popychało cement do nadmiernej aktywności, badacze przeanalizowali szlaki sygnałowe w komórkach periodontium. Bez PTH1R zaobserwowali więcej komórek z aktywowanym Smad3 — białkiem uczestniczącym w sygnalizacji transformującego czynnika wzrostu (TGF‑β) — oraz wyższe poziomy Osterix, kluczowego regulatora komórek tworzących kość i cement. Markery produkcji minerału, w tym fosfataza alkaliczna i DMP1, były zwiększone w pozostałym więzadle, wskazując, że komórki tam zachowywały się bardziej jak twórcy cementu niż jako wspierające komórki więzadła. Jednocześnie zespół zaobserwował wzrost ilości Dkk1, naturalnego hamulca szlaku Wnt, który zwykle pomaga powstrzymywać nadmierną mineralizację, oraz spadek S100A4 i innych cząsteczek ograniczających formowanie tkanek twardych. W połączeniu te zmiany stworzyły silny impuls ku nadmiernemu tworzeniu cementu i oddaleniu od miękkiej, elastycznej przestrzeni więzadła.
Co to oznacza dla przyszłej opieki stomatologicznej
Mówiąc prościej, praca ta pokazuje, że receptor PTH1R w dojrzałych komórkach periodontium działa jak zawór bezpieczeństwa, zapobiegając niekontrolowanemu wzrostowi mineralnej powłoki korzenia i zasklepianiu zęba z kością. Gdy ten zawór zostaje usunięty u myszy, szlaki sygnałowe sprzyjające tworzeniu tkanek twardych stają się nadaktywne, a te wspierające zdrowe więzadło ulegają stłumieniu. Wynikiem jest nadmierny wzrost cementu, utrata amortyzującego połączenia zęba i ostateczne zrośnięcie zęba z szczęką. Uściślenie, jak ta równowaga jest normalnie utrzymywana — i jak może zawieść — otwiera drogę do przyszłych strategii, które mogłyby zachować lub przywrócić przestrzeń więzadła, oferując nowe sposoby zapobiegania lub leczenia ankylozy i powiązanych problemów czaszkowo‑twarzowych u ludzi.
Cytowanie: Turkkahraman, H., Walton, C.J., Zhu, T. et al. Loss of PTH 1 receptor signaling in periodontal cells drives cementum dysfunction and molar ankylosis in mice. Bone Res 14, 46 (2026). https://doi.org/10.1038/s41413-026-00533-5
Słowa kluczowe: ankyloza zęba, cement, więzadło ozębnej, sygnalizacja PTH1R, kość czaszkowo‑twarzowa