Clear Sky Science · ar
فقدان إشارة مستقبل PTH1 في خلايا اللثة يسبب خللاً في الأسمنت والتصاق الضرس بالعظم في الفئران
لماذا دعم السن مهم بخلاف تسوس الأسنان
عادة نفكر في صحة الأسنان من منظور التجاويف وأمراض اللثة، لكن هناك بنية خفية أخرى تحافظ بهدوء على كل سن في مكانه: وسادة رقيقة حية تفصل جذور الأسنان عن عظم الفك المحيط. عندما يفشل هذا النظام الداعم، يمكن للأسنان أن تلتحم حرفياً بالعظم، فتصبح ثابتة ومن الصعب معالجتها. تكشف هذه الدراسة في الفئران كيف يعمل مستقبل هرموني واحد في خلايا اللثة كحاجز وقائي ضد هذا النوع المدمّر من الالتحام بين الجذر والعظم.
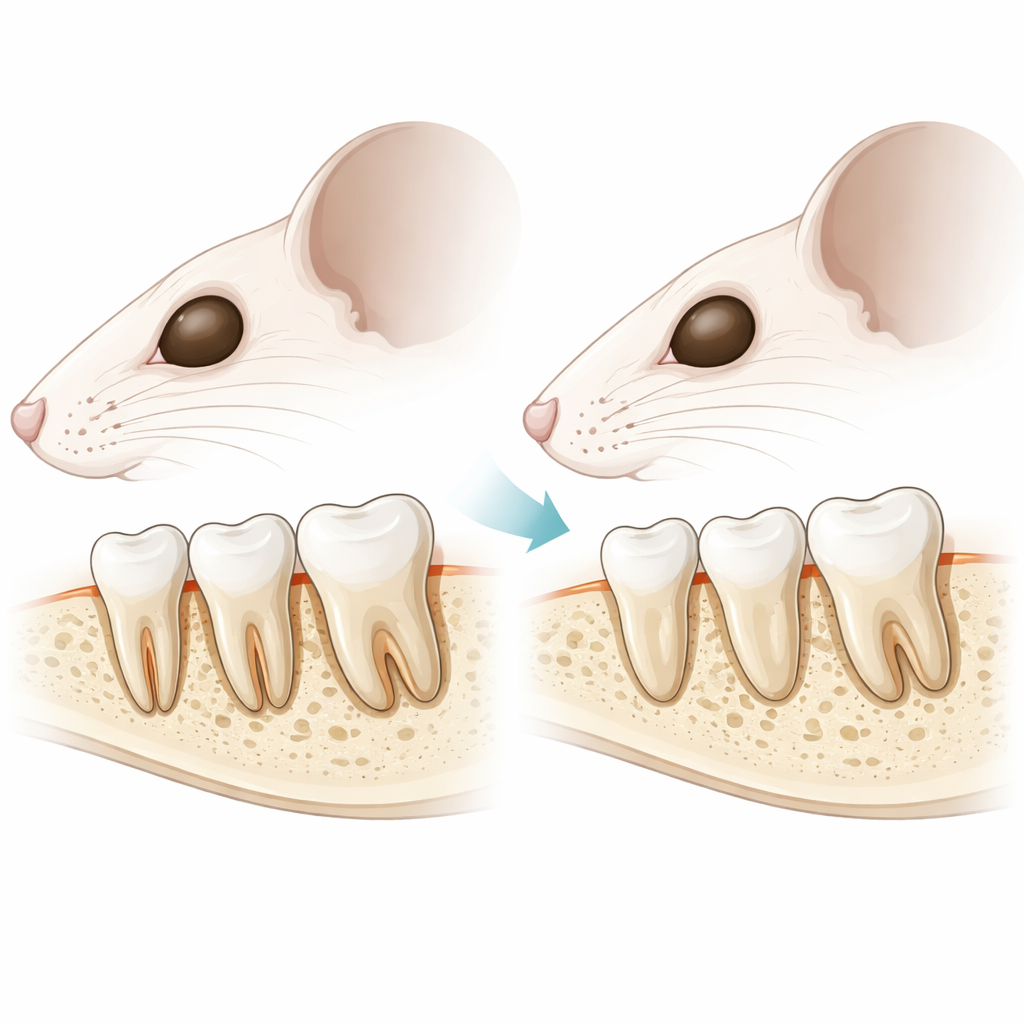
الأنسجة الهادئة التي تثبت الأسنان في مكانها
كل سن مثبت في تجويف بواسطة منظومة صغيرة من الأنسجة تُدعى النسيج المحيط بالسن (periodontium). يشمل ذلك عظم الفك المحيط بالجذر، وطِبقة رقيقة معدنية على الجذر تُسمى الأسمنت، وطبقة ليفية طرية بينهما تُعرف باسم الرباط اللثوي السني. يعمل هذا الرباط كجسر تعليق مجهري، يسمح للأسنان بتحمل قوى المضغ مع بقائها مرنة قليلاً. ركز الباحثون على مستقبل هرموني، PTH1R، المعروف بالفعل بأهميته لصحة العظام وظهور الأسنان في الطفولة، وسألوا ما دوره لاحقاً داخل الخلايا الناضجة التي تعيش في الأسمنت وعظم الفك حول الجذور.
تغيير جيني مستهدف بتأثيرات فكّية مفاجئة
لاستكشاف ذلك، صمّم الفريق فئراناً أُزيل فيها PTH1R فقط من خلايا محددة مغمورة بالمعدن في عظم الفك والأسمنت، مستخدمين أداة جينية تُدعى DMP1‑Cre. أظهرت فحوصات ثلاثية الأبعاد متقدمة بواسطة الميكرو‑CT أن هذه الحيوانات طورت فكا علوياً أقصر وعظاماً أرق تحت الأضراس مقارنة بأشقائها الطبيعيين. كما كانت جذور أضراسهم أقصر، وانخفض ارتفاع العظم الذي يرتفع عادة حولها. ومع ذلك، فقد اندلعت الأسنان إلى التجويف الفموي وبدا القواطع الأمامية طبيعية، مما مكن العلماء من دراسة كيف يؤثر فقدان PTH1R المتأخر هذا على نظام محيط السن المكتمل بدلاً من تطور السن المبكر.
عندما تختفي وسادة السن
أظهر التحليل المجهري التفصيلي تدهوراً دراماتيكياً في فراغ الرباط بمنطقة الأضراس. في الفئران السليمة، كانت جذور الأسنان وعظم الفك مفصولة بوضوح بشريط من الألياف المنظمة الغنية ببروتينات بنيوية مثل Periostin وDecorin والكولاجين. في الطفرات، حُلّ هذا الفاصل غالباً بنسيج معدني صلب يربط الجذر مباشرة بالعظم — حالة تُعرف بالالتصاق (ankylosis). كانت المصفوفة الليفية مجزأة أو مفقودة، وألياف الكولاجين فيها غير منظمة، وانخفضت البروتينات الأساسية للرباط بشكل حاد. في مناطق كثيرة بدا الرباط المتبقي مدفوعاً بعيداً عن سطح الجذر، مما يوحي بأن شيئاً ينمو من الجذر نفسه يملأ الفراغ الذي يفترض أن يشغله الرباط.
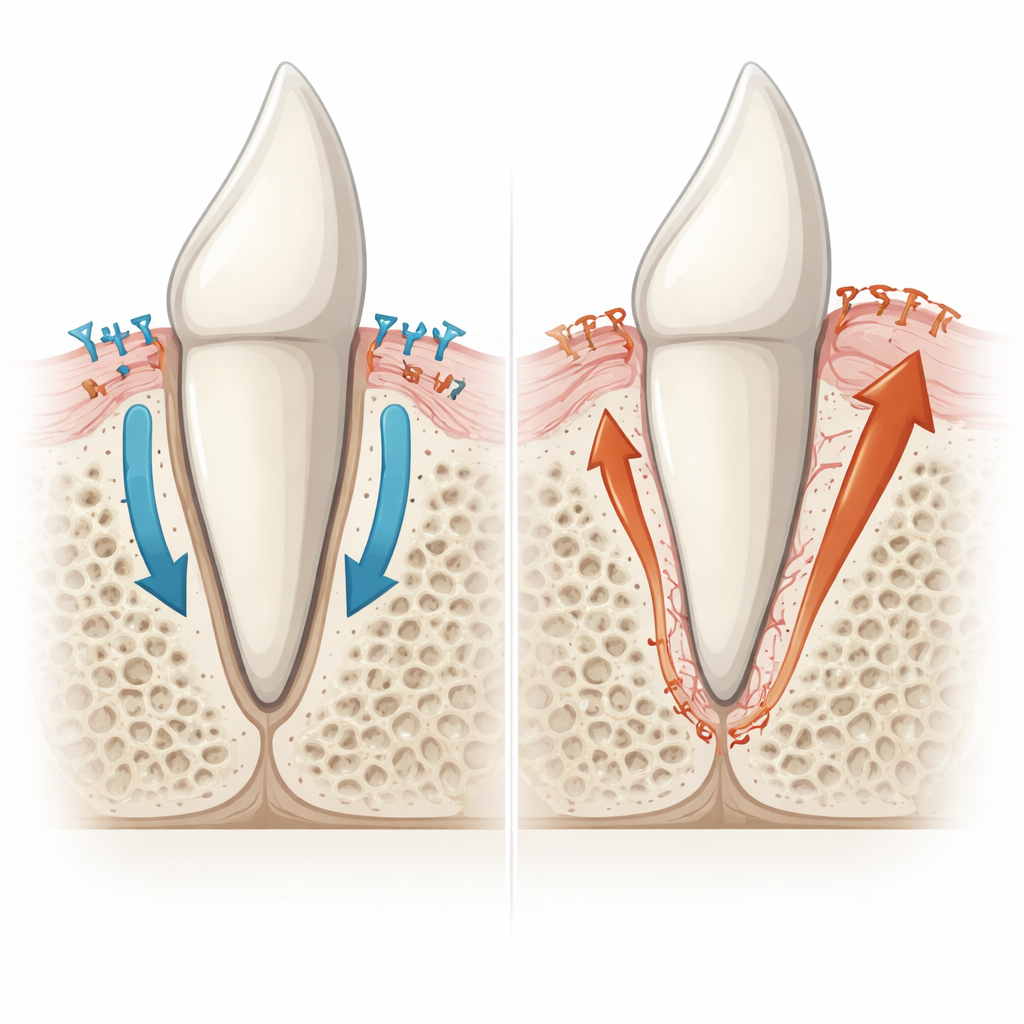
طلاء الجذر يخرج عن السيطرة
أظهر الفحص الأدق أن السبب ليس فرط نمو عظم الفك، بل توسع غير طبيعي في غطاء الجذر المعدني نفسه، أي الأسمنت. عادةً تغطي طبقة رقيقة عديمة الخلايا جزءاً كبيراً من الجذر، موفّرةً سطحاً نظيفاً لالتصاق ألياف الرباط. وتحت طرف الجذر يتكوّن نوع أسمك خلوياً من الأسمنت يحتوي على خلايا حية مدمجة. في الفئران الطافرة، تراكم في مناطق كان ينبغي أن تحتوي فقط على الطبقة الرقيقة عديمة الخلايا أسمنت أكثر سمكاً يشبه الأسمنت الخلوي وصل مباشرة إلى العظم. بدت الفراغات الدقيقة التي تسكنها الخلايا في هذا النسيج أشبه بالأسمنت منها بالعظم، وفشلت في جذب الخلايا القارضة للعظم التي عادة ما تعيد تشكيل عظم الفك. أكدت المؤشرات الجزيئية أن هذه المناطق الملتصقة تحمل بصمة الأسمنت لا العظم، مشيرة إلى أن فرط نشاط خلايا تكوين الأسمنت هو المحرّك الرئيسي للالتصاق.
الإشارات التي تميل التوازن نحو الالتحام
لفهم ما دفع الأسمنت إلى النشاط المفرط، فحص الباحثون مسارات الإشارة داخل خلايا النسيج المحيط بالسن. بدون PTH1R، وجدوا مزيداً من الخلايا التي تظهر تفعيل Smad3، وهو بروتين مشارك في إشارة عامل النمو التحويلي (TGF‑β)، ومستويات أعلى من Osterix، المسيطر الرئيس على الخلايا المكوِّنة للعظم والأسمنت. زادت مؤشرات الإنتاج المعدني، بما في ذلك الفوسفاتاز القلوي وDMP1، في كامل الرباط المتبقي، مشيرة إلى أن الخلايا هناك كانت تتصرف أكثر كمكوِّنات للأسمنت بدل أن تكون خلايا داعمة للرباط. في الوقت ذاته، لاحظ الفريق زيادة في Dkk1، وهو كابح طبيعي لمسار Wnt الذي يساعد عادة على ضبط التمعدن، وانخفاضاً في S100A4 وجزيئات أخرى تكبح تكوّن الأنسجة الصلبة. معاً خلقت هذه التغيرات دفعاً قوياً نحو تكوين الأسمنت الزائد وبعيداً عن فراغ رباط طري ومرن.
ماذا يعني هذا لرعاية الأسنان المستقبلية
بعبارات بسيطة، تُظهر هذه الدراسة أن مستقبل PTH1R في خلايا النسيج المحيط الناضجة يعمل كصمام أمان يمنع غطاء الجذر المعدني من النمو بشكل غير متحكم فيه وإغلاق السن على العظم. عندما يُزال هذا الصمام في الفئران، تصبح المسارات الإشارية التي تشجع تكوين الأنسجة الصلبة مفرطة النشاط، وتضعف المسارات التي تدعم رباطاً صحياً. النتيجة هي نمو زائد للأسمنت وفقدان اتصال ممتص للصدمات للسن، وفي نهاية المطاف التصاق السن بالعظم. من خلال توضيح كيف يُحافظ عادةً على هذا التوازن — وكيف يمكن أن يفشل — تفتح هذه النتائج الباب أمام استراتيجيات مستقبلية قد تحافظ على فراغ الرباط أو تستعيده، مقدمة طرقاً جديدة لمنع أو علاج الالتصاق ومشكلات الجمجمة والوجه ذات الصلة لدى البشر.
الاستشهاد: Turkkahraman, H., Walton, C.J., Zhu, T. et al. Loss of PTH 1 receptor signaling in periodontal cells drives cementum dysfunction and molar ankylosis in mice. Bone Res 14, 46 (2026). https://doi.org/10.1038/s41413-026-00533-5
الكلمات المفتاحية: تصاق الأسنان بالعظم, الأسمنت, رباط اللثة السني, إشارة PTH1R, عظم الجمجمة والوجه