Clear Sky Science · fr
Perte du signal du récepteur PTH1R dans les cellules parodontales entraîne un dysfonctionnement du cément et une ankylose molaire chez la souris
Pourquoi le soutien dentaire compte au-delà des caries
La plupart d’entre nous pensent à la santé dentaire en termes de caries et de maladies des gencives, mais une autre structure discrète maintient silencieusement chaque dent en place : un coussinet vivant et mince qui sépare la racine dentaire de l’os maxillaire environnant. Lorsque ce système de soutien fait défaut, les dents peuvent littéralement fusionner avec l’os, devenant immobiles et très difficiles à traiter. Cette étude menée chez la souris révèle comment un seul récepteur hormonal dans les cellules parodontales agit comme une protection contre ce type de fusion dommageable racine‑vers‑os.
Les tissus discrets qui maintiennent les dents en place
Chaque dent est ancrée dans une cavité par un petit écosystème de tissus appelé parodonte. Il inclut l’os qui entoure la racine, un mince revêtement minéral sur la racine appelé cément, et une couche molle et fibreuse intermédiaire connue sous le nom de ligament parodontal. Ce ligament agit comme un pont suspendu microscopique, permettant aux dents de supporter les forces de mastication tout en restant légèrement flexibles. Les chercheurs se sont intéressés à un récepteur hormonal, PTH1R, déjà connu pour son importance dans la santé osseuse et l’éruption dentaire pendant l’enfance, et se sont demandé quel rôle il joue plus tard dans la vie au sein des cellules matures qui habitent le cément et l’os autour des racines.
Une modification génétique ciblée avec des effets mandibulaires surprenants
Pour explorer cela, l’équipe a conçu des souris chez lesquelles PTH1R a été supprimé uniquement dans des cellules minéralisées spécifiques de l’os mandibulaire et du cément, en utilisant un outil génétique appelé DMP1‑Cre. Des scans micro‑CT 3D avancés ont montré que ces animaux développaient des maxillaires supérieurs plus courts et un os plus fin sous les molaires comparés à leurs congénères normaux. Les racines de leurs molaires étaient aussi plus courtes, et l’os qui les entoure présentait une hauteur réduite. Il est important de noter cependant que les dents ont poussé dans la bouche et que les incisives paraissaient normales, ce qui a permis aux scientifiques d’étudier comment cette perte tardive de PTH1R affecte un système parodontal déjà formé plutôt que le développement dentaire précoce.
Quand le coussinet dentaire disparaît
Une analyse microscopique détaillée a révélé une rupture spectaculaire de l’espace ligamentaire dans la région molaire. Chez les souris saines, la racine et l’os maxillaire étaient clairement séparés par une bande organisée de fibres riches en protéines structurales telles que la périostine, la décorine et le collagène. Chez les mutants, cet intervalle était souvent remplacé par un tissu minéralisé solide connectant directement la racine et l’os — une condition connue sous le nom d’ankylose. La matrice fibreuse était fragmentée ou absente, ses fibres de collagène désorganisées, et les protéines clés du ligament fortement réduites. Dans de nombreuses zones, le ligament restant semblait repoussé depuis la surface de la racine, suggérant qu’un matériau issu de la propre racine comblait l’espace où le ligament devrait se trouver.
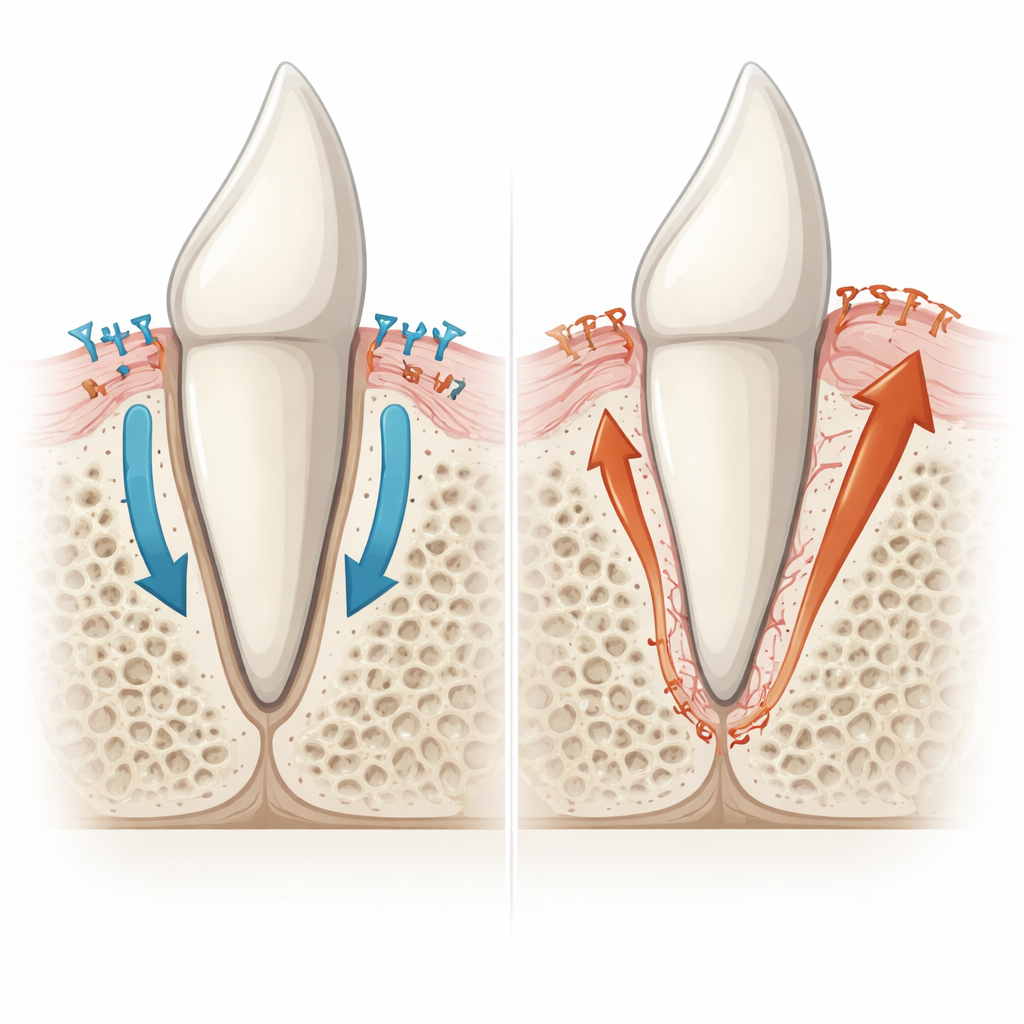
Le revêtement de la racine prend une mauvaise tournure
Un examen plus approfondi a montré que le coupable n’était pas un excès d’os, mais plutôt une expansion anormale du revêtement minéral de la racine : le cément. Normalement, une fine couche acellulaire de cément recouvre la majeure partie de la racine, offrant une surface propre pour l’attache des fibres ligamentaires. Sous l’apex de la racine, un type de cément plus épais et cellulaire se forme, contenant des cellules vivantes intégrées. Chez les souris mutantes, des régions qui devraient n’avoir que la fine couche acellulaire accumulaient à la place un cément plus épais, de type cellulaire, qui faisait pont direct avec l’os. Les minces logettes abritant des cellules dans ce tissu ressemblaient davantage à du cément qu’à de l’os, et elles n’attiraient pas les cellules ostéoclastes qui remodèlent normalement l’os maxillaire. Les marqueurs moléculaires ont confirmé que ces zones fusionnées portaient la signature du cément, pas de l’os, désignant des cellules formatrices de cément hyperactives comme principal moteur de l’ankylose.
Des signaux qui font basculer l’équilibre vers la fusion
Pour comprendre ce qui a poussé le cément à s’emballer, les chercheurs ont examiné les voies de signalisation à l’intérieur des cellules parodontales. En l’absence de PTH1R, ils ont trouvé davantage de cellules montrant une activation de Smad3, une protéine impliquée dans la signalisation du facteur de croissance transformant (TGF‑β), et des niveaux plus élevés d’Osterix, un régulateur clé des cellules formatrices d’os et de cément. Les marqueurs de production minérale, y compris la phosphatase alcaline et DMP1, étaient augmentés dans tout le ligament restant, indiquant que les cellules s’y comportaient davantage comme des fabricants de cément que comme des cellules ligamentaires de soutien. Parallèlement, l’équipe a observé des quantités accrues de Dkk1, un frein naturel de la voie Wnt qui aide normalement à contenir la minéralisation, et une baisse de S100A4 et d’autres molécules qui restreignent la formation de tissus durs. Ensemble, ces changements ont créé une forte poussée vers une production excessive de cément au détriment d’un espace ligamentaire mou et flexible.
Ce que cela implique pour les soins dentaires futurs
En termes simples, ce travail montre que le récepteur PTH1R dans les cellules parodontales matures agit comme une soupape de sécurité, empêchant le revêtement minéral de la racine de croître sans contrôle et de sceller la dent à l’os. Lorsque cette soupape est supprimée chez la souris, les voies de signalisation qui favorisent la formation de tissus durs deviennent hyperactives, tandis que celles qui soutiennent un ligament sain sont atténuées. Le résultat est une croissance excessive du cément, la perte de l’attache amortissante de la dent et la fusion éventuelle de la dent à la mâchoire. En clarifiant comment cet équilibre est normalement maintenu — et comment il peut échouer — ces résultats ouvrent la voie à des stratégies futures susceptibles de préserver ou de restaurer l’espace ligamentaire, offrant de nouvelles approches pour prévenir ou traiter l’ankylose et les problèmes craniofaciaux associés chez l’humain.
Citation: Turkkahraman, H., Walton, C.J., Zhu, T. et al. Loss of PTH 1 receptor signaling in periodontal cells drives cementum dysfunction and molar ankylosis in mice. Bone Res 14, 46 (2026). https://doi.org/10.1038/s41413-026-00533-5
Mots-clés: ankylose dentaire, cément, ligament parodontal, signalisation PTH1R, os craniofacial