Clear Sky Science · nl
Verlies van PTH1-receptorsignalering in parodontale cellen veroorzaakt cementumdisfunctie en molaarankylose bij muizen
Waarom tandondersteuning belangrijk is voorbij gaatjes
De meesten van ons denken aan mondgezondheid in termen van cariës en tandvleesontsteking, maar een andere, minder opvallende structuur houdt elke tand op zijn plaats: een dun, levend kussen dat de tandwortel scheidt van het omliggende kaakbot. Wanneer dit ondersteuningssysteem faalt, kunnen tanden letterlijk aan het bot vastgroeien, waardoor ze immobiel en moeilijk te behandelen worden. Deze studie bij muizen onthult hoe één hormoonreceptor in parodontale cellen fungeert als een beveiliging tegen dit soort schadelijke wortel‑naar‑bot fusie.
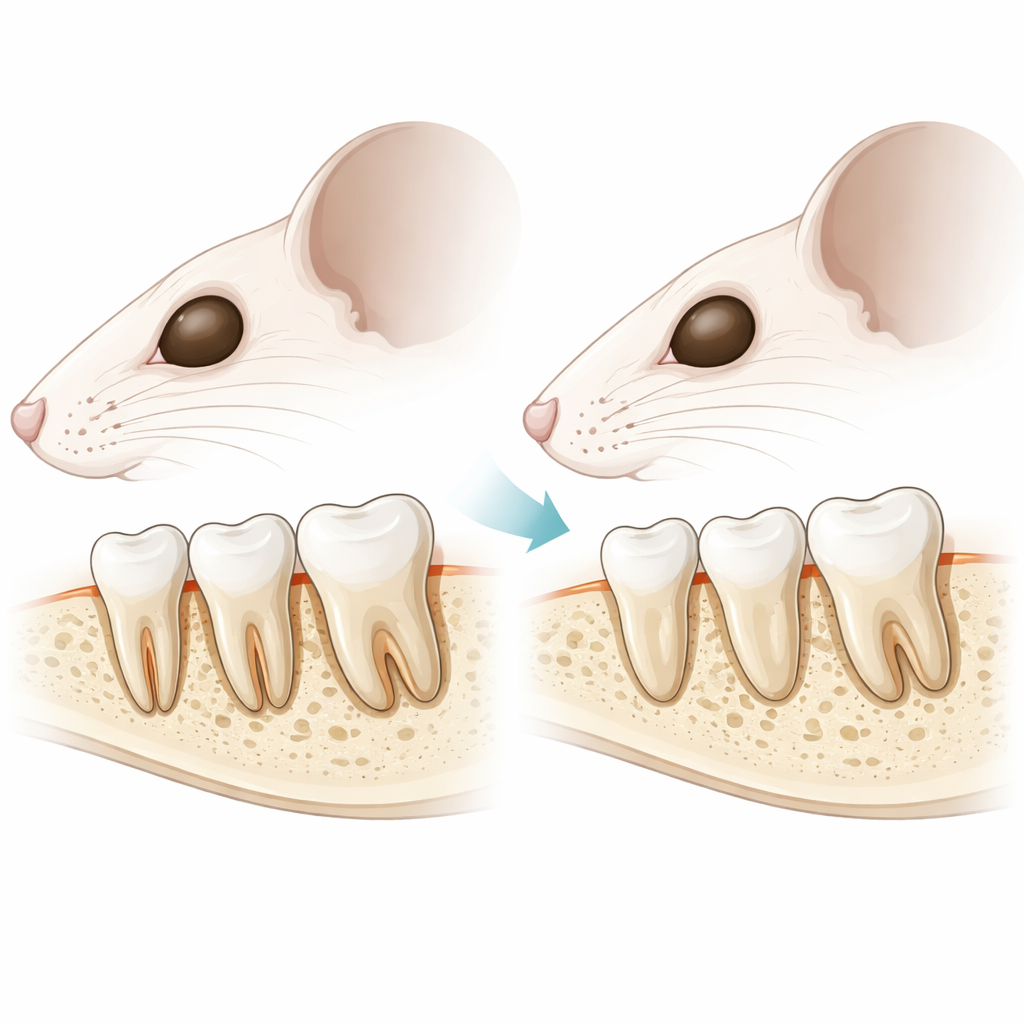
De stille weefsels die tanden op hun plaats houden
Elke tand is verankerd in een alvéole door een klein ecosysteem van weefsels dat het parodontium wordt genoemd. Het omvat het kaakbot dat de wortel omgeeft, een dunne minerale bekleding op de wortel genaamd cementum, en een zachte, vezelige laag daartussen bekend als het parodontale ligament. Dit ligament werkt als een microscopische hangbrug, waardoor tanden kauwkrachten kunnen weerstaan terwijl ze licht flexibel blijven. De onderzoekers richtten zich op een hormoonreceptor, PTH1R, die al bekend is als belangrijk voor botgezondheid en tanddoorbraak in de kinderjaren, en vroegen wat deze receptor later in het leven doet in de rijpe cellen die in cementum en kaakbot rond de wortels leven.
Een gerichte genetische wijziging met verrassende kaakeffecten
Om dit te onderzoeken, creëerde het team muizen waarbij PTH1R alleen werd verwijderd uit specifieke minerale‑ingesloten cellen in het kaakbot en cementum, met behulp van een genetisch hulpmiddel genaamd DMP1‑Cre. Geavanceerde 3D micro‑CT‑scans toonden dat deze dieren kortere bovenkaken en dunner bot onder de kiezen ontwikkelden vergeleken met normale nestgenoten. Hun kieswortels waren ook korter en het bot dat normaal om hen heen omhoog loopt was in hoogte verminderd. Belangrijk is dat de tanden wel in de mond doorbraken en de voortanden (incisieven) er normaal uitzagen, waardoor de wetenschappers konden bestuderen hoe dit late verlies van PTH1R een reeds gevormd parodontaal systeem beïnvloedt in plaats van de vroege tandontwikkeling.
Wanneer het tandkussen verdwijnt
Gedetailleerde microscopische analyse onthulde een dramatische aantasting van de ligamentruimte in het molargebied. Bij gezonde muizen waren de tandwortel en het kaakbot duidelijk gescheiden door een geordende band van vezels die rijk is aan structurele eiwitten zoals Periostin, Decorine en collageen. Bij de mutanten werd die ruimte vaak vervangen door vast, gemineraliseerd weefsel dat wortel en bot direct verbond — een aandoening bekend als ankylose. De vezelige matrix was gefragmenteerd of afwezig, de collageenvezels waren gedesorganiseerd en belangrijke ligamenteiwitten waren sterk verminderd. In veel gebieden leek het resterende ligament weggedrukt van het worteloppervlak, wat suggereert dat iets dat uit de wortel zelf groeit de ruimte vult waar het ligament zou moeten zitten.
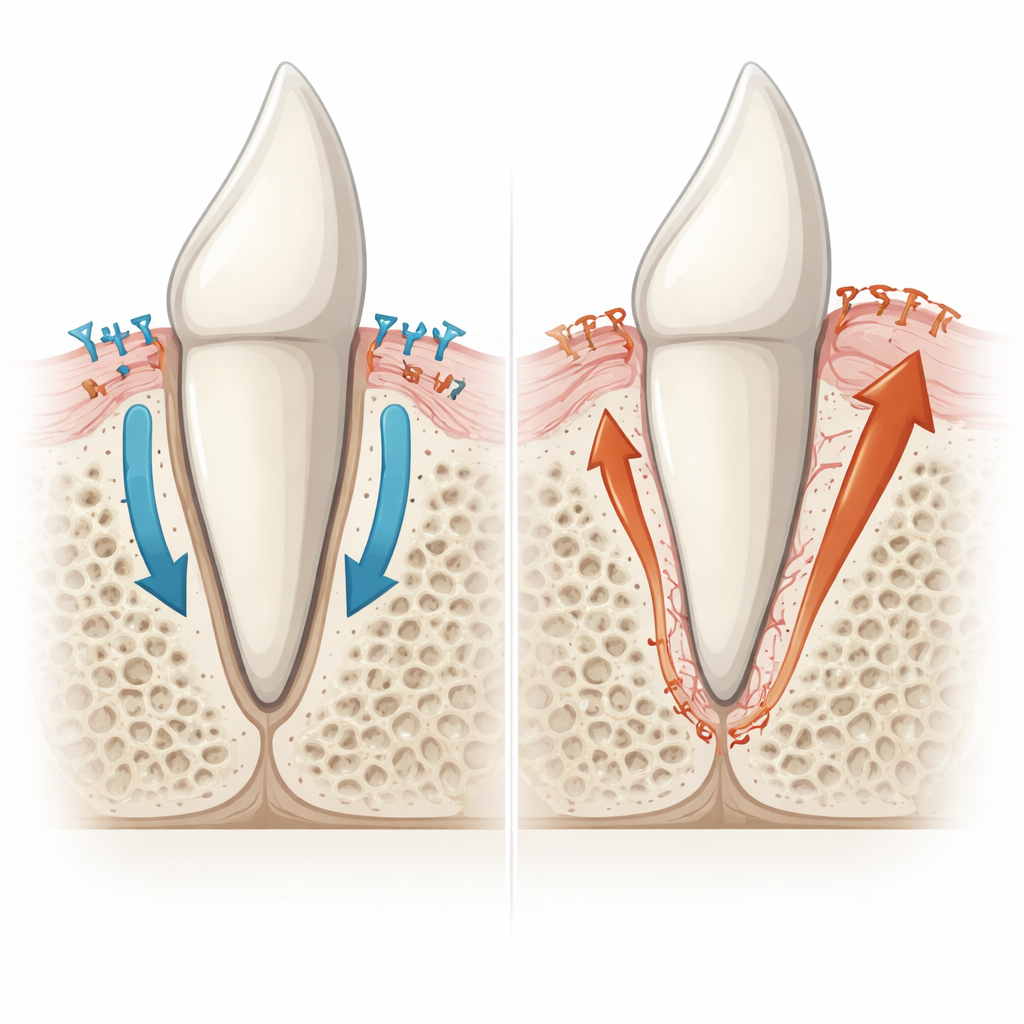
Wortelbekleding die de regels overtreedt
Nadere inspectie toonde aan dat de schuldige geen overgroei van het kaakbot was, maar een abnormale uitbreiding van de wortelbekleding zelf, het cementum. Normaal bedekt een dunne, acellulaire laag cementum een groot deel van de wortel en biedt een schone oppervlakte waar ligamentvezels aan kunnen hechten. Onder de punt van de wortel vormt zich een dikkere, cellulaire vorm van cementum, met ingesloten levende cellen. Bij de mutante muizen stapelden regio’s die alleen de dunne acellulaire laag hadden moeten hebben juist dikkere, cellulaire‑achtige cementumlagen op die direct naar het bot oversloten. De kleine ruimten waar cellen in dit weefsel huisden leken meer op cementum dan op bot, en het trok niet de botafbrekende cellen aan die normaal het kaakbot remodelleren. Moleculaire markers bevestigden dat deze gefuseerde regio’s het kenmerk van cementum droegen, niet van bot, wat wijst op overactieve cementumvormende cellen als de belangrijkste veroorzaker van ankylose.
Signalen die het evenwicht naar fusie kantelen
Om te begrijpen wat cementum in overdrive bracht, onderzochten de onderzoekers signaalroutes binnen parodontale cellen. Zonder PTH1R vonden ze meer cellen met geactiveerd Smad3, een eiwit betrokken bij TGF‑β‑signalisatie, en hogere niveaus van Osterix, een belangrijke regelaar van bot‑ en cementumvormende cellen. Markers van mineraalproductie, waaronder alkalische fosfatase en DMP1, waren verhoogd door het resterende ligament, wat aangeeft dat cellen daar zich meer gedroegen als cementumbouwers dan als ondersteunende ligamentcellen. Tegelijkertijd observeerde het team verhoogde hoeveelheden Dkk1, een natuurlijke rem op het Wnt‑pad dat normaal helpt mineralisatie onder controle te houden, en een afname van S100A4 en andere moleculen die de vorming van hard weefsel remmen. Samen creëerden deze veranderingen een sterke druk richting extra cementum en weg van een zachte, flexibele ligamentruimte.
Wat dit betekent voor toekomstige tandheelkundige zorg
Simpel gezegd laat dit werk zien dat de PTH1R‑receptor in rijpe parodontale cellen fungeert als een veiligheidsklep, die voorkomt dat de minerale bekleding van de wortel ongecontroleerd groeit en de tand aan het bot dichtsmeert. Wanneer die klep bij muizen wordt verwijderd, raken signaalroutes die de vorming van hard weefsel bevorderen overactief en worden de routes die een gezond ligament ondersteunen afgezwakt. Het resultaat is overmatige cementumgroei, verlies van de schokdempende bevestiging van de tand en uiteindelijk fusionering van de tand met de kaak. Door te verduidelijken hoe dit evenwicht normaal wordt gehandhaafd — en hoe het kan falen — openen deze bevindingen de deur naar toekomstige strategieën die de ligamentruimte kunnen behouden of herstellen, en zo nieuwe manieren bieden om ankylose en gerelateerde craniofaciale problemen bij mensen te voorkomen of te behandelen.
Bronvermelding: Turkkahraman, H., Walton, C.J., Zhu, T. et al. Loss of PTH 1 receptor signaling in periodontal cells drives cementum dysfunction and molar ankylosis in mice. Bone Res 14, 46 (2026). https://doi.org/10.1038/s41413-026-00533-5
Trefwoorden: tandankylose, cementum, parodontaal ligament, PTH1R-signalisatie, craniofaciaal bot