Clear Sky Science · de
Verlust der PTH1-Rezeptorsignalgebung in parodontalen Zellen verursacht Zementfunktionsstörung und Molarankylose bei Mäusen
Warum Zahnhalt über Karies hinaus Bedeutung hat
Die meisten von uns denken an Zahngesundheit in erster Linie im Kontext von Karies und Zahnfleischerkrankungen, doch eine unscheinbare Struktur hält jeden Zahn still: ein dünnes, lebendes Polster, das die Wurzel vom umgebenden Kieferknochen trennt. Versagt dieses Stützsystem, können Zähne buchstäblich mit dem Knochen verwachsen, unbeweglich werden und nur schwer behandelbar sein. Diese Studie an Mäusen zeigt, wie ein einzelner Hormonrezeptor in parodontalen Zellen als Schutzmechanismus gegen diese schädliche Wurzel‑zu‑Knochen‑Verschmelzung dient.
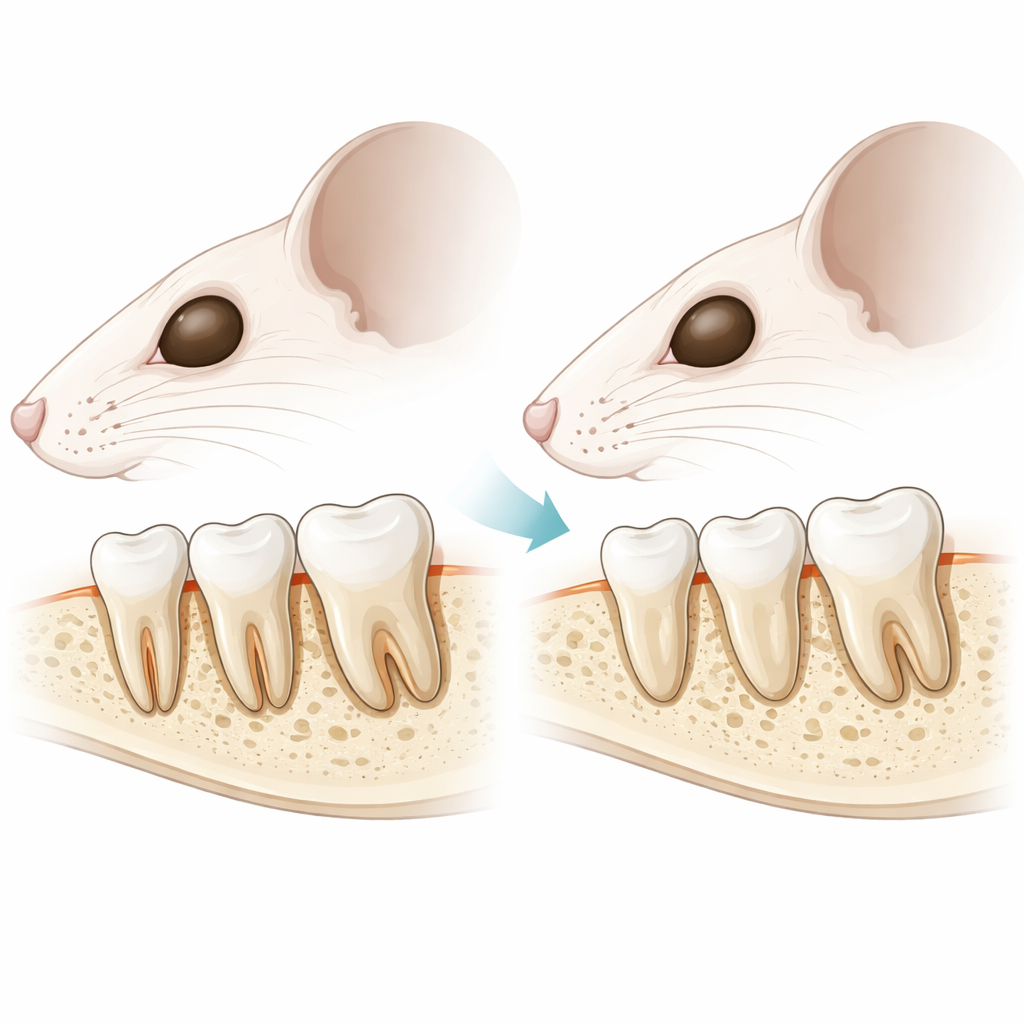
Die unauffälligen Gewebe, die Zähne halten
Jeder Zahn ist in einer Alveole durch ein kleines Gewebeökosystem, das Parodontium, verankert. Dazu gehören der den Zahn umgebende Kieferknochen, eine dünne mineralische Schicht auf der Wurzel, das Zementum, und dazwischen eine weiche, faserige Schicht, das Parodontalligament. Dieses Ligament funktioniert wie eine mikroskopische Hängebrücke: Es erlaubt den Zähnen, Kaukräften zu widerstehen und zugleich leicht nachzugeben. Die Forschenden richteten ihr Augenmerk auf einen Hormonrezeptor, PTH1R, der bereits als wichtig für Knochenstoffwechsel und Zahnaufbruch im Kindesalter bekannt ist, und fragten, welche Rolle er später im Leben in den reifen Zellen des Zementums und des umgebenden Kieferknochens spielt.
Eine gezielte genetische Veränderung mit überraschenden Kiefereffekten
Um das zu untersuchen, erzeugte das Team Mäuse, bei denen PTH1R nur in bestimmten mineralisch eingebetteten Zellen des Kiefers und Zementums entfernt wurde, mithilfe eines genetischen Werkzeugs namens DMP1‑Cre. Fortgeschrittene 3D‑Mikro‑CT‑Scans zeigten, dass diese Tiere kürzere Oberkiefer und dünneren Knochen unter den Backenzähnen entwickelten im Vergleich zu normalen Wurfgeschwistern. Auch die Wurzeln der Molaren waren kürzer und der Knochen, der sich normalerweise um sie herum aufwölbt, war in der Höhe reduziert. Wichtig war jedoch, dass die Zähne ins Maul durchbrachen und die Schneidezähne normal aussahen, sodass die Wissenschaftler untersuchen konnten, wie sich dieser späte Verlust von PTH1R auf ein bereits ausgebildetes Parodontium auswirkt, statt auf frühe Zahnentwicklung.
Wenn das Zahnpolster verschwindet
Feinere mikroskopische Analysen zeigten einen dramatischen Zusammenbruch des Ligamentraums im Molarenbereich. Bei gesunden Mäusen waren Wurzel und Kieferknochen deutlich durch ein organisiertes Faserband getrennt, das reich an Strukturproteinen wie Periostin, Decorin und Kollagen ist. Bei den Mutanten war diese Lücke oft durch festes mineralisiertes Gewebe ersetzt, das Wurzel und Knochen direkt verband — ein Zustand, der als Ankylose bekannt ist. Die faserige Matrix war fragmentiert oder fehlte, ihre Kollagenfasern desorganisiert, und wichtige Ligamentproteine waren stark reduziert. In vielen Bereichen schien das verbliebene Ligament von der Wurzeloberfläche weggedrückt, was darauf hindeutet, dass etwas aus der Wurzel selbst herauswuchs und den Raum füllte, in dem das Ligament sein sollte.
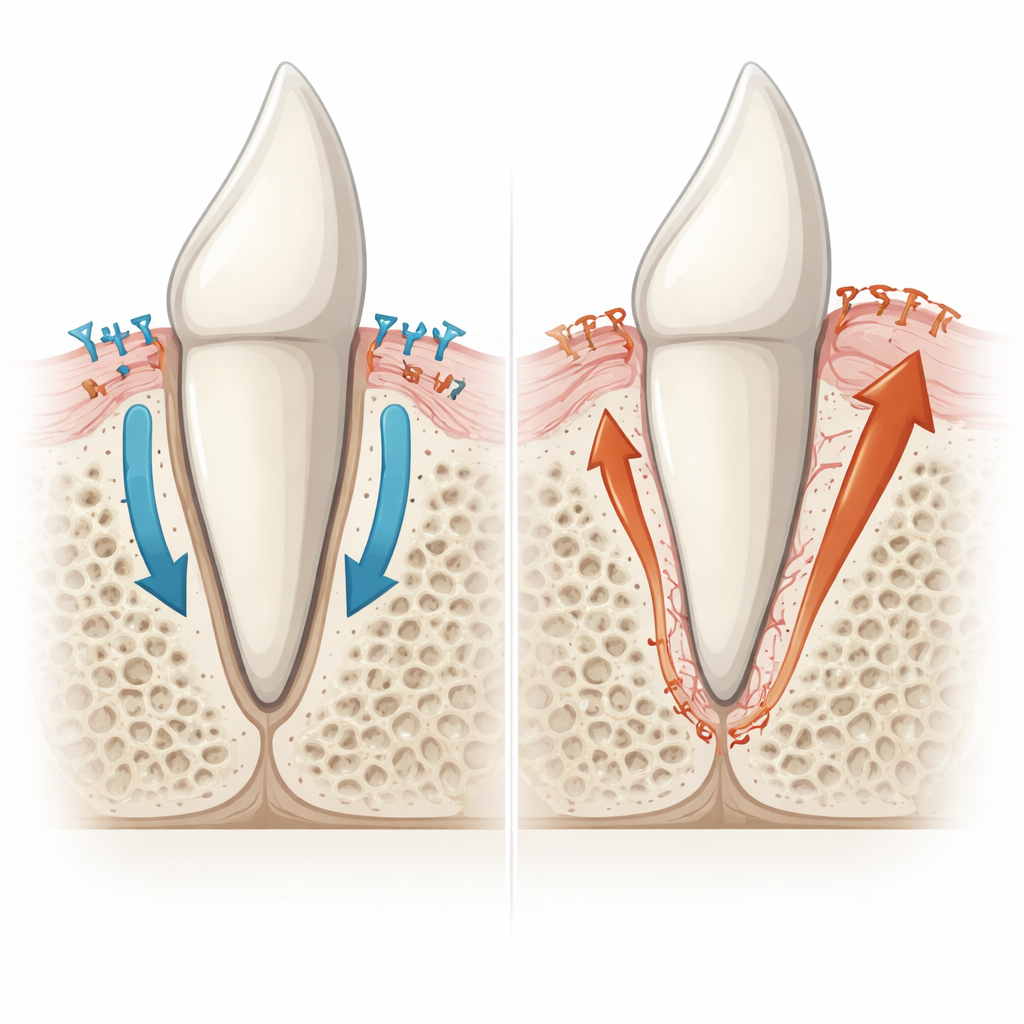
Die Wurzelbeschichtung läuft Amok
Bei genauerer Betrachtung stellte sich heraus, dass nicht übermäßig gewachsener Kieferknochen der Übeltäter war, sondern eine abnorme Ausdehnung der eigenen mineralischen Beschichtung der Wurzel, des Zementums. Normalerweise bedeckt eine dünne, zellfreie Zementumschicht weite Teile der Wurzel und bietet eine saubere Oberfläche für die Anheftung von Ligamentfasern. Unterhalb der Wurzelspitze bildet sich eine dickere, zellhaltige Form des Zementums mit eingebetteten lebenden Zellen. Bei den Mutanten sammelten sich in Regionen, die eigentlich nur die dünne zellfreie Schicht haben sollten, stattdessen dickere, zellähnliche Zementumansammlungen an, die direkt zum Knochen überbrückten. Die winzigen Räume, die Zellen in diesem Gewebe beherbergen, erinnerten eher an Zementum als an Knochen, und dieses Gewebe zog nicht die knochenabbauenden Zellen an, die normalerweise den Kieferknochen ummodellieren. Molekulare Marker bestätigten, dass diese verwachsenen Bereiche das Profil von Zementum und nicht von Knochen trugen, was überaktive zementumbildende Zellen als Hauptverursacher der Ankylose nahelegt.
Signale, die das Gleichgewicht zur Verschmelzung kippen
Um zu verstehen, was das Zementum in den Übermodus versetzte, untersuchten die Forschenden Signalwege in parodontalen Zellen. Ohne PTH1R fanden sie mehr Zellen mit aktiviertem Smad3, einem Protein der Transforming‑Growth‑Factor (TGF‑β)‑Signalgebung, und höhere Spiegel von Osterix, einem wichtigen Regulator von Knochen‑ und Zementumbildenden Zellen. Marker der Mineralbildung, darunter alkalische Phosphatase und DMP1, waren im verbliebenen Ligament erhöht, was darauf hindeutet, dass sich die Zellen dort eher wie Zementumbildner als wie stützende Ligamentzellen verhielten. Gleichzeitig beobachtete das Team erhöhte Mengen von Dkk1, einem natürlichen Bremsfaktor der Wnt‑Signalgebung, die normalerweise die Mineralisierung in Schach hält, sowie einen Rückgang von S100A4 und anderen Molekülen, die die Bildung harter Gewebe hemmen. Zusammengenommen erzeugten diese Veränderungen einen starken Antrieb hin zu vermehrtem Zementum und weg von einem weichen, flexiblen Ligamentraum.
Was das für die zukünftige Zahnmedizin bedeutet
Vereinfacht gesagt zeigen die Ergebnisse, dass der PTH1R‑Rezeptor in ausgereiften parodontalen Zellen als Sicherheitsventil wirkt, das verhindert, dass die mineralische Beschichtung der Wurzel unkontrolliert wächst und den Zahn am Knochen versiegelt. Wenn dieses Ventil bei Mäusen entfernt wird, werden Signalwege, die die Bildung harter Gewebe fördern, überaktiv, während jene, die ein gesundes Ligament unterstützen, abgeschwächt werden. Das Ergebnis ist übermäßiges Zementumwachstum, Verlust der stoßdämpfenden Verbindung des Zahns und schließlich die Verschmelzung des Zahns mit dem Kiefer. Indem diese Studie klärt, wie dieses Gleichgewicht normalerweise aufrechterhalten wird — und wie es versagen kann — eröffnet sie Perspektiven für Strategien, die den Ligamentraum erhalten oder wiederherstellen könnten und damit neue Ansätze zur Vorbeugung oder Behandlung von Ankylosen und verwandten kraniofazialen Problemen beim Menschen ermöglichen.
Zitation: Turkkahraman, H., Walton, C.J., Zhu, T. et al. Loss of PTH 1 receptor signaling in periodontal cells drives cementum dysfunction and molar ankylosis in mice. Bone Res 14, 46 (2026). https://doi.org/10.1038/s41413-026-00533-5
Schlüsselwörter: Zahnankylose, Zementum, Parodontalligament, PTH1R-Signalgebung, kraniofazialer Knochen