Clear Sky Science · pl
Identyfikacja nowej populacji progenitorów Tnn+ tworzących włóknistą chrząstkę przyczepu ścięgna
Dlaczego połączenie ścięgna z kością ma znaczenie
Za każdym razem, gdy rzucasz piłką, wchodzisz po schodach lub odpychasz się, by biec, niewidoczne połączenia w twoim ciele wykonują coś niezwykłego: łączą miękkie, elastyczne ścięgno z twardą, sztywną kością. Te niewielkie strefy przejściowe, zwane miejscami przyczepu ścięgien, są częstymi punktami urazów i często gorzej się goją po zabiegach chirurgicznych. W tym badaniu odkryto wcześniej nieznaną grupę komórek, które pomagają budować to krytyczne miejsce styku, oraz wykazano, jak codzienne siły mechaniczne, takie jak pociągnięcie mięśnia i ruch stawu, kierują ich działaniem.
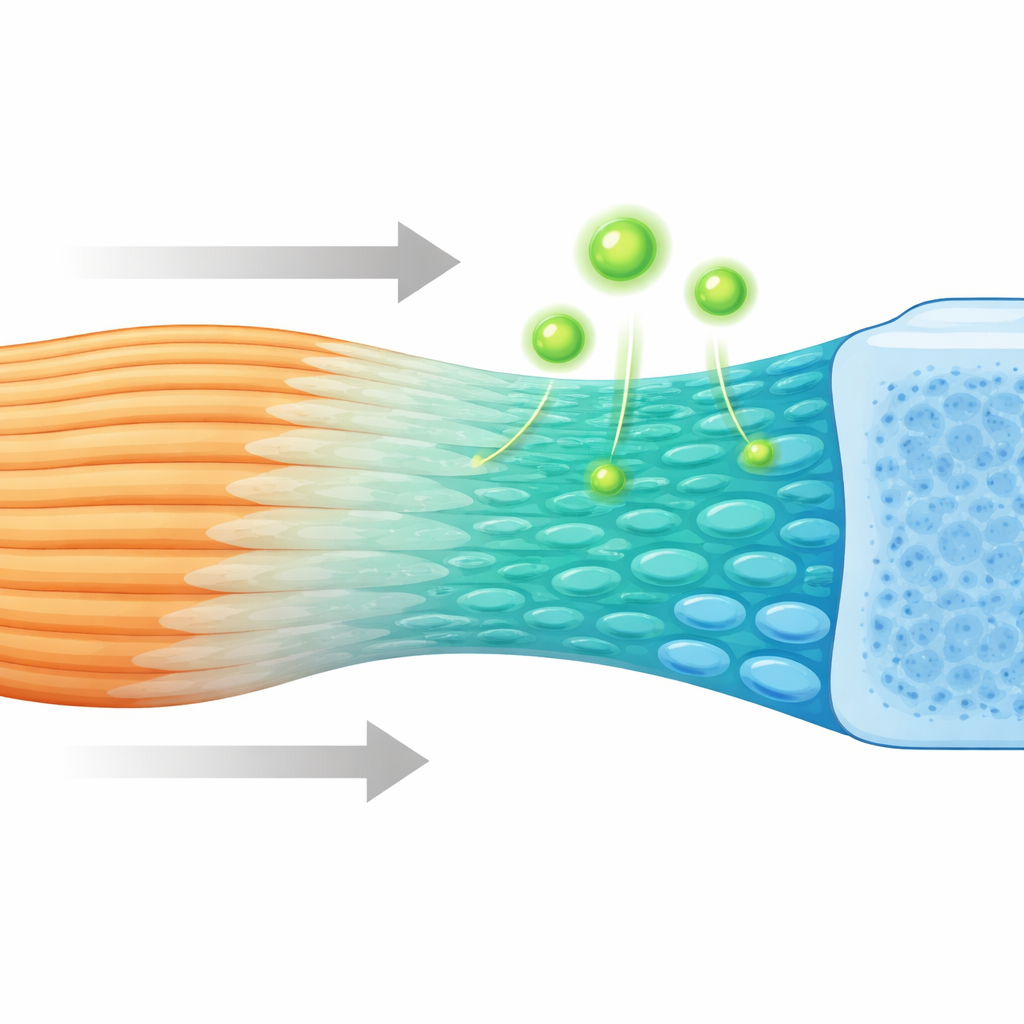
Przyjrzenie się ukrytemu połączeniu
W miejscu, gdzie ścięgno zakotwicza się w kości, tkanka nie przechodzi nagle z miękkiej w twardą. Zamiast tego występuje cienka, stopniowo zmieniająca się warstwa chrząstki włóknistej, w której skład i sztywność przekształcają się stopniowo. Ten gradient pomaga wygładzić naprężenia i zapobiega rozerwaniu. Naukowcy od dawna podejrzewali, że wyspecjalizowane komórki progenitorowe muszą budować tę strefę, lecz tożsamość i zachowanie tych komórek pozostawały niejasne. Wykorzystując wysokorozdzielcze przestrzenne mapowanie ekspresji genów oraz sekwencjonowanie pojedynczych komórek u myszy, badacze zmapowali rozmieszczenie tysięcy indywidualnych komórek i które geny włączają w trakcie formowania i dojrzewania przyczepu.
Odkrycie wyspecjalizowanej komórki-budowniczego
Śledząc aktywność genów od późnego życia embrionalnego aż do pierwszego miesiąca po narodzinach, zespół zidentyfikował odrębną populację komórek progenitorowych oznakowanych genem Tnn (kodującym cząsteczkę macierzy tenascinę-W). Komórki pozytywne dla Tnn pojawiają się wcześnie na granicy ścięgna i kości, w wąskim pasie oddzielonym od zwykłych komórek ścięgna oraz od chrząstki końca kości. Eksperymenty śledzenia linii komórkowych wykazały, że komórki oznakowane Tnn oraz ich potomstwo pozostają skoncentrowane w regionie chrząstki włóknistej i są ściśle związane ze strefami, które później ulegną mineralizacji. Z czasem te komórki przechodzą od elastycznego, przypominającego komórki macierzyste stanu do zaangażowanej roli w produkcji chrząstki i macierzy bogatej w minerały, pełniąc de facto funkcję wyspecjalizowanych budowniczych chrząstki przyczepu ścięgna.
Co się dzieje, gdy brak tych budowniczych
Aby sprawdzić, czy progenitory Tnn+ są rzeczywiście niezbędne, naukowcy stworzyli myszy, w których te komórki można było selektywnie usunąć po porodzie. Gdy komórki Tnn+ zostały zniszczone, chrząstka włóknista w przyczepie ścięgna rozwijała się nieprawidłowo. Normalnie warstwowa struktura stała się cienka i zdezorganizowana, z mniejszą liczbą i mniejszymi komórkami chrząstki włóknistej. Obrazowanie w skali mikroskopowej i trójwymiarowej wykazało zmniejszoną zawartość minerałów oraz słabszą kość podchrzęstną pod strefą przyczepu. Badania mechaniczne potwierdziły, że zmienione enthesisy były mniej sztywne i miały niższą wytrzymałość materiałową, co wskazuje, że utrata populacji progenitorów prowadzi do strukturalnie i funkcjonalnie gorszego połączenia ścięgno–kość.
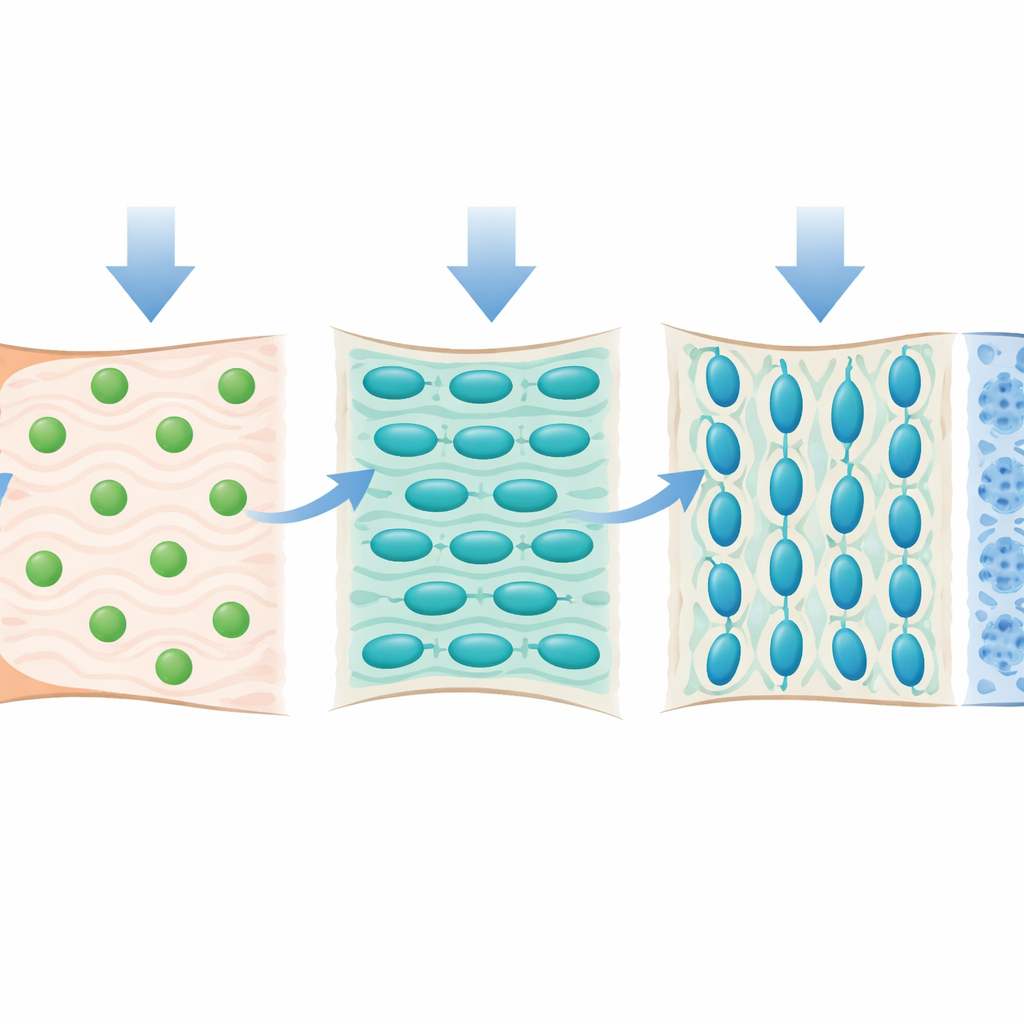
Jak obciążenie i ruch kształtują to miejsce styku
Badanie zbadało również, jak siły mechaniczne wpływają na te komórki progenitorowe. Badacze użyli toksyny botulinowej, aby częściowo sparaliżować mięsień barku, znacznie zmniejszając normalne pociągnięcie ścięgna podczas wzrostu. W tych warunkach odciążenia chrząstka włóknista pozostała niedorozwinięta: komórki były mniejsze, macierz cieńsza, a kluczowe składniki chrząstki, takie jak kolagen typu II, były wyraźnie zmniejszone. Analiza pojedynczych komórek wykazała spadek liczby progenitorów Tnn+, a te, które pozostały, miały mniejszą zdolność dojrzewania w komórki produkujące chrząstkę. Geny zaangażowane w budowę macierzy, mineralizację i kanały jonowe odpowiadające za mechanosensorykę były również stłumione, co sugeruje, że komórki Tnn+ są wyczulone na odczuwanie i reagowanie na sygnały mechaniczne.
Co to oznacza dla gojenia i naprawy
Mówiąc prosto, praca ta pokazuje, że przejściowa, wczesna fala progenitorów Tnn+ specyficznie buduje chrząstkę włóknistą kotwiczącą ścięgno do kości, oraz że normalne obciążenie mechaniczne jest niezbędne zarówno do utrzymania ich liczby, jak i do uruchomienia ich potencjału tworzenia chrząstki. Gdy te komórki zostaną usunięte lub gdy pociąg mięśnia zostanie odjęty, strefa przyczepu pozostaje zahamowana wzrostowo i mechanicznie słaba. Te spostrzeżenia pomagają wyjaśnić, dlaczego naprawy ścięgno–kość mogą zawodzić, i wskazują kierunki działań: terapie mogą wymagać zarówno rekrutacji lub ochrony wyspecjalizowanych progenitorów w enthesis, jak i zapewnienia odpowiedniej stymulacji mechanicznej, aby prawdziwie zregenerować trwałe, stopniowane połączenie ścięgno–kość.
Cytowanie: Zhang, T., Zhang, L., Yuan, Z. et al. Identification of a new population of Tnn+ progenitors to form tendon enthesis fibrocartilage. Bone Res 14, 43 (2026). https://doi.org/10.1038/s41413-026-00519-3
Słowa kluczowe: przyczep ścięgna, chrząstka włóknista, komórki progenitorowe, obciążenie mechaniczne, regeneracja tkanek