Clear Sky Science · ar
تحديد جمهور جديد من الخلايا السلفية Tnn+ لتكوين الغضروف الليفي لموصل الوتر إلى العظم
لماذا يهم رابط الوتر بالعظم
في كل مرة ترمي فيها كرة أو تصعد السلالم أو تدفع للانطلاق في ركض، تقوم نقاط تلاقي غير مرئية في جسمك بأمر استثنائي بهدوء: تربط الوتر اللين والمرن بالعظم الصلب والجامد. هذه المناطق الانتقالية الصغيرة، المسماة مواقع تثبيت الأوتار، هي نقاط إصابة شائعة وغالبًا ما تلتئم بشكل ضعيف بعد الجراحة. تكشف هذه الدراسة عن مجموعة خلايا غير معروفة سابقًا تساعد في بناء هذا الواجهة الحرجة وتظهر كيف توجه القوى الميكانيكية اليومية، مثل سحب العضلات وحركة المفاصل، عملها.
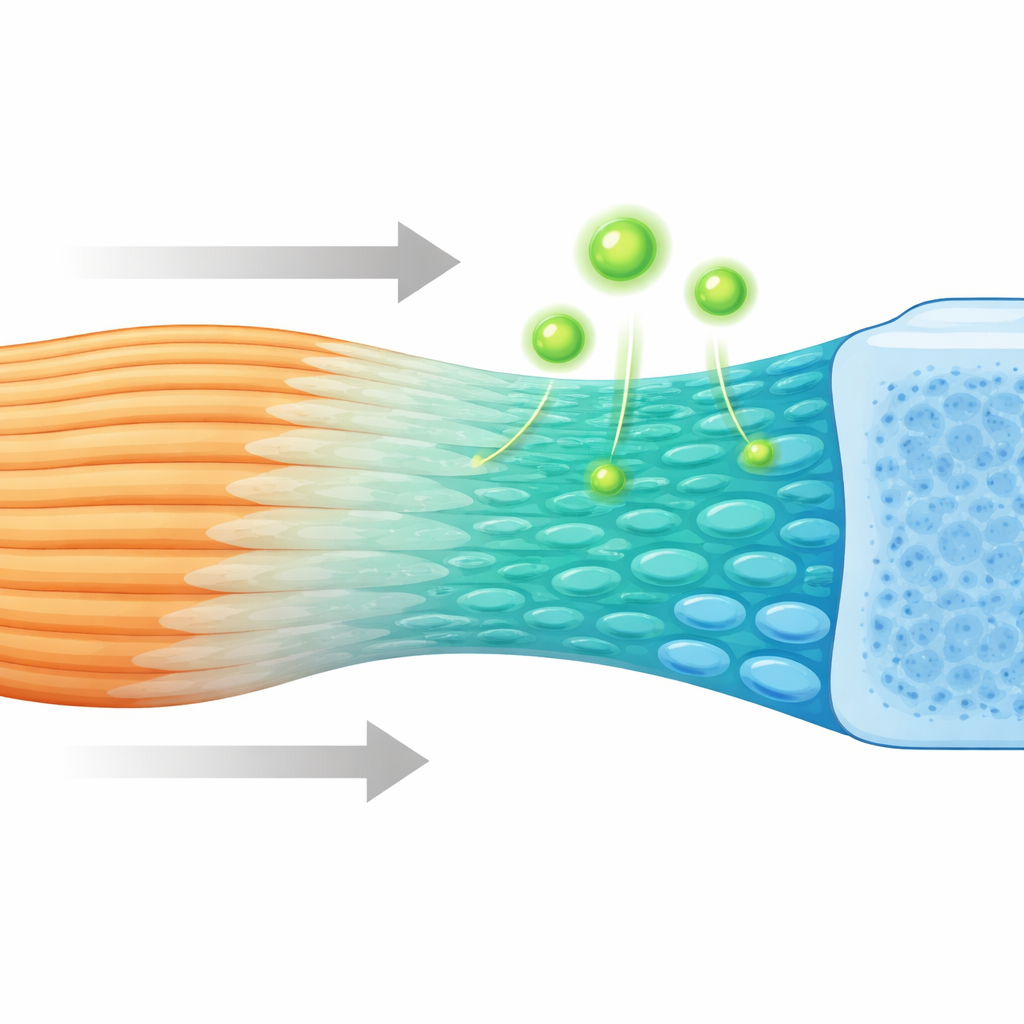
نظرة أقرب على الوصلة الخفية
حيث يثبت الوتر في العظم، لا يتغير النسيج فجأة من لين إلى صلب. بل يمر عبر طبقة رقيقة متدرجة من الغضروف الليفي تتغير تدريجيًا في التركيب والصلابة. تساعد هذه التدرجات على تمهيد الإجهاد ومنع التمزق. على الرغم من أن العلماء اشتبهوا منذ زمن طويل أن خلايا سلفية متخصصة هي التي تبني هذه المنطقة، ظلّت هوية هذه الخلايا وسلوكها غير واضحة. باستخدام رسم خرائط جيني مكاني عالي الدقة وتسلسل خلية واحدة في الفئران، رسم الباحثون كيف تُرتب آلاف الخلايا الفردية وأي الجينات تُفعَّل أثناء تكوّن التثبيت ونضجه.
اكتشاف خلية بنّاءة متخصصة
بتتبّع نشاط الجينات من الحياة الجنينية المتأخرة وحتى الشهر الأول بعد الولادة، حدَّد الفريق مجموعة مميزة من الخلايا السلفية المعلمة بجين Tnn (الذي يُشفّر جزيء المصفوفة tenascin-W). تظهر هذه الخلايا الإيجابية لـTnn مبكرًا عند واجهة الوتر–العظم، في شريط ضيق منفصل عن خلايا الوتر العادية وعن غضروف نهاية العظم المجاور. أظهرت تجارب تتبع السلالة أن الخلايا المعلمة بـTnn ونسلها تظلّ مركزة في منطقة الغضروف الليفي ومرتبطة بقوة بالمناطق التي ستتكلَّس لاحقًا. مع مرور الوقت، تتحوّل هذه الخلايا من حالة مرنة شبيهة بالخلايا الجذعية إلى دور مخصّص في إنتاج الغضروف والمصفوفة الغنية بالمعادن، لتعمل في الأساس كبنّائين متخصصين لغضروف تثبيت الوتر.
ماذا يحدث عندما تفقد هذه الخلايا البنّاءة
لاختبار ما إذا كانت الخلايا السلفية الإيجابية لـTnn ضرورية بالفعل، أنشأ الباحثون فئرانًا يمكن فيها القضاء انتقائيًا على هذه الخلايا بعد الولادة. عندما أُزيلت الخلايا الإيجابية لـTnn، تطور الغضروف الليفي في موضع التثبيت بشكل غير طبيعي. أصبحت البنية المعتادة الطبقية رقيقة وغير منظمة، مع خلايا غضروف ليفي أقل حجما وعدداً. كشف التصوير على نطاقات مجهرية وثلاثية الأبعاد عن انخفاض في المحتوى المعدني وضعف العظم تحت الغضروف في منطقة التثبيت. وأكدت الاختبارات الميكانيكية أن هذه الوصلات المعدلة كانت أقل صلابة وذات مقاومة مادية أقل، مما يشير إلى أن فقدان مجموعة الخلايا السلفية يؤدي إلى اتصال وِتري-عظمي أضعف من الناحيتين البنائية والوظيفية.
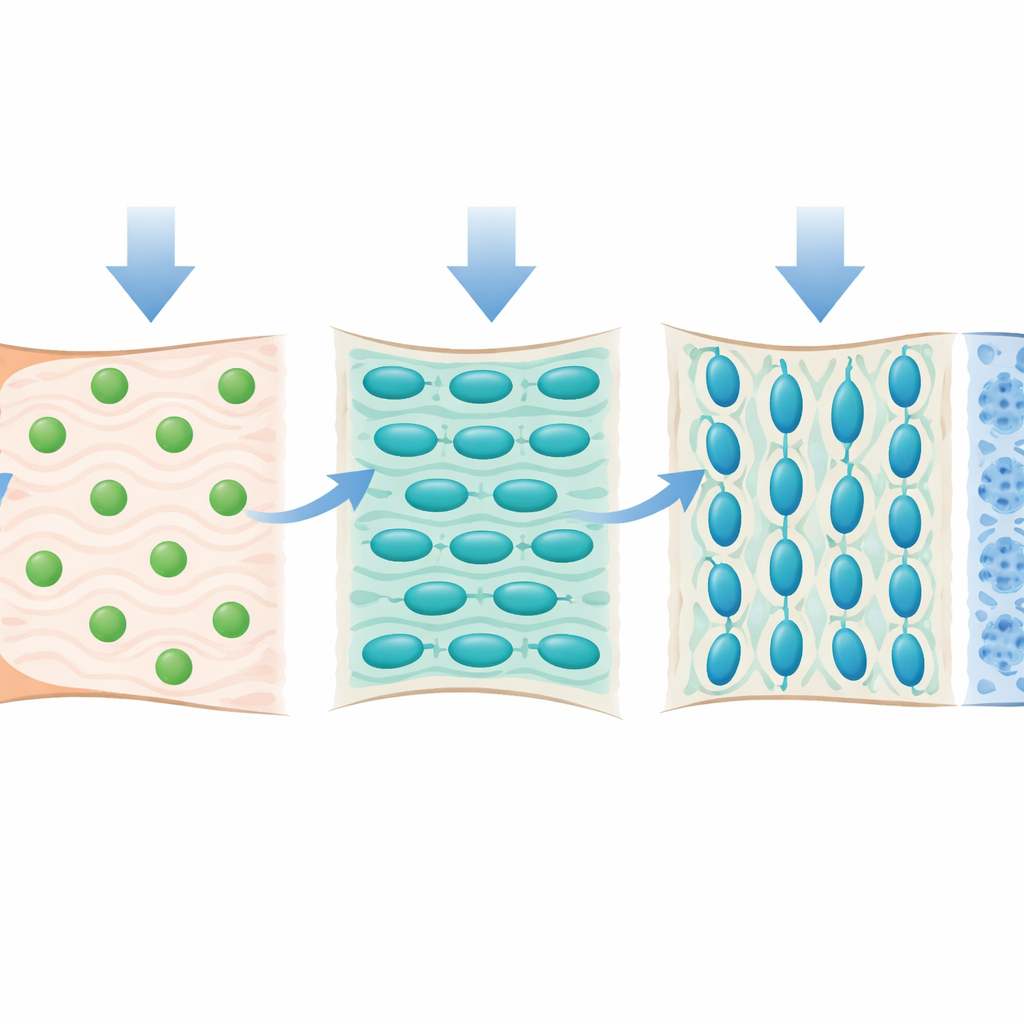
كيف يشكل الحمل والحركة الواجهة
سألت الدراسة أيضًا كيف تؤثر القوى الميكانيكية على هذه الخلايا السلفية. استخدم الباحثون سمّ البوتولينوم لشل جزئي لعضلة الكتف، مما قلّل بشدة السحب الطبيعي على الوتر أثناء النمو. تحت هذه الظروف غير المحمّلة، ظلَّ الغضروف الليفي غير متطور: كانت الخلايا أصغر، وكانت المصفوفة أرق، وكانت مكونات غضروفية رئيسية مثل الكولاجين من النوع الثاني منخفضة بصورة ملحوظة. أظهر تحليل الخلية الواحدة أن عدد الخلايا السلفية الإيجابية لـTnn انخفض، وأن الخلايا المتبقية أبدت قدرة أقل على النضج إلى خلايا منتجة للغضروف. كما كُبِحت الجينات المشاركة في بناء المصفوفة والتكلس وقنوات الاستشعار الميكانيكي الأيونية، مما يوحي بأن خلايا Tnn+ مضبوطة لتشعر بالإشارات الميكانيكية وتستجيب لها.
ما الذي يعنيه هذا للشفاء والإصلاح
بعبارات بسيطة، توضح هذه الدراسة أن موجة عابرة ومبكرة من الخلايا السلفية الإيجابية لـTnn تبني تحديدًا الغضروف الليفي الذي يثبّت الوتر في العظم، وأن التحميل الميكانيكي الطبيعي ضروري للحفاظ على أعدادها وإطلاق قدرتها على تشكيل الغضروف. عندما تُزال هذه الخلايا أو تُلغى قوة سحب العضلة، يبقى موضع التثبيت متخلفًا وضعيفًا ميكانيكيًا. تساعد هذه النتائج في تفسير سبب فشل إصلاحات الوتر إلى العظم وتشير إلى استراتيجيات مستقبلية: قد تحتاج العلاجات إلى استقطاب أو حماية الخلايا السلفية المتخصصة عند موقع التثبيت وتوفير التحفيز الميكانيكي المناسب لتوجيهها، من أجل تجديد اتصال متدرج ودائم بين الوتر والعظم.
الاستشهاد: Zhang, T., Zhang, L., Yuan, Z. et al. Identification of a new population of Tnn+ progenitors to form tendon enthesis fibrocartilage. Bone Res 14, 43 (2026). https://doi.org/10.1038/s41413-026-00519-3
الكلمات المفتاحية: موصل الوتر إلى العظم, غضروف ليفي, خلايا سلفية, التحميل الميكانيكي, تجدد الأنسجة