Clear Sky Science · es
Identificación de una nueva población de progenitores Tnn+ para formar el fibrocartílago de la entesis tendinosa
Por qué importa la unión tendón-hueso
Cada vez que lanzas una pelota, subes escaleras o das el impulso para correr, unas uniones invisibles de tu cuerpo hacen algo notable: conectan el tendón blando y elástico con el hueso duro y rígido. Estas pequeñas zonas de transición, llamadas sitios de inserción tendinosa, son puntos habituales de lesión y con frecuencia cicatrizan mal tras una intervención. Este estudio descubre un grupo de células hasta ahora desconocido que ayuda a construir esta interfaz crítica y muestra cómo fuerzas mecánicas cotidianas, como el tirón muscular y el movimiento articular, guían su labor.
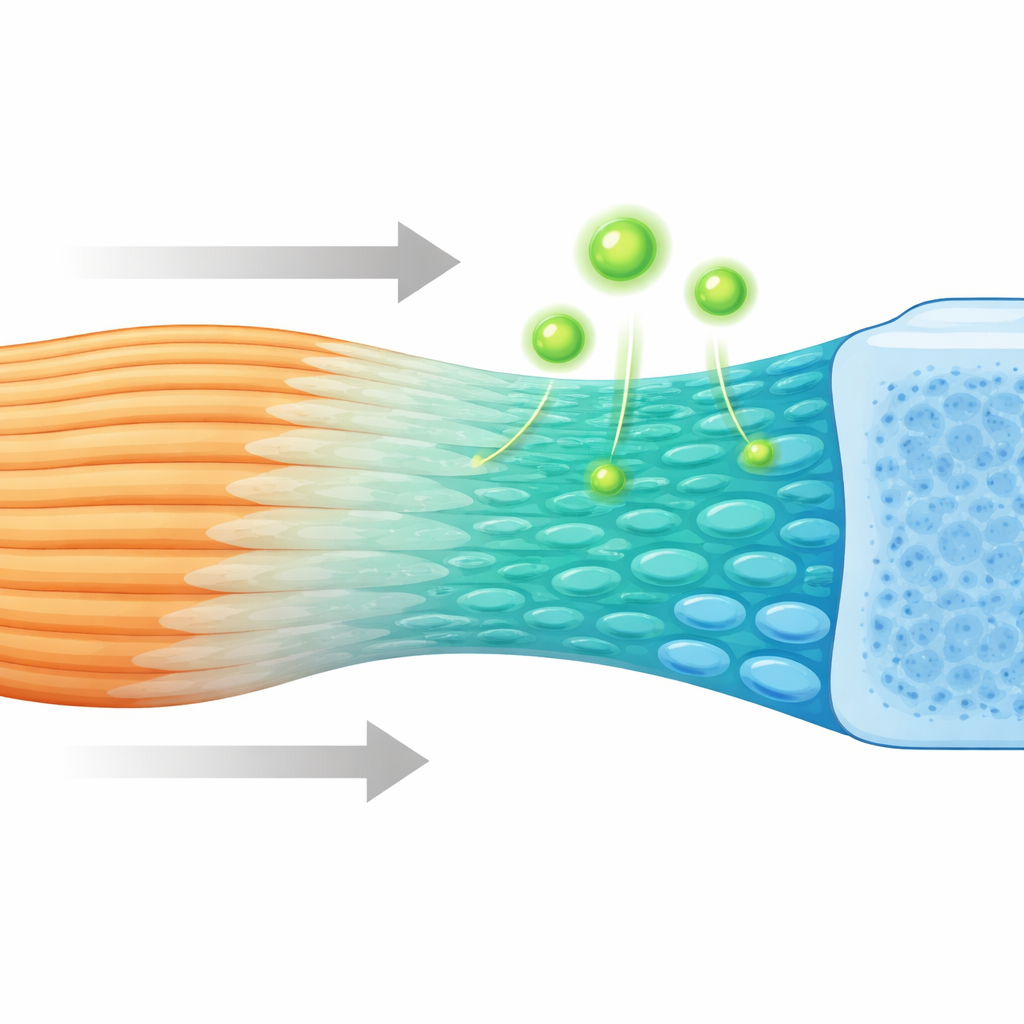
Una mirada más cercana a la unión oculta
Donde un tendón se ancla al hueso, el tejido no cambia bruscamente de blando a duro. En lugar de eso, atraviesa una delgada capa graduada de fibrocartílago que varía gradualmente en composición y rigidez. Este gradiente ayuda a suavizar las tensiones y a prevenir desgarros. Aunque los científicos sospechaban desde hace tiempo que células progenitoras especializadas debían construir esta zona, la identidad y el comportamiento de esas células habían permanecido poco claros. Mediante cartografiado espacial de genes de alta resolución y secuenciación de células individuales en ratones, los investigadores trazaron cómo se disponen miles de células individuales y qué genes activan a medida que la inserción se forma y madura.
Descubrimiento de una célula constructora especializada
Siguiendo la actividad génica desde la vida embrionaria tardía hasta el primer mes tras el nacimiento, el equipo identificó una población distintiva de células progenitoras marcada por el gen Tnn (que codifica la molécula de matriz tenascina-W). Estas células Tnn-positivas aparecen temprano en la interfase tendón–hueso, en una banda estrecha separada de las células tendinosas ordinarias y del cartílago del extremo óseo cercano. Experimentos de trazado de linaje mostraron que las células marcadas por Tnn y sus descendientes permanecen concentradas en la región de fibrocartílago y están estrechamente asociadas con zonas que más tarde se mineralizarán. Con el tiempo, estas células pasan de un estado flexible y similar al de células madre a un papel comprometido en la producción de cartílago y matriz rica en mineral, actuando esencialmente como constructores dedicados del fibrocartílago de la inserción tendinosa.
Qué ocurre cuando se pierden estos constructores
Para poner a prueba si los progenitores Tnn-positivos son realmente necesarios, los investigadores crearon ratones en los que estas células podían ser eliminadas selectivamente después del nacimiento. Cuando se ablacionaron las células Tnn-positivas, el fibrocartílago en la inserción tendinosa se desarrolló de forma anómala. La estructura normalmente estratificada se volvió delgada y desorganizada, con células de fibrocartílago menos numerosas y de menor tamaño. El análisis por imagen a escalas microscópicas y tridimensionales reveló un contenido mineral reducido y un hueso subcondral más débil bajo la zona de inserción. Las pruebas mecánicas confirmaron que estas entesis alteradas eran menos rígidas y presentaban una resistencia material inferior, lo que indica que la pérdida de la población progenitora conduce a una conexión tendón-hueso estructural y funcionalmente deficiente.
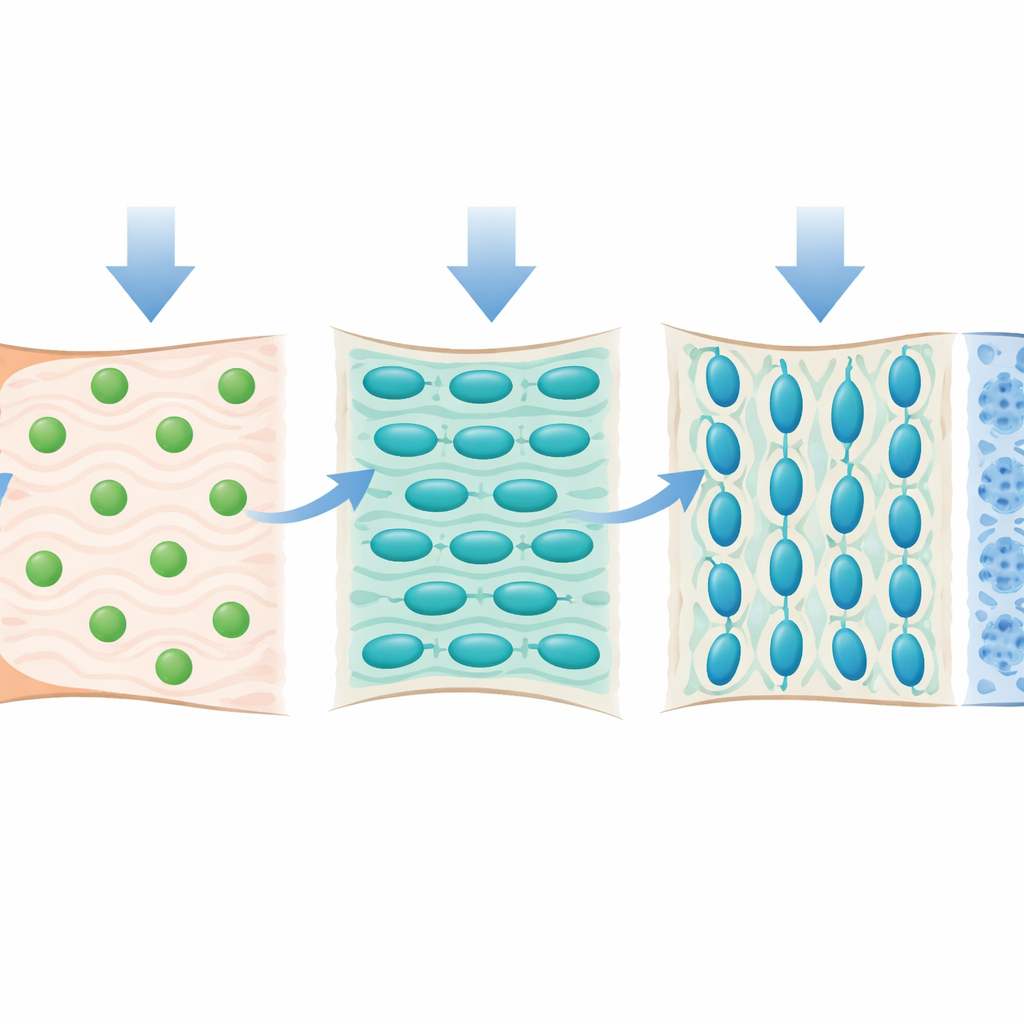
Cómo la carga y el movimiento moldean la interfaz
El estudio también investigó cómo las fuerzas mecánicas influyen sobre estos progenitores. Los investigadores usaron toxina botulínica para paralizar parcialmente un músculo del hombro, reduciendo en gran medida el tirón normal sobre el tendón durante el crecimiento. Bajo estas condiciones sin carga, el fibrocartílago permaneció poco desarrollado: las células eran más pequeñas, la matriz más fina y componentes clave del cartílago, como el colágeno tipo II, se vieron notablemente reducidos. El análisis de células individuales mostró que el número de progenitores Tnn-positivos disminuyó, y los que permanecieron mostraron una menor capacidad para madurar hacia células productoras de cartílago. Genes implicados en la construcción de matriz, la mineralización y canales iónicos mecanosensores también se vieron atenuados, lo que sugiere que las células Tnn-positivas están sintonizadas para detectar y responder a señales mecánicas.
Qué significa esto para la curación y la reparación
En términos sencillos, este trabajo muestra que una oleada transitoria y precoz de células progenitoras Tnn-positivas construye específicamente el fibrocartílago que ancla el tendón al hueso, y que la carga mecánica normal es esencial tanto para mantener su número como para desbloquear su potencial formador de cartílago. Cuando estas células se eliminan, o cuando se suprime el tirón muscular, la zona de inserción queda achaparrada y mecánicamente débil. Estas ideas ayudan a explicar por qué las reparaciones tendón-hueso pueden fallar y señalan estrategias futuras: las terapias podrían necesitar tanto reclutar o proteger progenitores especializados en la entesis como proporcionar estimulación mecánica adecuada para guiarlos, con el fin de regenerar realmente una conexión tendón-hueso graduada y duradera.
Cita: Zhang, T., Zhang, L., Yuan, Z. et al. Identification of a new population of Tnn+ progenitors to form tendon enthesis fibrocartilage. Bone Res 14, 43 (2026). https://doi.org/10.1038/s41413-026-00519-3
Palabras clave: entesis tendinosa, fibrocartílago, células progenitoras, carga mecánica, regeneración de tejidos