Clear Sky Science · fr
Identification d'une nouvelle population de précurseurs Tnn+ formant le fibrocartilage de l’enthèse tendineuse
Pourquoi la liaison tendon‑os importe
Chaque fois que vous lancez une balle, montez des escaliers ou prenez appui pour courir, des jonctions invisibles de votre corps réalisent quelque chose d'exceptionnel : elles relient le tendon souple et élastique à l'os dur et rigide. Ces zones de transition, appelées sites d'attache tendineuse, sont des points fréquents de blessure et cicatrisent souvent mal après une intervention chirurgicale. Cette étude met au jour un groupe de cellules jusque‑là inconnu qui contribue à construire cette interface essentielle et montre comment des forces mécaniques quotidiennes, comme la traction musculaire et le mouvement des articulations, guident leur action.
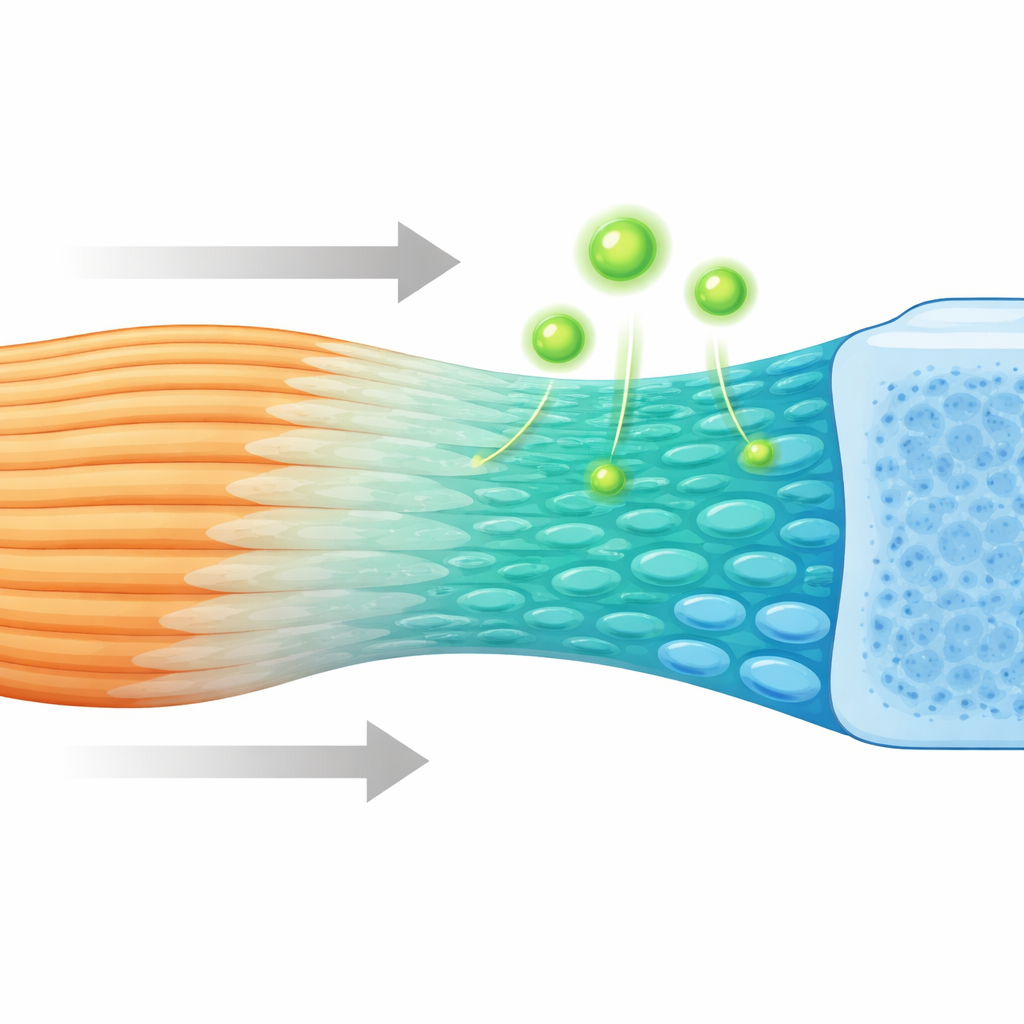
Un regard rapproché sur la jonction cachée
Là où un tendon s'ancre dans un os, le tissu ne passe pas brusquement du mou au dur. Il traverse plutôt une fine couche graduée de fibrocartilage dont la composition et la rigidité évoluent progressivement. Ce gradient aide à lisser les contraintes et à prévenir les déchirures. Si les scientifiques soupçonnaient depuis longtemps que des cellules progénitrices spécialisées construisent cette zone, l'identité et le comportement de ces cellules restaient flous. En combinant cartographie spatiale des gènes à haute résolution et séquençage unicellulaire chez la souris, les chercheurs ont cartographié l'agencement de milliers de cellules individuelles et les gènes qu'elles activent au fur et à mesure de la formation et de la maturation de l'attache.
Découverte d'une cellule bâtisseuse spécialisée
En suivant l'activité génique de la fin de la vie embryonnaire jusqu'au premier mois après la naissance, l'équipe a identifié une population distincte de cellules progénitrices marquées par le gène Tnn (qui code la molécule matricielle tenascin‑W). Ces cellules Tnn‑positives apparaissent tôt à l'interface tendon–os, dans une bande étroite distincte des cellules tendineuses ordinaires et du cartilage de l'extrémité osseuse voisine. Des expériences de traçage de lignage ont montré que les cellules marquées par Tnn et leurs descendants restent concentrés dans la région de fibrocartilage et sont étroitement associées aux zones qui se minéraliseront ultérieurement. Au fil du temps, ces cellules passent d'un état flexible, de type souche, à un rôle engagé dans la production de cartilage et d'une matrice riche en minéraux, agissant essentiellement comme des constructeurs dédiés du fibrocartilage d'attache tendineuse.
Que se passe‑t‑il lorsque ces bâtisseurs disparaissent
Pour tester si les progéniteurs Tnn‑positifs sont réellement nécessaires, les chercheurs ont créé des souris dans lesquelles ces cellules pouvaient être éliminées sélectivement après la naissance. Lorsque les cellules Tnn‑positives ont été ablatées, le fibrocartilage de l'attache tendineuse s'est développé de façon anormale. La structure normalement en couches est devenue mince et désorganisée, avec moins de cellules de fibrocartilage et des cellules de plus petite taille. Des imageries microscopiques et tridimensionnelles ont révélé une réduction de la teneur en minéraux et un affaiblissement de l'os sous‑chondral sous la zone d'attache. Des essais mécaniques ont confirmé que ces enthèses altérées étaient moins rigides et présentaient une résistance matérielle plus faible, indiquant que la perte de cette population progénitrice conduit à une connexion tendon‑os structurellement et fonctionnellement inférieure.
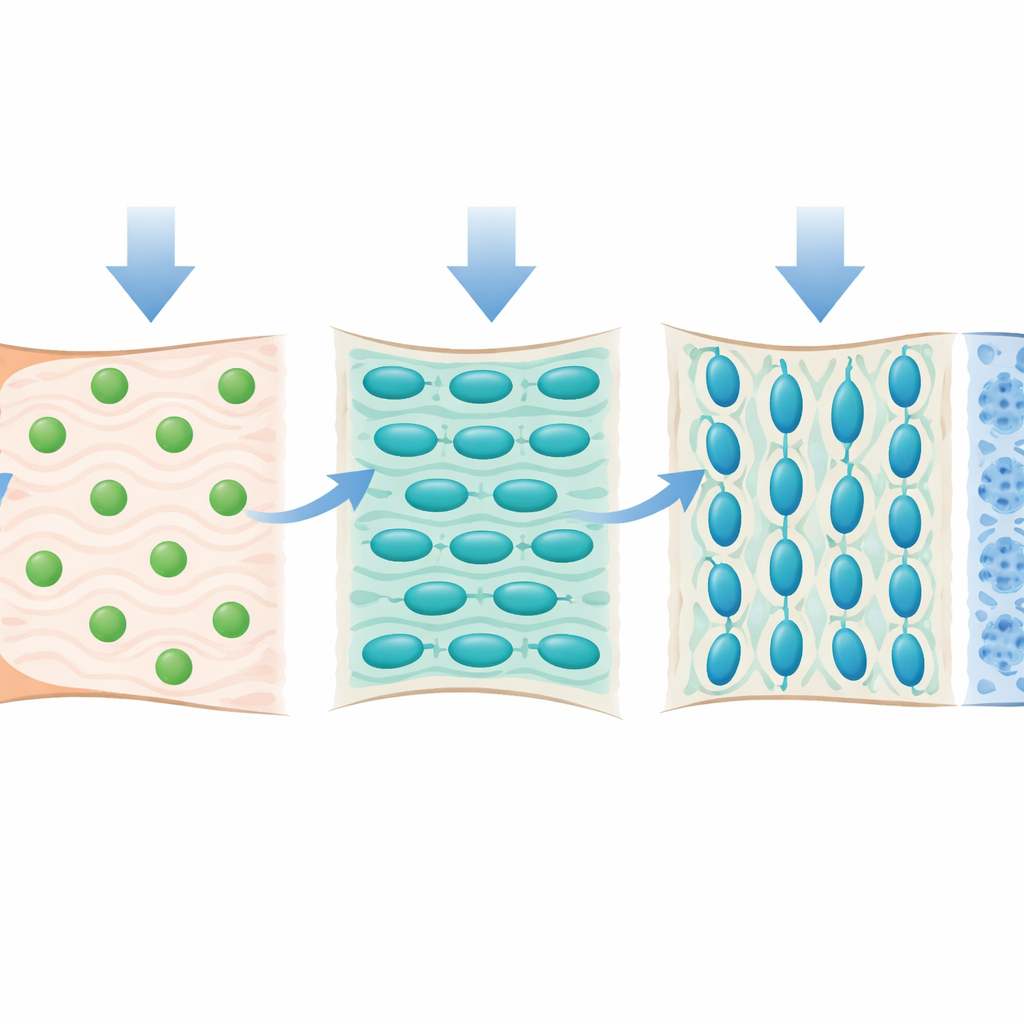
Comment la charge et le mouvement façonnent l'interface
L'étude a également exploré comment les forces mécaniques influencent ces cellules progénitrices. Les investigateurs ont utilisé la toxine botulique pour paralyser partiellement un muscle de l'épaule, réduisant fortement la traction normale exercée sur le tendon pendant la croissance. Dans ces conditions de décharge, le fibrocartilage est resté sous‑développé : les cellules étaient plus petites, la matrice plus mince et des composants clés du cartilage, comme le collagène de type II, étaient nettement réduits. L'analyse unicellulaire a montré que le nombre de progéniteurs Tnn‑positifs diminuait, et que ceux qui restaient avaient une capacité moindre à maturer en cellules productrices de cartilage. Les gènes impliqués dans la construction de la matrice, la minéralisation et les canaux ioniques de mécanosensation étaient également atténués, suggérant que les cellules Tnn‑positives sont réglées pour percevoir et répondre aux signaux mécaniques.
Ce que cela implique pour la guérison et la réparation
Concrètement, ce travail montre qu'une vague transitoire et précoce de cellules progénitrices Tnn‑positives construit spécifiquement le fibrocartilage qui ancre le tendon à l'os, et que la charge mécanique normale est essentielle à la fois pour maintenir leur nombre et pour libérer leur potentiel à former du cartilage. Lorsque ces cellules sont supprimées, ou lorsque la traction musculaire disparaît, la zone d'attache reste avortée et mécaniquement faible. Ces connaissances aident à expliquer pourquoi les réparations tendon‑os peuvent échouer et orientent des stratégies futures : les thérapies devront probablement à la fois recruter ou protéger les progéniteurs spécialisés à l'enthèse et fournir une stimulation mécanique appropriée pour les guider, afin de régénérer durablement une connexion tendon‑os graduée et résistante.
Citation: Zhang, T., Zhang, L., Yuan, Z. et al. Identification of a new population of Tnn+ progenitors to form tendon enthesis fibrocartilage. Bone Res 14, 43 (2026). https://doi.org/10.1038/s41413-026-00519-3
Mots-clés: enthèse tendineuse, fibrocartilage, cellules progénitrices, charge mécanique, régénération tissulaire