Clear Sky Science · it
Identificazione di una nuova popolazione di progenitori Tnn+ per formare il fibrocartilagine dell’inserzione tendinea
Perché il collegamento tendine-osso è importante
Ogni volta che lanci una palla, sali le scale o spingi per correre, giunzioni invisibili nel tuo corpo compiono qualcosa di notevole: connettono il tendine, morbido ed elastico, all’osso, duro e rigido. Queste piccole zone di transizione, chiamate siti di inserzione tendinea, sono punti frequenti di lesione e spesso guariscono male dopo un intervento chirurgico. Questo studio svela un gruppo di cellule finora sconosciuto che contribuisce a costruire questa interfaccia critica e mostra come forze meccaniche quotidiane, come la trazione muscolare e il movimento articolare, guidino il loro operato.
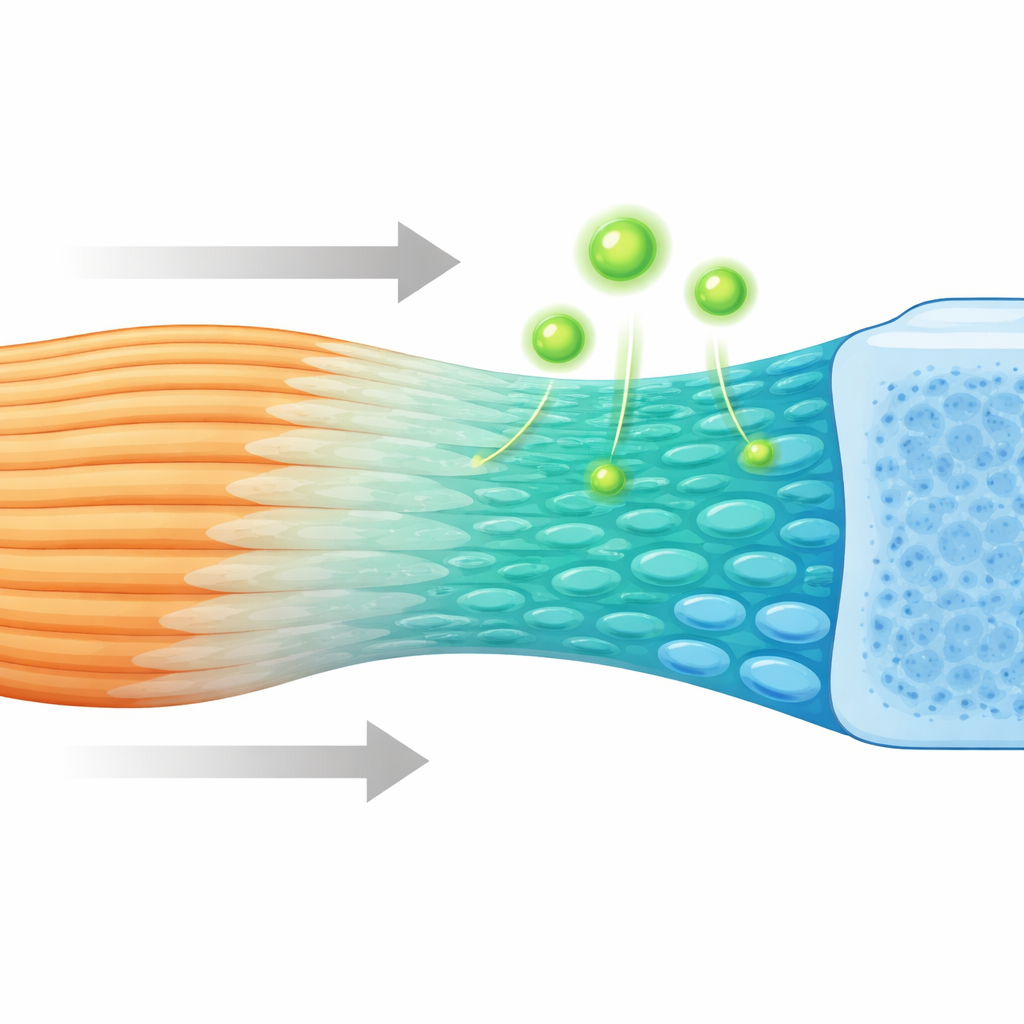
Uno sguardo più attento alla giunzione nascosta
Dove un tendine si ancora all’osso, il tessuto non cambia bruscamente da morbido a duro. Piuttosto, attraversa uno strato sottile e graduale di fibrocartilagine che varia progressivamente in composizione e rigidità. Questo gradiente aiuta ad attenuare lo stress e a prevenire lacerazioni. Sebbene gli scienziati sospettassero da tempo che cellule progenitrici specializzate costruiscano questa zona, l’identità e il comportamento di tali cellule sono rimasti poco chiari. Utilizzando mappature geniche spaziali ad alta risoluzione e sequenziamento single-cell nei topi, i ricercatori hanno tracciato come migliaia di singole cellule siano disposte e quali geni attivino mentre l’inserzione si forma e matura.
Scoperta di una cellula costruttrice specializzata
Seguendo l’attività genica dalla tarda vita embrionale fino al primo mese dopo la nascita, il gruppo ha identificato una popolazione distinta di cellule progenitrici contrassegnate dal gene Tnn (che codifica la molecola di matrice tenascina-W). Queste cellule Tnn-positive compaiono precocemente all’interfaccia tendine–osso, in una banda stretta separata dalle normali cellule tendinee e dalla cartilagine dell’estremità ossea vicina. Esperimenti di lineage-tracing hanno mostrato che le cellule marcate da Tnn e i loro discendenti rimangono concentrate nella regione di fibrocartilagine e sono strettamente associate a zone che in seguito si mineralizzeranno. Col tempo, queste cellule passano da uno stato flessibile e simile a cellule staminali a un ruolo impegnato nella produzione di cartilagine e matrice ricca di minerali, agendo essenzialmente come costruttori dedicati del fibrocartilagine dell’inserzione tendinea.
Cosa succede quando questi costruttori vengono persi
Per verificare se i progenitori Tnn-positivi siano davvero necessari, i ricercatori hanno creato topi in cui queste cellule potevano essere eliminate selettivamente dopo la nascita. Quando le cellule Tnn-positive sono state ablazionate, il fibrocartilagine all’inserzione tendinea si è sviluppato in modo anomalo. La struttura normalmente stratificata è diventata sottile e disorganizzata, con cellule di fibrocartilagine meno numerose e di dimensioni inferiori. Immagini a scala microscopica e tridimensionale hanno rivelato una riduzione del contenuto minerale e un indebolimento dell’osso subcondrale sotto la zona di inserzione. Test meccanici hanno confermato che queste entesi alterate erano meno rigide e presentavano una minore resistenza del materiale, indicando che la perdita della popolazione progenitrice porta a una connessione tendine-osso strutturalmente e funzionalmente inferiore.
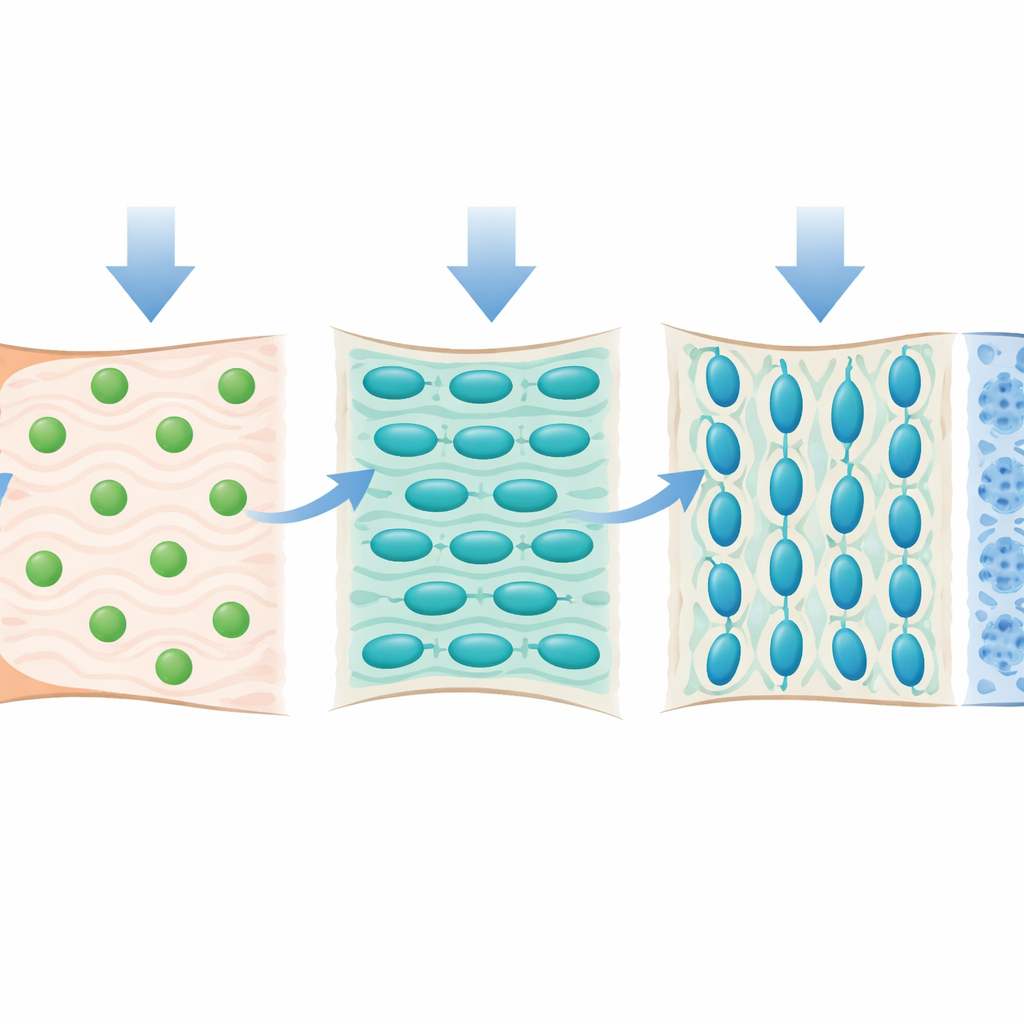
Come carico e movimento plasmano l’interfaccia
Lo studio ha anche indagato come le forze meccaniche influenzino questi progenitori. Gli investigatori hanno utilizzato la tossina botulinica per paralizzare parzialmente un muscolo della spalla, riducendo notevolmente la trazione normale sul tendine durante la crescita. In queste condizioni senza carico, il fibrocartilagine è rimasto sotto-sviluppato: le cellule erano più piccole, la matrice più sottile e componenti chiave della cartilagine come il collagene di tipo II erano marcatamente ridotti. L’analisi single-cell ha mostrato che il numero di progenitori Tnn-positivi è diminuito e che quelli rimasti mostravano una minore capacità di maturare in cellule produttrici di cartilagine. Anche i geni coinvolti nella costruzione della matrice, nella mineralizzazione e nei canali ionici meccanosensori risultavano attenuati, suggerendo che le cellule Tnn-positive sono sintonizzate per percepire e rispondere a segnali meccanici.
Cosa significa tutto questo per la guarigione e la riparazione
In termini semplici, questo lavoro mostra che un’onda transitoria e precoce di cellule progenitrici Tnn-positive costruisce specificamente il fibrocartilagine che ancora il tendine all’osso, e che il carico meccanico normale è essenziale sia per mantenere il loro numero sia per sbloccare il loro potenziale di formazione di cartilagine. Quando queste cellule vengono rimosse, o quando la trazione muscolare viene meno, la zona di inserzione resta arrestata nello sviluppo e meccanicamente debole. Queste intuizioni aiutano a spiegare perché le riparazioni tendine-osso possono fallire e indicano strategie future: le terapie potrebbero dover sia reclutare o proteggere progenitori specializzati all’enthesis sia fornire una stimolazione meccanica appropriata per guidarli, al fine di rigenerare realmente una connessione tendine-osso duratura e graduata.
Citazione: Zhang, T., Zhang, L., Yuan, Z. et al. Identification of a new population of Tnn+ progenitors to form tendon enthesis fibrocartilage. Bone Res 14, 43 (2026). https://doi.org/10.1038/s41413-026-00519-3
Parole chiave: inserzione tendinea, fibrocartilagine, cellule progenitrici, carico meccanico, rigenerazione tissutale