Clear Sky Science · pl
TAK1 jest kluczowym regulatorem sygnalizacji onkogennych i blokady różnicowania w mięsaku prążkowanokomórkowym
Dlaczego to badanie nad rakiem dziecięcym ma znaczenie
Mięsak prążkowanokomórkowy to agresywny nowotwór wieku dziecięcego, który pod mikroskopem przypomina niedojrzałą tkankę mięśniową szkieletową. Komórki tych guzów mają genetyczne narzędzia potrzebne do przekształcenia się w normalne mięśnie, lecz uporczywie odmawiają „dorastania”. Zamiast tego ciągle się dzielą i rozprzestrzeniają. W tym badaniu odkryto centralny przełącznik molekularny — białko zwane TAK1 — które pomaga utrzymywać komórki nowotworowe w tym niebezpiecznym, trwającym w nieskończoność stanie proliferacji. Wyłączenie TAK1 spowolniło wzrost guza i skłoniło komórki do przejścia w stronę bardziej przypominających normalne komórki mięśniowe.
Problem: zamrożone komórki mięśni u dzieci
Mięsak prążkowanokomórkowy stanowi około połowy wszystkich pediatrycznych mięsaków tkanek miękkich i znaczącą część nowotworów wieku dziecięcego. Występuje w dwóch głównych postaciach — embrionalnej i pęcherzykowej — napędzanych przez różne zmiany genetyczne. Mimo tych różnic obie formy mają wspólną cechę: komórki przypominają prekursorowe komórki mięśniowe utknięte we wczesnym stanie. Wyrażają regulatory budowy mięśni, ale nie kończą drogi do utworzenia dojrzałych włókien mięśniowych. Jednocześnie uruchamiają liczne szlaki wzrostu i przeżycia, co utrudnia leczenie jednym, ukierunkowanym lekiem. Klinicyści i naukowcy od dawna podejrzewali istnienie punktów kontroli wyżej w hierarchii, które koordynują te sygnały wzrostu i blokują różnicowanie, lecz trudno było je zidentyfikować.
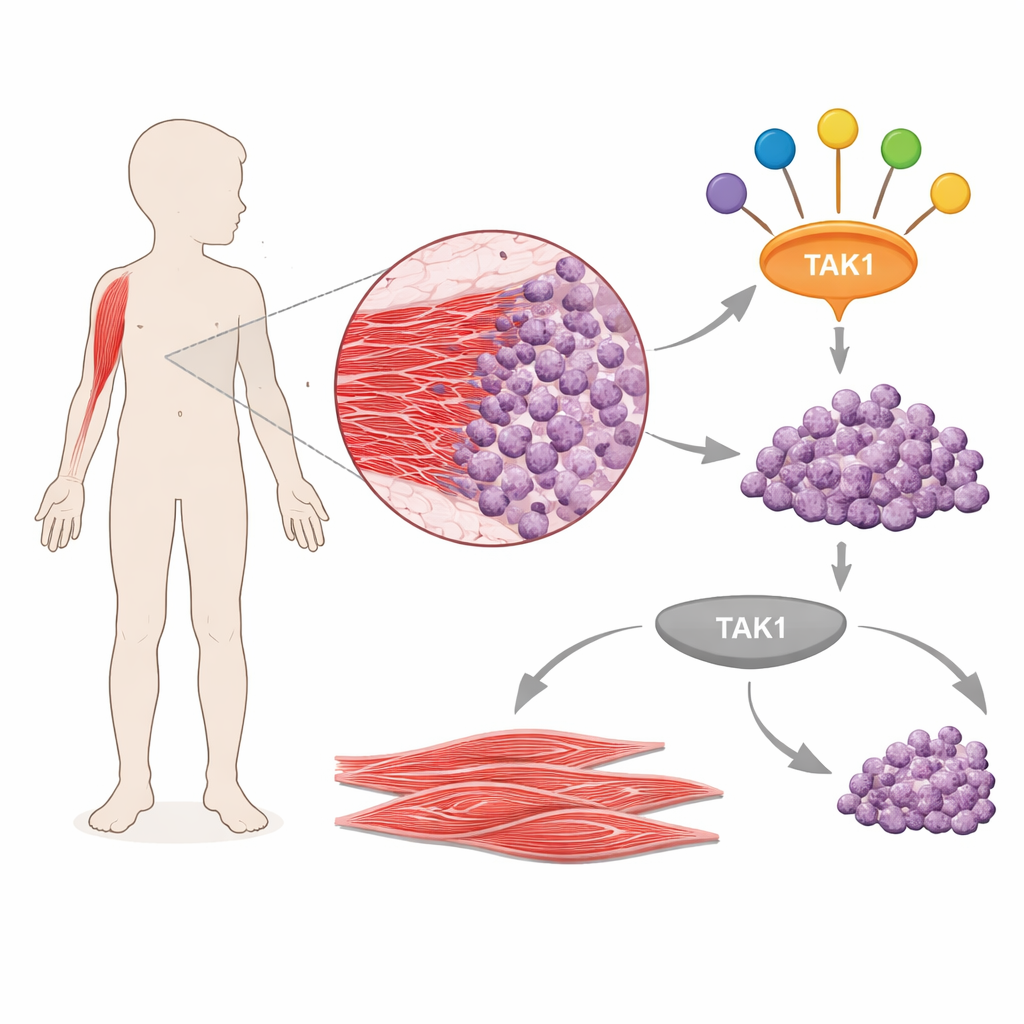
Przełącznik główny dla sygnałów nowotworowych
Zespół skupił się na TAK1, białku sygnałowym znanym z przekazywania informacji od czynników wzrostu i cząsteczek zapalnych do kilku głównych szlaków wewnątrz komórek. Analizując publicznie dostępne dane dotyczące ekspresji genów w próbkach pacjentów, wykazali, że TAK1 i kilka jego partnerów jest konsekwentnie podwyższonych w mięsakach prążkowanokomórkowych w porównaniu z normalnym mięśniem. Potwierdzili to w wielu liniach komórkowych pochodzących z ludzkich guzów, gdzie zarówno ilość TAK1, jak i jego aktywna, fosforylowana forma były wyższe niż w normalnych komórkach mięśniowych. Sugerowało to, że TAK1 nie tylko jest obecny, lecz także włączony w tych nowotworach i potencjalnie działa jako węzeł łączący kilka dróg wspierających rozwój raka.
Wyłączenie TAK1 spowalnia wzrost i rozprzestrzenianie
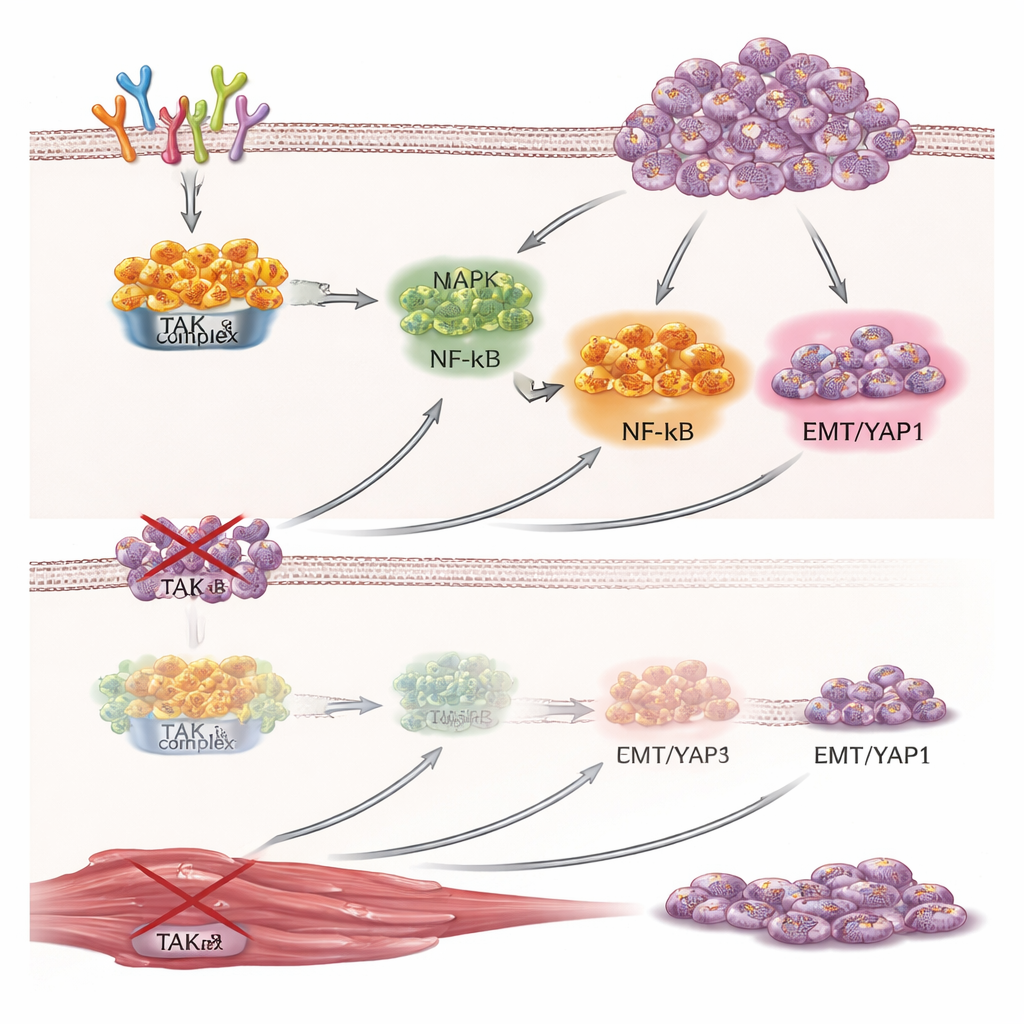
Aby przetestować rolę TAK1, badacze zastosowali dwie strategie zmniejszenia jego aktywności w hodowanych w laboratorium komórkach mięsaków prążkowanokomórkowych: wyciszanie genetyczne (za pomocą krótkich RNA typu hairpin lub małych interferujących RNA) oraz inhibitor małocząsteczkowy 5Z‑7‑oxozeaenol. Oba podejścia zdecydowanie zmniejszyły tempo podziałów komórkowych, mierzone przez syntezę DNA, aktywność metaboliczną i zdolność do tworzenia kolonii w czasie. Komórki stały się także mniej zdolne do migrowania przez pory i inwazji przez żel imitujący tkankę, co wskazuje, że TAK1 napędza zachowania związane z tworzeniem przerzutów. Duża skala sekwencjonowania RNA i analizy tablic proteinowych wykazała, że po wyciszeniu TAK1 wiele genów i białek powiązanych z cyklem komórkowym, sygnalizacją czynników wzrostu i przejściem epitelialno‑mezynchymalnym zostało przytłumionych, podczas gdy programy związane z budową struktury mięśnia i różnicowaniem zostały wzmocnione.
Uwolnienie hamulca różnicowania mięśni
Jednym z najbardziej uderzających efektów blokady TAK1 był wzrost markerów dojrzewania mięśni. W kilku liniach komórkowych mięsaka prążkowanokomórkowego zmniejszenie aktywności TAK1 prowadziło do znacznie większej liczby komórek wyrażających ciężkie łańcuchy miozyny i myogeninę — charakterystyczne białka późnych stadiów komórek mięśniowych. Reporter wrażliwy na ważny mięśniowo‑specyficzny promotor również stał się bardziej aktywny, co wskazuje, że mechanizmy ekspresji genów przesuwają się w kierunku programu mięśniowego. Dalsze analizy mechanistyczne powiązały część tego efektu z szlakiem Hippo–YAP1, dobrze znanym regulatorem wielkości narządów i nowotworów. Wyciszenie TAK1 zmniejszało poziomy białka YAP1. Gdy naukowcy przywrócili formę YAP1 odporną na degradację, w dużej mierze odwróciło to zwiększone różnicowanie mięśni wywołane utratą TAK1, co sugeruje, że TAK1 normalnie pomaga stabilizować YAP1 i poprzez niego utrzymuje komórki guza w niedojrzałym, proliferacyjnym stanie.
Testowanie TAK1 w guzach żywych organizmów
Hodowle komórkowe w szalce petri mogą opowiedzieć tylko część historii, więc zespół zaprojektował komórki mięsaka prążkowanokomórkowego z przełącznikiem celującym w TAK1, który można było wyłączyć podając myszom doksycyklinę. Gdy komórki te wszczepiono pod skórę myszy, guzy powstawały w obu grupach, lecz w zwierzętach leczonych doksycykliną rosły znacznie wolniej i ważyły mniej na koniec badania. Badanie mikroskopowe wykazało mniej dzielących się komórek i więcej wielojądrzastych, przypominających mięśnie komórek w guzach z wyciszonym TAK1. Analiza białek odzwierciedlała wyniki z hodowli komórek: poziomy TAK1 spadły, YAP1 zmniejszył się, a marker różnicowania mięśni — myogenina — wzrósł, wzmacniając ideę, że TAK1 podtrzymuje wzrost guza, jednocześnie aktywnie blokując wrodzoną tendencję komórek do dojrzewania.
Co to może oznaczać dla przyszłych terapii
Podsumowując, badanie wskazuje TAK1 jako centralnego koordynatora sygnałów promujących nowotwór w mięsakach prążkowanokomórkowych oraz jako kluczowego egzekutora zasady „braku dojrzewania”, która utrzymuje te komórki w szkodliwym, przypominającym komórki macierzyste stanie. Dzięki osłabieniu TAK1 badacze jednocześnie stłumili kilka szlaków wzrostu, zmniejszyli zachowania inwazyjne i umożliwili komórkom postęp w kierunku normalnego różnicowania mięśni, zarówno in vitro, jak i w guzach mysich. Dla pacjentów otwiera to perspektywę terapii, które robią więcej niż tylko zabijanie szybko dzielących się komórek: leki ukierunkowane na TAK1 mogłyby także skłaniać komórki nowotworowe do opuszczenia cyklu komórkowego i zmniejszenia złośliwości. Prace są nadal przedkliniczne, a takie kwestie jak dostarczanie leku, bezpieczeństwo i oporność trzeba będzie rozwiązać, lecz TAK1 wyróżnia się teraz jako obiecujący cel terapeutyczny w tym trudnym nowotworze dziecięcym.
Cytowanie: Vuong, A.T., Joshi, A.S., Roy, A. et al. TAK1 is a key regulator of oncogenic signaling and differentiation blockade in rhabdomyosarcoma. Oncogene 45, 1714–1728 (2026). https://doi.org/10.1038/s41388-026-03767-z
Słowa kluczowe: mięsak prążkowanokomórkowy, kinaza TAK1, nowotwór wieku dziecięcego, różnicowanie mięśni, sygnalizacja YAP1