Clear Sky Science · he
TAK1 הוא רגולטור מרכזי של איתות סרטני וחסימת התמיינות ברבדומיוסרקומה
מדוע מחקר זה על סרטן ילדות חשוב
רבדומיוסרקומה הוא סרטן בילדות אגרסיבי שנראה, תחת המיקרוסקופ, דומה מאוד לשריר שלדי לא בוגר. תאי הגידול הללו נושאים את הכלים הגנטיים הנדרשים כדי להפוך לשריר תקין, אך הם מסרבים להתבגר. במקום זאת הם ממשיכים להתחלק ולהתפשט. מחקר זה חושף מתג מולקולרי מרכזי, חלבון בשם TAK1, שמסייע לשמור על התאים הסרטניים במצב המסוכן של גדילה בלתי פוסקת. בכיבוי TAK1 הצליחו החוקרים להאט את גדילת הגידול ולעודד את התאים לכיוון הופעה ותפקוד דמויי שריר נורמלי.
הבעיה: תאי שריר תקועים בילדות
רבדומיוסרקומה מהווה כמות ניכרת מכלל הסרקומות הרכות בילדים וחלק משמעותי מסרטן בילדות בכלל. הוא מופיע בשני צורות עיקריות, עוברי (embryonal) ואלוואולרי (alveolar), שמונעות על ידי שינויים גנטיים שונים. למרות הבדלים אלה, שתי הצורות חולקות תכונה מפתח: תאי הגידול דומים לתאי גזע של שריר שנקלעו לשלב מוקדם. הם מבטאים רגולטורים לבניית שריר אך לא משלימים את המסלול להיווצרות סיבי שריר בוגרים. במקביל הם מפעילים מסלולי גדילה והישרדות מרובים, מה שמקשה על טיפול בעזרת תרופה ממוקדת אחת. קלינאים וחוקרים חשדו זמן רב שישנן נקודות בקרה עליונות שמרכזות את אותות הגדילה האלה וחוסמות התמיינות, אך קשה היה לזהות את המתגים הראשיים האלה.
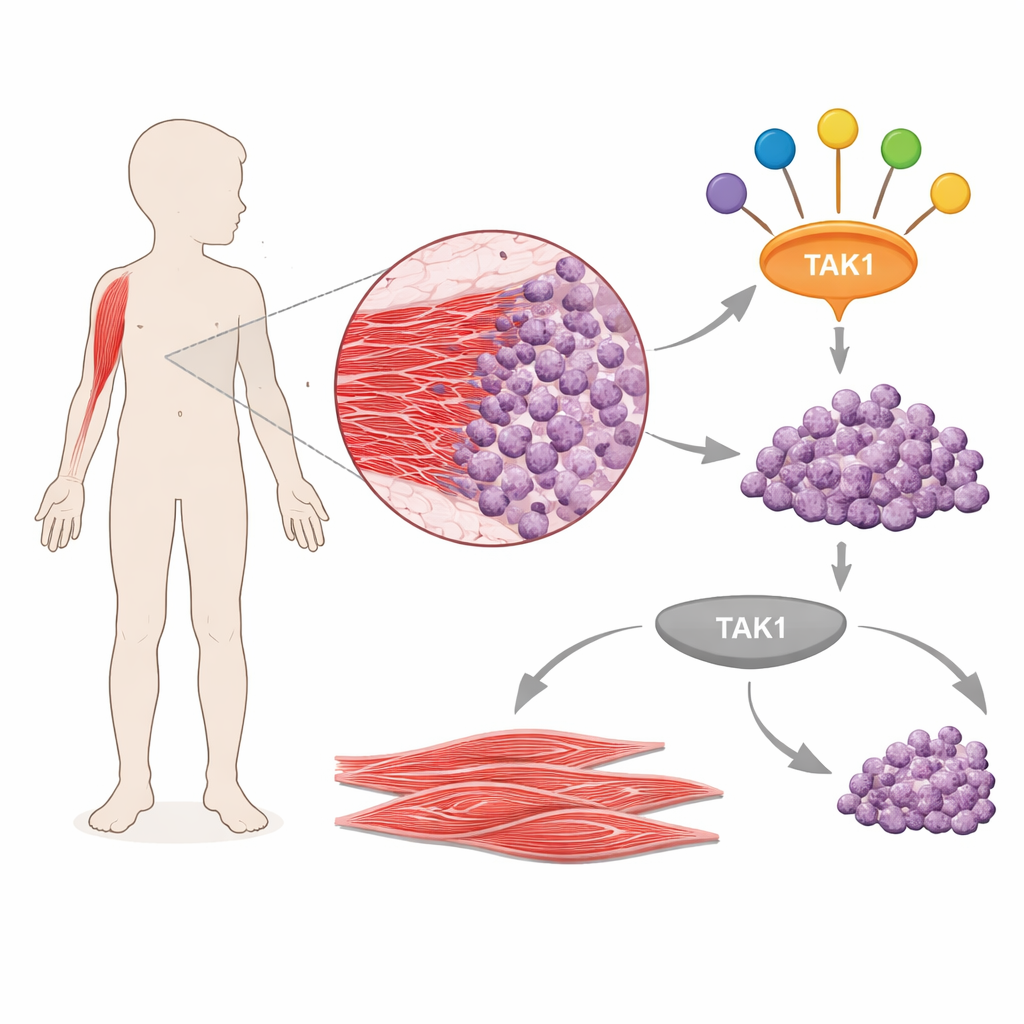
מתג ראשי לאותות סרטניים
הצוות התרכז ב‑TAK1, חלבון איתות הידוע כמשדר מסרים מתאי גידול וממולקולות דלקת למספר מסלולים מרכזיים בתא. על ידי כריית נתוני ביטוי גנים שזמינים לציבור מתוך גידולים של מטופלים, הם מצאו ש‑TAK1 וכמה מחלבוניו שותפים נמצאים באופן עקבי ברמות גבוהות ברבדומיוסרקומה בהשוואה לשריר נורמלי. הם איששו זאת במספר קווי תאים שמקורם בגידולים אנושיים, שם גם כמות TAK1 וגם הצורה הפעילה שלו המזורחנת היו גבוהים יותר מאשר בתאי שריר אנושיים רגילים. ממצא זה מרמז ש‑TAK1 אינו רק נוכח אלא גם פעיל בסרטנים אלה, ופועל כצומת שמחבר כמה מסלולים המעודדים סרטן בתוך התא.
כיבוי TAK1 מאט גדילה והתפשטות
כדי לבחון את תפקידו של TAK1 השתמשו החוקרים בשתי אסטרטגיות להפחתת פעולתו בתאי רבדומיוסרקומה במעבדה: דיכוי גנטי (באמצעות RNA בקשר שיער קצר או מולקולות RNA מתערבות קטנות) ומעכב מולקולרי קטן בשם 5Z‑7‑oxozeaenol. שתי הגישות הקטינו באופן משמעותי את קצב החלוקה של התאים הסרטניים, כפי שנמדד על ידי סינתזת DNA, פעילות מטבולית ויכולת יצירת מושבות לאורך זמן. התאים גם הפכו לפחות ניידים ופחות פולשניים כשהתרכזו לעבור דרך נקבים ולחדור דרך ג'ל המדמה רקמה, מה שמעיד ש‑TAK1 מסייע בהתנהגויות הקשורות למטסטזה. רצף RNA בקנה מידה רחב וניתוח מערכי חלבון הראו שכאשר TAK1 הושתק, גנים וחלבונים רבים הקשורים למחזור התא, איתות גורמי גדילה ומעבר אפיתלי‑מזנכימלי דוכאו, בעוד שתוכניות המעורבות בבניית מבנה השריר ובהתמיינות הוגברו.
שחרור הבלם על התמיינות שרירית
אחד ההשפעות המשמעותיות ביותר של חסימת TAK1 היה עליית סמנים של בגרות שרירית. במספר קווי תאים של רבדומיוסרקומה, הפחתת TAK1 הביאה לעלייה משמעותית במספר התאים שמבטאים שרשרת כבדה של מיוזין ומיוגנין, חלבונים המאפיינים שלבי התבגרות מאוחרים של תאי שריר. מד דוח הרגיש לפרומוטור חשוב הספציפי לשריר הפגין גם הוא פעילות מוגברת, מה שמעיד שמכונת ביטוי הגנים נעה לכיוון תוכנית שרירית. עבודת מנגנון נוספת שיזמה חלק מהאפקט הזה לנוכחות מסלול היפו‑YAP1 (Hippo–YAP1), רגולטור מוכר של גודל איברים וסרטן. דיכוי TAK1 הפחית את רמות חלבון YAP1. כאשר החוקרים החזירו צורה של YAP1 העמידה בפני פירוק, היא הביאה להחזרה חלקית של העידוד בהתמיינות השריר שנגרם על ידי אובדן TAK1, ורמזה ש‑TAK1 באופן רגיל מסייע לייצב את YAP1 ובאמצעותו שומר על תאי הגידול במצב לא מתמיין ומתחלק.
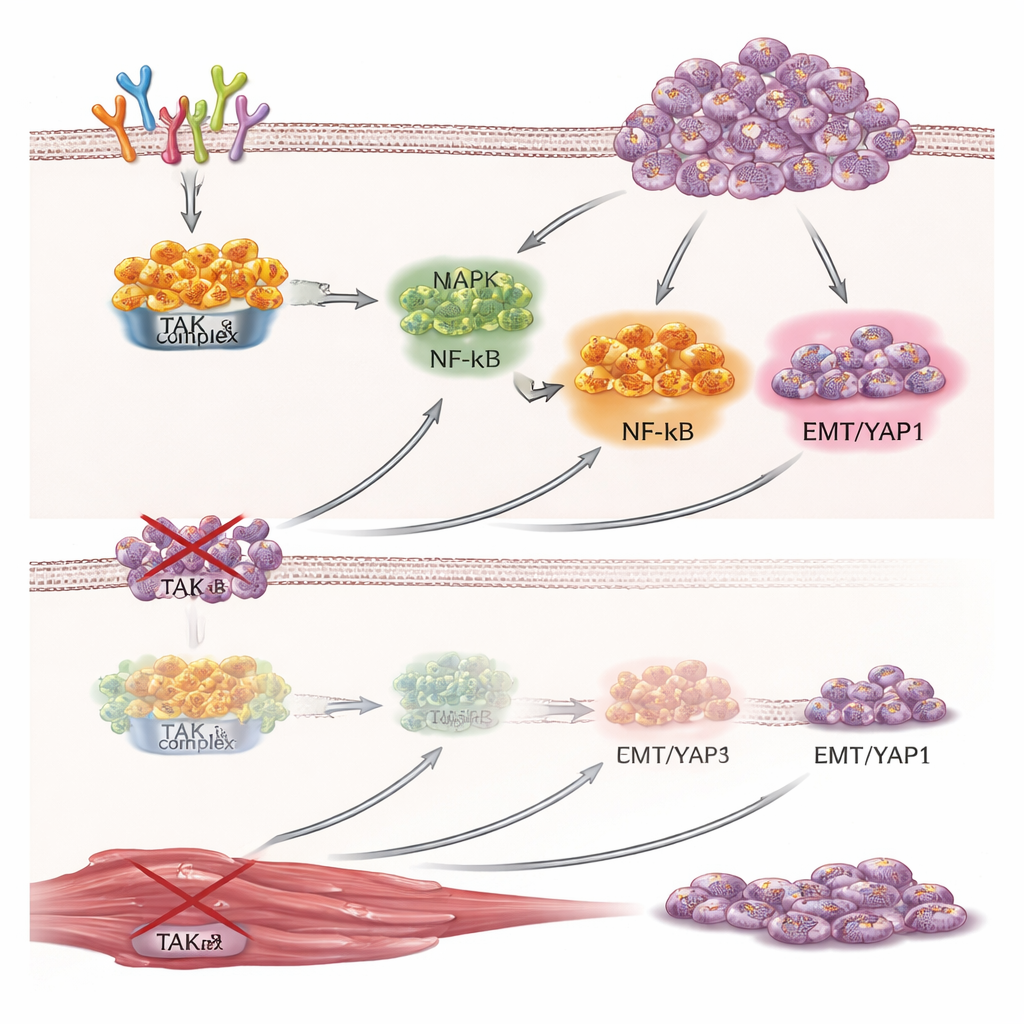
בדיקת TAK1 בגידולים חיים
צלחות מעבדה יכולות לספר רק חלק מהסיפור, ולכן הצוות מהנדס תאי רבדומיוסרקומה לשאת מתג המכוון ל‑TAK1 שניתן לכבותו על ידי מתן דוקסיציקלין בעכברים. כאשר תאים אלה הושתלו מתחת לעור של עכברים, נוצרו גידולים בשתי הקבוצות, אך אלו שקיבלו דוקסיציקלין גדלו הרבה יותר לאט ושקלו פחות בסיום המחקר. בדיקה מיקרוסקופית גילתה פחות תאים מתחלקים ויותר תאים רב‑גרעיניים ודמויי שריר בגידולים שבהם TAK1 הושתק. ניתוח חלבוני חזר על ממצאי תרבית התאים: רמות TAK1 ירדו, YAP1 הצטמצם וסמן ההתמיינות השרירית מיוגנין עלה, מה שחיזק את הרעיון ש‑TAK1 מקיים את גדילת הגידול ובו בזמן חוסם את הנטייה המולדת של התאים להתבגר.
מה יכול להיות לזה משמעות לטיפולים עתידיים
בסך הכל, המחקר מציב את TAK1 כרכז מרכזי של אותות המעודדים סרטן ברבדומיוסרקומה וכאכיפן של 'כלל אי‑הבשלה' השומר את התאים במצב מזוהם ושל תאי‑אם. על ידי הפחתת פעילות TAK1, החוקרים החלישו בו‑זמנית מספר מסלולי גדילה, הורידו התנהגות פולשנית ואפשרו לתאים להתקדם לכיוון התמיינות שרירית נורמלית, הן בתרבית תאים והן בגידולים בעכברים. עבור חולים, הדבר מעלה את האפשרות לטיפולים שלא רק מפחיתים את כמות התאים המחלקים במהירות: תרופות המכוונות ל‑TAK1 עשויות גם לדחוף תאי גידול לצאת ממחזור התא ולהפוך לפחות ממאירים. העבודה עדיין פרה‑קלינית, ויש לטפל בסוגיות כמו מתן תרופות, בטיחות והתנגדות, אך TAK1 בולט עכשיו כמטרה טיפולית מבטיחה בסרטן ילדות מאתגר זה.
ציטוט: Vuong, A.T., Joshi, A.S., Roy, A. et al. TAK1 is a key regulator of oncogenic signaling and differentiation blockade in rhabdomyosarcoma. Oncogene 45, 1714–1728 (2026). https://doi.org/10.1038/s41388-026-03767-z
מילות מפתח: רבדומיוסרקומה, קינאזת TAK1, סרטן בילדות, התמיינות שרירית, איתות YAP1