Clear Sky Science · ar
TAK1 منظم رئيسي للإشارات المسببة للسرطان ومسبب لحصار النضج في ورم اللحمة المخططية الهيكلية
لماذا تهم هذه الدراسة عن سرطانات الأطفال
ورم اللحمة المخططية الهيكلية هو سرطان طفولي عدواني يشبه، تحت المجهر، نسيج العضلة الهيكلية غير الناضج. تحمل خلايا الورم هذه الأدوات الجينية اللازمة لتصبح عضلة طبيعية، لكنها ترفض نضجها بعناد. بدلاً من ذلك تستمر في الانقسام والانتشار. تكشف هذه الدراسة عن مفتاح جزيئي مركزي، بروتين يدعى TAK1، يساعد على إبقاء خلايا السرطان هذه في حالة نمو خطيرة لا تتوقف. عند إيقاف عمل TAK1، تمكن الباحثون من إبطاء نمو الورم ودفع الخلايا نحو التشبه بخلايا عضلية أكثر طبيعية.
المشكلة: خلايا عضلية متوقفة في الأطفال
يشكل ورم اللحمة المخططية الهيكلية نحو نصف ساركومات الأنسجة الرخوة لدى الأطفال وجزءاً ملحوظاً من سرطانات الطفولة بشكل عام. يأتي في شكلين رئيسيين، جنيني وحويصلي، يدفعهما تغيّرات جينية مختلفة. بالرغم من هذه الاختلافات، يشتركان في سمة أساسية: خلاياه تبدو كمقدّمات عضلية عالقة في حالة مبكرة. تعبر عن منظمات بناء العضلات لكنها لا تكمل الرحلة لتشكيل ألياف عضلية ناضجة. وفي الوقت نفسه، تستفيد هذه الخلايا من مسارات متعددة للنمو والبقاء، ما يجعل معالجتها بصبغة دواء موجه واحد أمراً صعباً. لطالما اشتبه الأطباء والعلماء بوجود نقاط تحكم عليا تنسق هذه الإشارات وتعوق التمايز، لكن صعوبة تحديد هذه المفاتيح كانت كبيرة.
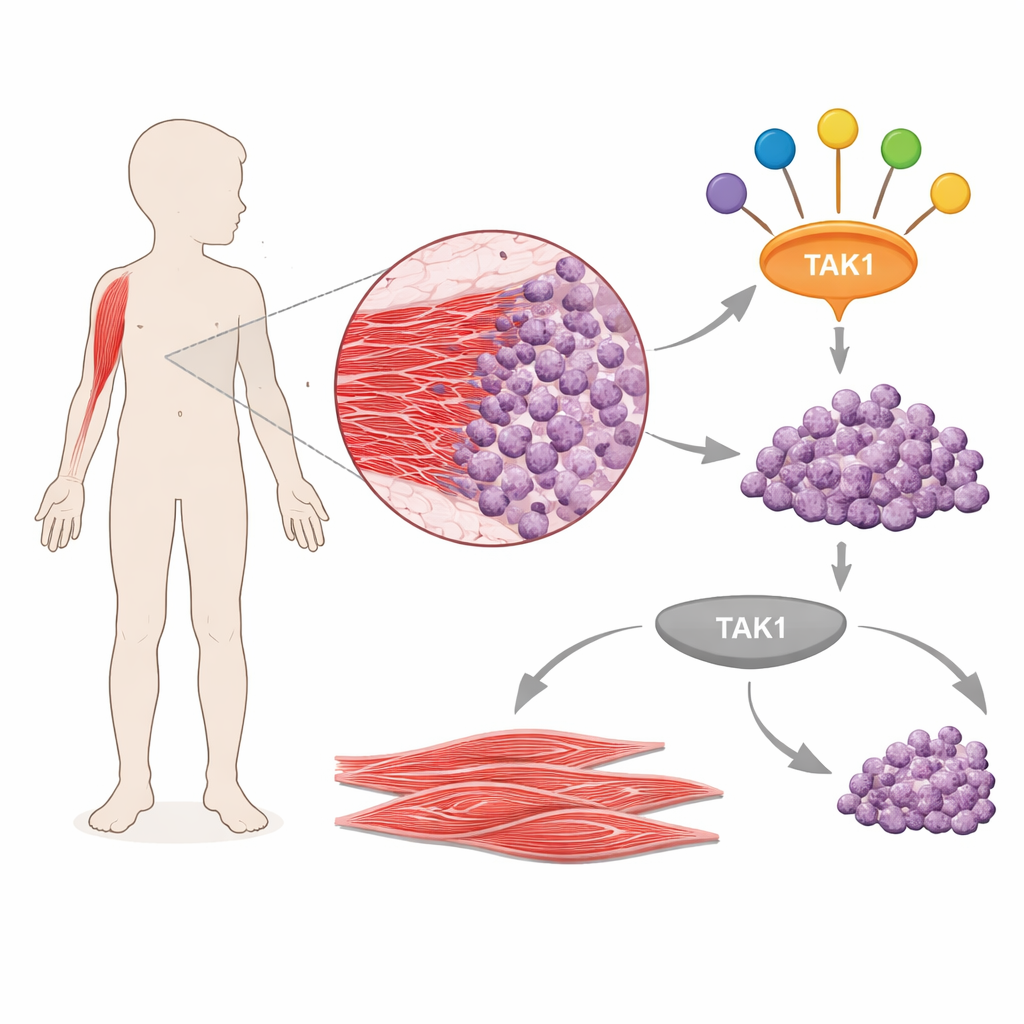
مفتاح رئيسي لإشارات السرطان
ركز الفريق على TAK1، بروتين إشاري معروف بنقله رسائل من عوامل النمو والجزيئات الالتهابية إلى عدة مسارات رئيسية داخل الخلايا. من خلال تحليل بيانات التعبير الجيني المتاحة للجمهور من أورام المرضى، وجدوا أن TAK1 وعدداً من بروتيناته الشريكة مرتفعة باستمرار في ورم اللحمة المخططية مقارنة بالعضلة الطبيعية. أكدوا ذلك في خطوط خلوية مشتقة من أورام بشرية متعددة، حيث كانت كمية TAK1 وشكله النشط المفسفر أعلى من خلايا العضلة البشرية الطبيعية. دل ذلك على أن TAK1 ليس موجوداً فحسب بل مفعل في هذه السرطانات، وربما يعمل كمحور يربط عدة مسارات مروجة للسرطان داخل الخلية.
خفض TAK1 يبطئ النمو والانتشار
لاختبار دور TAK1، استخدم الباحثون استراتيجيتين لتقليل نشاطه في خلايا ورم اللحمة المخططية المزروعة في المعمل: إسكات جيني (باستخدام RNA صغير الشعر أو RNA متداخل قصير) ومثبط جزيئي صغير يدعى 5Z‑7‑oxozeaenol. كلتا الطريقتين قللتا بشكل حاد من سرعة انقسام الخلايا السرطانية، كما قيس بواسطة تصنيع الحمض النووي، النشاط الأيضي، وقدرتها على تكوين مستعمرات عبر الزمن. أصبحت الخلايا أيضاً أقل قدرة على الهجرة عبر المسام وغزو الهلام المحاكي للنسيج، مما يشير إلى أن TAK1 يساهم في دفع سلوكيات مرتبطة بالانبثاث. أظهرت تحليلات تسلسل RNA واسعة النطاق ومصفوفات البروتين أنه عند إسكات TAK1، تم خفض العديد من الجينات والبروتينات المرتبطة بدورة الخلية، وإشارات عوامل النمو، والانتقال الظهاري-اللحمي، بينما تم تنشيط برامج معنية ببناء بنية العضلة والتمايز.
رفع المكابح عن تمايز العضلة
كانت إحدى التأثيرات اللافتة لحجب TAK1 هي قفزة في معالم نضج العضلة. عبر عدة خطوط خلوية لورم اللحمة المخططية، أدى تقليل TAK1 إلى زيادة عدد الخلايا المعبرة عن السلسلة الثقيلة للمايوسين والمايوجِنِين، وهما بروتينان مميزان لمرحلة العضلة المتأخرة. كما أصبح مؤشر تقريري حساس لمشغِّل عضلي مهم أكثر نشاطاً، مما يشير إلى أن آلية التعبير الجيني الأساسية تتحول نحو برنامج عضلي. أظهرت أعمال آلية إضافية أن جزءاً من هذا التأثير يعود إلى مسار Hippo–YAP1، المنظم المعروف لحجم الأعضاء والسرطان. خفض TAK1 قلل من مستويات بروتين YAP1. وعندما أعاد العلماء إدخال شكل من YAP1 يقاوم التحلل، عكس ذلك إلى حد بعيد التعزيز في التمايز العضلي الناجم عن فقد TAK1، ما يوحي بأن TAK1 يساعد عادة في تثبيت YAP1 ومن خلاله يبقي خلايا الورم في حالة غير متميزة وقابلة للتكاثر.
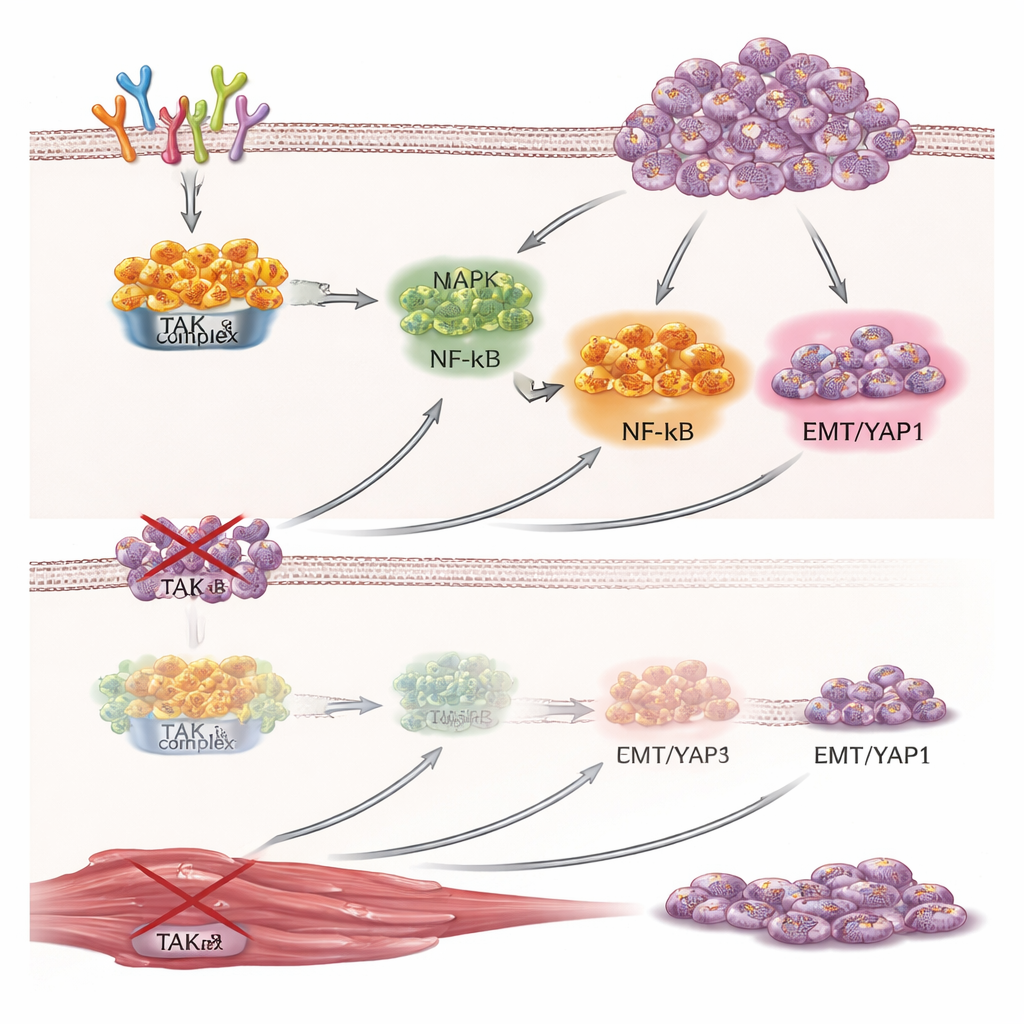
اختبار TAK1 في أورام حية
الأطباق المخبرية تروي جزءاً من القصة فقط، لذلك صنّع الفريق خلايا ورم اللحمة المخططية بحيث تحمل مفتاح استهداف TAK1 يمكن إيقافه بإطعام الفئران دوكسيسيكلين. عند زرع هذه الخلايا تحت جلد الفئران، تكونت أورام في كلا المجموعتين، لكن الأورام في الحيوانات المعالجة بالدوكسيسيكلين نمت أبطأ بكثير ووزنت أقل في نهاية الدراسة. أظهر الفحص المجهري خلايا أقل انقساماً والمزيد من الخلايا متعددة النوى الشبيهة بالعضلة في الأورام التي تم إسكات TAK1 فيها. عكست تحليلات البروتين نتائج مزارع الخلايا: انخفضت مستويات TAK1، وتناقص YAP1، وصعد علامة تمايز العضلة المايوجِنِين، مما يعزز الفكرة أن TAK1 يدعم نمو الورم بينما يعيق في الوقت نفسه ميل الخلايا الفطري إلى النضج.
ماذا قد يعني هذا للعلاجات المستقبلية
بشكل عام، تضع الدراسة TAK1 كمنسق مركزي للإشارات المروجة للسرطان في ورم اللحمة المخططية وكنافذ رئيسي لقاعدة "لا نضج" التي تبقي هذه الخلايا محتبسة في حالة جذعية ضارة. بخفض TAK1، أضعف الباحثون عدة مسارات نمو في آن واحد، قللوا السلوك الغازي، وسمحوا للخلايا بالتقدم نحو تمايز عضلي طبيعي، سواء في مزارع الخلايا أو في أورام الفئران. للمرضى، يفتح هذا احتمال علاجات لا تكتفي بقتل الخلايا سريعة الانقسام فحسب: فالمُثبِطات المستهدفة لـ TAK1 قد تدفع أيضاً خلايا الورم للخروج من دورة الخلية وتصبح أقل خباثة. العمل لا يزال قبل سريري، ويجب معالجة قضايا مثل توصيل الدواء، والسلامة، والمقاومة، لكن TAK1 يبرز الآن كهدف علاجي واعد في هذا السرطان الطفولي الصعب.
الاستشهاد: Vuong, A.T., Joshi, A.S., Roy, A. et al. TAK1 is a key regulator of oncogenic signaling and differentiation blockade in rhabdomyosarcoma. Oncogene 45, 1714–1728 (2026). https://doi.org/10.1038/s41388-026-03767-z
الكلمات المفتاحية: ورم اللحمة المخططية الهيكلية, كِيناز TAK1, سرطان الطفولة, تمايز العضلات, إشارة YAP1