Clear Sky Science · de
TAK1 ist ein Schlüsselregulator von onkogenem Signaling und Differenzierungsblockade beim Rhabdomyosarkom
Warum diese Studie zu einer Kinderkrebserkrankung wichtig ist
Das Rhabdomyosarkom ist ein aggressiver Kindeszeitkrebs, der unter dem Mikroskop stark unreifem Skelettmuskel ähnelt. Diese Tumorzellen besitzen die genetischen Werkzeuge, um zu normalem Muskel zu werden, weigern sich jedoch beharrlich, erwachsen zu werden. Stattdessen teilen sie sich weiter und breiten sich aus. Die Studie identifiziert einen zentralen molekularen Schalter, ein Protein namens TAK1, das dazu beiträgt, diese Krebszellen in ihrem gefährlichen, andauernden Wachstumszustand zu halten. Durch das Abschalten von TAK1 gelang es den Forschern, das Tumorwachstum zu verlangsamen und die Zellen in Richtung normaler, muskelähnlicher Zellen zu bringen.
Das Problem: eingefrorene Muskelzellen bei Kindern
Das Rhabdomyosarkom macht etwa die Hälfte aller pädiatrischen Weichteilsarkome und einen bemerkenswerten Anteil der kindlichen Krebserkrankungen insgesamt aus. Es tritt in zwei Hauptformen auf, embryonal und alveolär, die durch unterschiedliche genetische Veränderungen angetrieben werden. Trotz dieser Unterschiede teilen beide eine zentrale Eigenschaft: Ihre Zellen ähneln Muskelvorläufern, die in einem frühen Zustand feststecken. Sie exprimieren Muskelaufbau‑Regulatoren, schließen den Weg zur Bildung reifer Muskelfasern jedoch nicht ab. Gleichzeitig nutzen sie mehrere Wachstums‑ und Überlebenswege, was die Behandlung mit einem einzelnen zielgerichteten Medikament erschwert. Kliniker und Wissenschaftler vermuteten lange, dass es übergeordnete Kontrollpunkte geben muss, die diese Wachstumssignale koordinieren und die Differenzierung blockieren, doch diese Schalter waren nur schwer festzustellen.
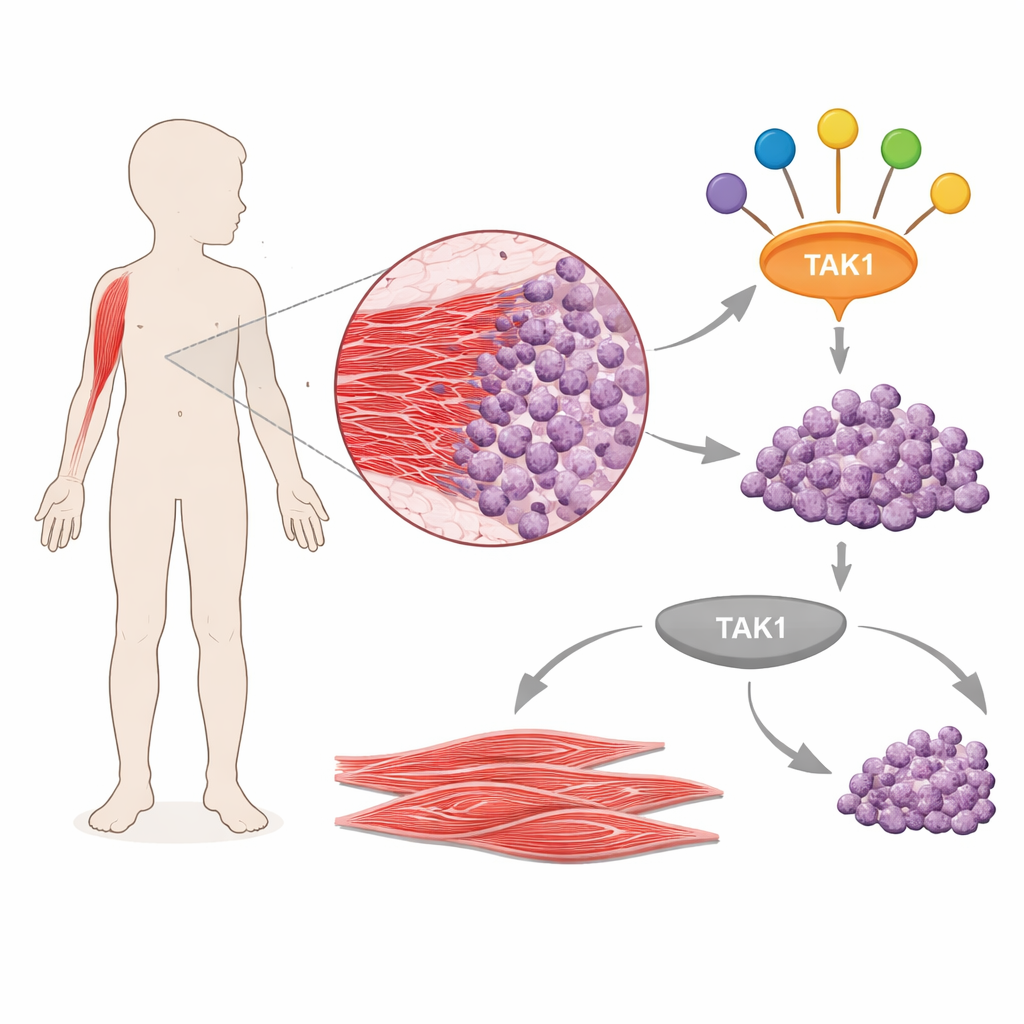
Ein Hauptschalter für Krebs‑Signale
Das Team konzentrierte sich auf TAK1, ein Signaling‑Protein, das dafür bekannt ist, Signale von Wachstumsfaktoren und Entzündungsmolekülen in mehrere wichtige intrazelluläre Wege weiterzuleiten. Durch Auswertung öffentlich verfügbarer Genexpressionsdaten aus Patientenproben fanden sie, dass TAK1 und mehrere seiner Partnerproteine im Rhabdomyosarkom im Vergleich zu normalem Muskel durchgängig erhöht sind. Dies bestätigte sich in mehreren aus humanen Tumoren abgeleiteten Zelllinien, in denen sowohl die Menge an TAK1 als auch seine aktive, phosphorylierte Form höher war als in normalen menschlichen Muskelzellen. Das deutete darauf hin, dass TAK1 in diesen Tumoren nicht nur vorhanden, sondern aktiviert ist und möglicherweise als Knotenpunkt fungiert, der mehrere krebsfördernde Wegstrecken innerhalb der Zelle verknüpft.
TAK1‑Reduktion bremst Wachstum und Ausbreitung
Um die Rolle von TAK1 zu testen, verwendeten die Forscher zwei Strategien, um seine Aktivität in im Labor kultivierten Rhabdomyosarkomzellen zu verringern: genetisches Herunterregeln (mittels short hairpin RNA oder small interfering RNA) und einen kleinmolekularen Inhibitor namens 5Z‑7‑oxozeaenol. Beide Ansätze verringerten deutlich die Teilungsrate der Krebszellen, gemessen an DNA‑Synthese, Stoffwechselaktivität und ihrer Fähigkeit, über Zeit Kolonien zu bilden. Die Zellen waren zudem weniger in der Lage, durch Poren zu migrieren und durch ein Gele zu invasieren, das Gewebe nachahmt, was darauf hinweist, dass TAK1 Verhaltensweisen antreibt, die mit Metastasierung assoziiert sind. Umfangreiche RNA‑Sequenzierungen und Proteinarray‑Analysen zeigten, dass bei Silencing von TAK1 viele Gene und Proteine, die mit Zellzyklus, Wachstumsfaktor‑Signalübertragung und epithelial‑mesenchymaler Transition verbunden sind, herunterreguliert wurden, während Programme zur Ausbildung von Muskelstruktur und Differenzierung hochgefahren wurden.
Die Bremse der Muskel‑Differenzierung lösen
Einer der auffälligsten Effekte der TAK1‑Blockade war ein Anstieg von Markern der Muskelreifung. In mehreren Rhabdomyosarkom‑Zelllinien führte die Reduktion von TAK1 dazu, dass deutlich mehr Zellen Myosin‑Schwerketten und Myogenin exprimierten — typische Proteine spätstadialer Muskelzellen. Ein Reporter, der auf einen wichtigen musclespezifischen Promotor reagiert, wurde ebenfalls aktiver, was anzeigt, dass die zugrunde liegende Genexpressionsmaschinerie sich in Richtung eines Muskelprogramms verschiebt. Weitere mechanistische Untersuchungen führten einen Teil dieses Effekts auf den Hippo–YAP1‑Signalweg zurück, einen bekannten Regulator von Organgröße und Krebs. TAK1‑Silencing verringerte die YAP1‑Proteinspiegel. Wenn die Wissenschaftler eine Form von YAP1 wieder einführten, die gegen Abbau resistent ist, hob dies weitgehend den durch TAK1‑Verlust induzierten Zuwachs an Muskel‑Differenzierung auf, was darauf hindeutet, dass TAK1 normalerweise hilft, YAP1 zu stabilisieren und über diesen Weg die Tumorzellen in einem undifferenzierten, proliferativen Zustand hält.
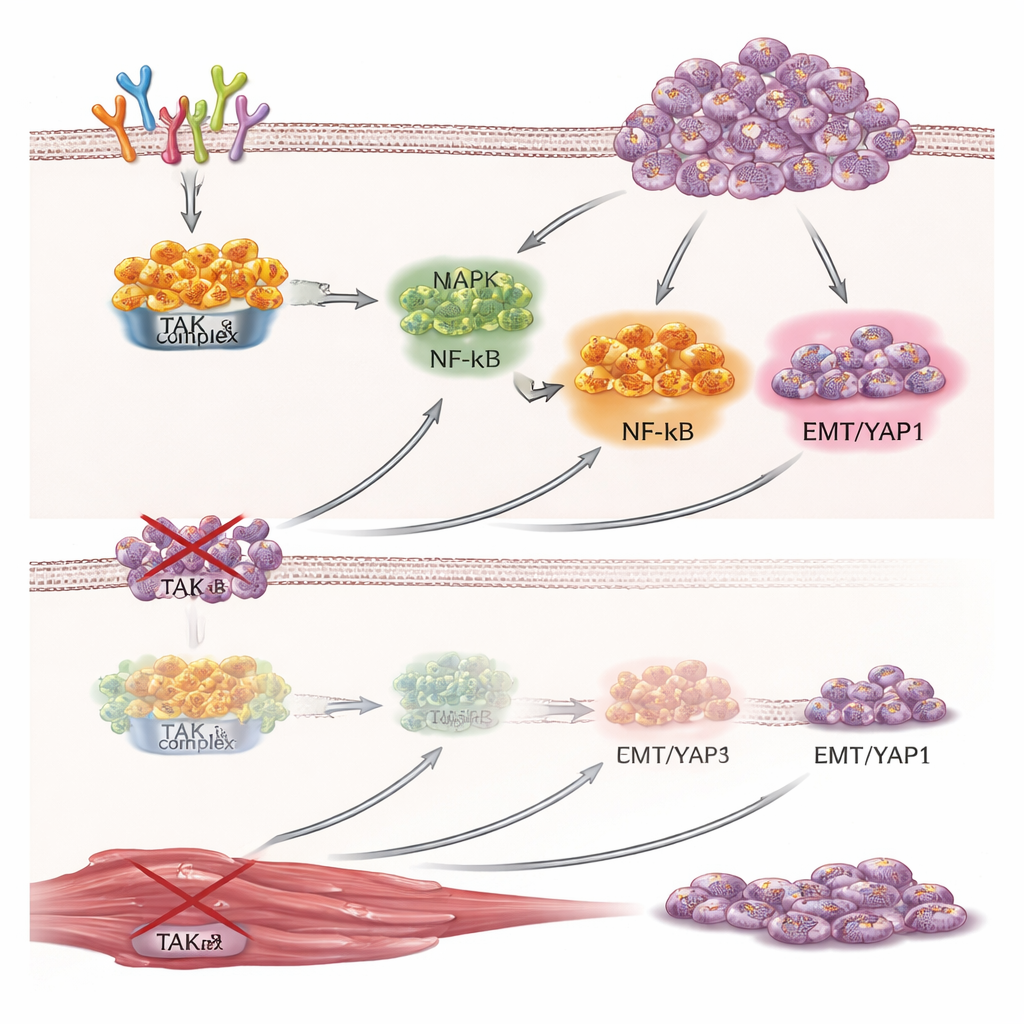
TAK1 im Test in lebenden Tumoren
Laborschalen erzählen nur einen Teil der Geschichte, also konstruierten die Forscher Rhabdomyosarkomzellen mit einem auf TAK1 zielenden Schalter, der bei Fütterung der Mäuse mit Doxycyclin abgeschaltet werden konnte. Als diese Zellen unter die Haut von Mäusen implantiert wurden, bildeten sich in beiden Gruppen Tumoren, doch wuchsen die Tumoren in den doxycyclinbehandelten Tieren deutlich langsamer und wogen am Ende der Studie weniger. Mikroskopische Untersuchungen zeigten weniger teilende Zellen und mehr multinukleäre, muskelähnliche Zellen in den TAK1‑stummgeschalteten Tumoren. Die Proteinanalyse spiegelte die Befunde aus der Zellkultur wider: TAK1‑Spiegel sanken, YAP1 nahm ab und der Muskel‑Differenzierungsmarker Myogenin stieg, was die Idee untermauert, dass TAK1 das Tumorwachstum stützt und gleichzeitig die angeborene Neigung der Zellen zur Reifung aktiv blockiert.
Was das für zukünftige Therapien bedeuten könnte
Insgesamt positioniert die Studie TAK1 als zentralen Koordinator krebsfördernder Signale im Rhabdomyosarkom und als wichtigen Vollstrecker der „Keine‑Reifung“‑Regel, die diese Zellen in einem schädlichen, stamzellähnlichen Zustand hält. Durch die Herunterregulierung von TAK1 schwächten die Forscher gleichzeitig mehrere Wachstumswege, reduzierten invasives Verhalten und ermöglichten den Zellen, sowohl in Kultur als auch in Mausmodellen in Richtung normaler Muskel‑Differenzierung voranzuschreiten. Für Patienten eröffnet dies die Möglichkeit von Therapien, die mehr tun als nur schnell teilende Zellen abzutöten: Medikamente, die TAK1 gezielt hemmen, könnten Tumorzellen dazu bringen, den Zellzyklus zu verlassen und weniger malign zu werden. Die Arbeit ist noch präklinisch, und Fragen wie Wirkstoffverteilung, Sicherheit und Resistenz müssen geklärt werden, doch TAK1 hebt sich nun als vielversprechendes therapeutisches Ziel in diesem herausfordernden Kinderkrebs hervor.
Zitation: Vuong, A.T., Joshi, A.S., Roy, A. et al. TAK1 is a key regulator of oncogenic signaling and differentiation blockade in rhabdomyosarcoma. Oncogene 45, 1714–1728 (2026). https://doi.org/10.1038/s41388-026-03767-z
Schlüsselwörter: Rhabdomyosarkom, TAK1‑Kinasen, Kinderkrebs, Muskel‑Differenzierung, YAP1‑Signalübertragung