Clear Sky Science · it
TAK1 è un regolatore chiave della segnalazione oncogenica e del blocco della differenziazione nel rabdomiosarcoma
Perché questo studio sul cancro infantile è importante
Il rabdomiosarcoma è un tumore infantile aggressivo che, al microscopio, somiglia molto a muscolo scheletrico immaturo. Queste cellule tumorali possiedono gli strumenti genetici necessari per diventare muscolo normale, ma si rifiutano ostinatamente di maturare. Invece continuano a dividersi e a diffondersi. Questo studio mette in luce un interruttore molecolare centrale, una proteina chiamata TAK1, che contribuisce a mantenere queste cellule tumorali in uno stato di crescita pericolosa e senza fine. Disattivando TAK1, i ricercatori sono riusciti a rallentare la crescita tumorale e a spingere le cellule verso uno stato più simile al muscolo normale.
Il problema: cellule muscolari congelate nei bambini
Il rabdomiosarcoma rappresenta circa la metà di tutti i sarcomi dei tessuti molli pediatrici e una frazione significativa dei tumori infantili in generale. Si presenta in due forme principali, embrionale e alveolare, guidate da alterazioni genetiche diverse. Nonostante queste differenze, entrambe condividono una caratteristica chiave: le loro cellule somigliano a precursori muscolari bloccati in uno stato precoce. Esprimono regolatori della costruzione muscolare ma non completano la trasformazione in fibre muscolari mature. Allo stesso tempo, sfruttano molteplici vie di crescita e sopravvivenza, rendendole difficili da trattare con un singolo farmaco mirato. Clinici e scienziati hanno a lungo sospettato l’esistenza di punti di controllo a monte che coordinano questi segnali di crescita e bloccano la differenziazione, ma questi interruttori principali sono stati difficili da individuare.
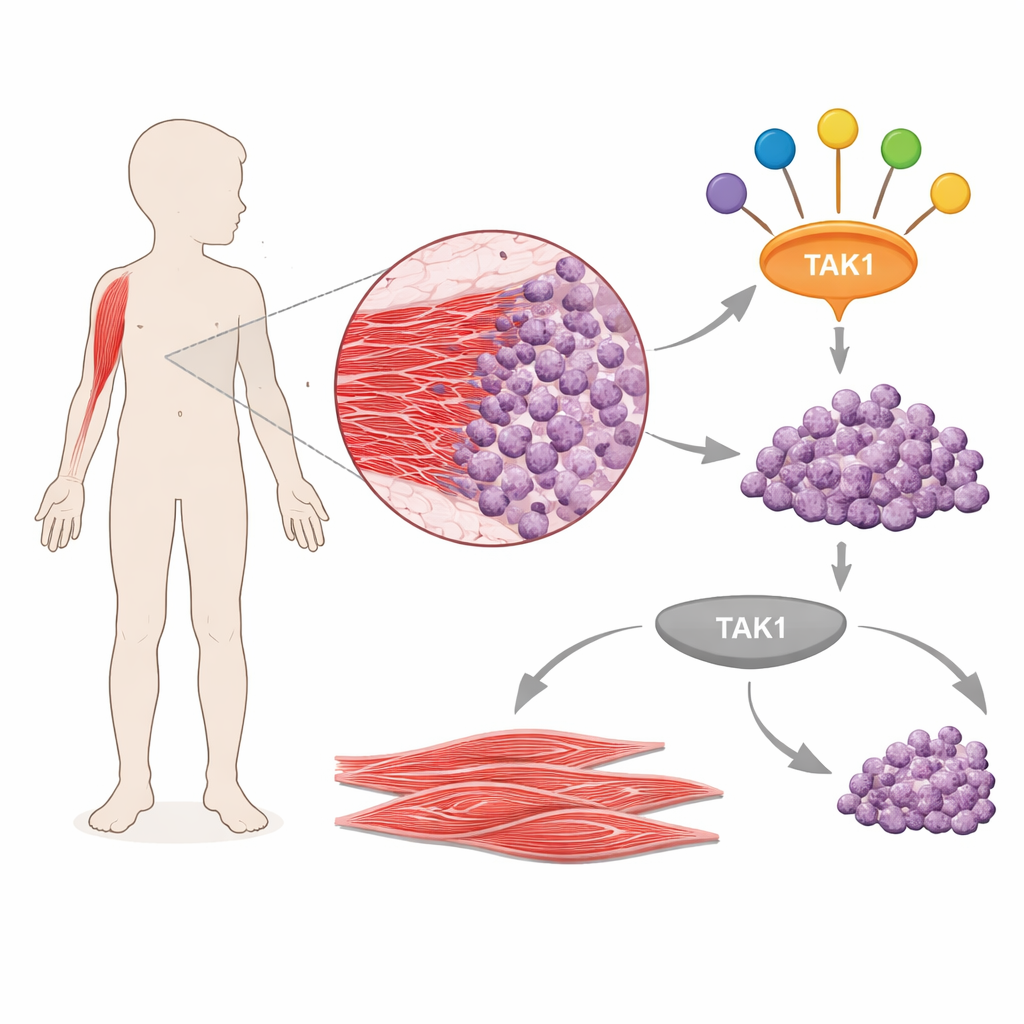
Un interruttore maestro per i segnali tumorali
Il gruppo si è concentrato su TAK1, una proteina di segnalazione nota per trasmettere messaggi da fattori di crescita e molecole infiammatorie verso diverse vie principali all’interno della cellula. Analizzando dati di espressione genica pubblici provenienti da tumori di pazienti, hanno scoperto che TAK1 e diversi dei suoi partner proteici sono costantemente elevati nel rabdomiosarcoma rispetto al muscolo normale. Hanno confermato questi risultati in più linee cellulari derivate da tumori umani, dove sia la quantità di TAK1 sia la sua forma attiva, fosforilata, risultavano superiori rispetto alle cellule muscolari umane normali. Ciò suggerisce che TAK1 non è solo presente ma è attivato in questi tumori, potenzialmente agendo come un hub che collega diverse vie che promuovono il cancro all’interno della cellula.
Spegnere TAK1 rallenta crescita e diffusione
Per testare il ruolo di TAK1, i ricercatori hanno usato due strategie per ridurne l’attività in cellule di rabdomiosarcoma coltivate in laboratorio: il knockdown genetico (utilizzando RNA a forcina corta o piccole molecole di RNA interferente) e un inibitore di piccola molecola chiamato 5Z‑7‑oxozeaenol. Entrambi gli approcci hanno ridotto drasticamente la velocità di divisione delle cellule tumorali, misurata mediante sintesi del DNA, attività metabolica e capacità di formare colonie nel tempo. Le cellule sono risultate anche meno abili a migrare attraverso pori e ad invadere un gel che imita il tessuto, indicando che TAK1 favorisce comportamenti associati alla metastasi. Sequenziamento RNA su larga scala e analisi di array proteici hanno mostrato che quando TAK1 veniva silenziato, molti geni e proteine legati al ciclo cellulare, alla segnalazione dei fattori di crescita e alla transizione epitelio‑mesenchimale venivano soppressi, mentre venivano attivati programmi coinvolti nella costruzione della struttura muscolare e nella differenziazione.
Rilasciare il freno sulla differenziazione muscolare
Uno degli effetti più sorprendenti del blocco di TAK1 è stato un’impennata nei marcatori della maturazione muscolare. In diverse linee cellulari di rabdomiosarcoma, la riduzione di TAK1 ha portato a molte più cellule che esprimevano catena pesante della miosina e miosina‑g, proteine caratteristiche delle fasi tardive della differenziazione muscolare. Un reporter sensibile a un importante promotore specifico per il muscolo è diventato anch’esso più attivo, indicando che la macchina sottostante dell’espressione genica si stava spostando verso un programma muscolare. Ulteriori lavori meccanicistici hanno ricondotto parte di questo effetto alla via Hippo–YAP1, un noto regolatore delle dimensioni degli organi e del cancro. Il knockdown di TAK1 ha ridotto i livelli della proteina YAP1. Quando gli scienziati hanno reintrodotto una forma di YAP1 resistente alla degradazione, hanno sostanzialmente annullato l’aumento della differenziazione muscolare dovuto alla perdita di TAK1, suggerendo che TAK1 normalmente aiuta a stabilizzare YAP1 e, tramite quest’ultima, mantiene le cellule tumorali in uno stato indifferenziato e proliferativo.
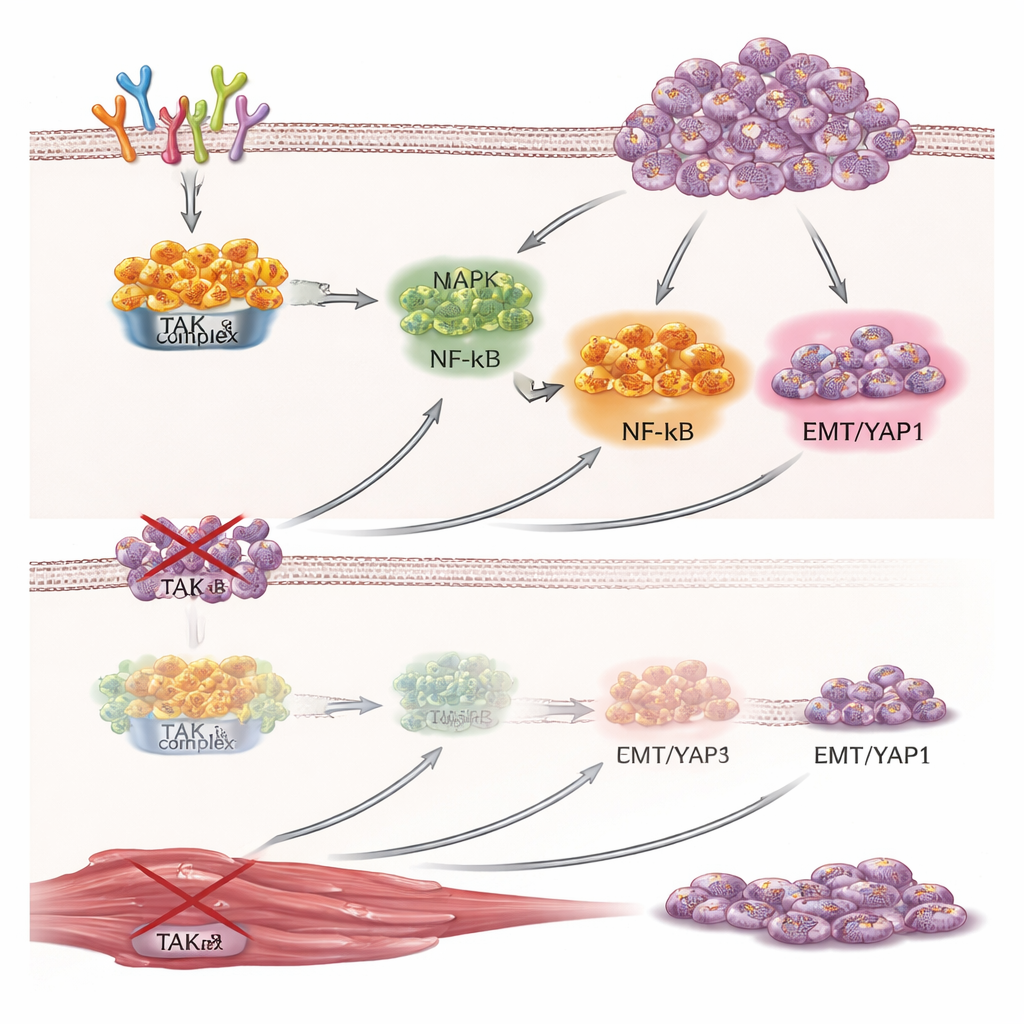
Testare TAK1 nei tumori viventi
I piatti di laboratorio possono raccontare solo una parte della storia, così il gruppo ha ingegnerizzato cellule di rabdomiosarcoma con un interruttore che mirava a TAK1 e che poteva essere spento somministrando doxiciclina ai topi. Quando queste cellule sono state impiantate sotto la pelle dei roditori, si sono formati tumori in entrambi i gruppi, ma quelli negli animali trattati con doxiciclina sono cresciuti molto più lentamente e avevano un peso inferiore alla fine dello studio. L’esame microscopico ha rivelato meno cellule in divisione e più cellule multinucleate, simili a muscolo, nei tumori con TAK1 silenziato. L’analisi proteica ha rispecchiato i risultati in coltura cellulare: i livelli di TAK1 sono diminuiti, YAP1 è calato e il marcatore di differenziazione muscolare miosina‑g è aumentato, rafforzando l’idea che TAK1 sostiene la crescita tumorale mentre blocca attivamente la tendenza intrinseca delle cellule a maturare.
Cosa potrebbe significare per i trattamenti futuri
Complessivamente, lo studio colloca TAK1 come un coordinatore centrale dei segnali che promuovono il cancro nel rabdomiosarcoma e come un importante custode della regola del “nessuna maturazione” che mantiene queste cellule in uno stato dannoso simile a cellule staminali. Riducendo l’attività di TAK1, i ricercatori hanno indebolito simultaneamente diverse vie di crescita, ridotto i comportamenti invasivi e permesso alle cellule di progredire verso la differenziazione muscolare normale, sia in coltura che in tumori murini. Per i pazienti, questo apre la possibilità di terapie che fanno più che uccidere le cellule che si dividono rapidamente: farmaci mirati a TAK1 potrebbero anche indurre le cellule tumorali a uscire dal ciclo cellulare e diventare meno maligne. Il lavoro è ancora preclinico, e questioni come la somministrazione del farmaco, la sicurezza e la resistenza devono essere affrontate, ma TAK1 emerge ora come un promettente target terapeutico per questo complesso tumore infantile.
Citazione: Vuong, A.T., Joshi, A.S., Roy, A. et al. TAK1 is a key regulator of oncogenic signaling and differentiation blockade in rhabdomyosarcoma. Oncogene 45, 1714–1728 (2026). https://doi.org/10.1038/s41388-026-03767-z
Parole chiave: rabdomiosarcoma, chinasi TAK1, cancro infantile, differenziazione muscolare, segnalazione YAP1