Clear Sky Science · nl
Detectie van veranderingen in chromatineconditie in PBMC's die geassocieerd zijn met Type 2-diabetes mellitus
Een nieuw venster op diabetes via bloedcellen
Type 2-diabetes wordt doorgaans gevolgd met bloedsuikerwaarden en langetermijnmaatstaven zoals HbA1c. Deze tests zeggen echter weinig over hoe iemands immuunsysteem met de ziekte omgaat, terwijl laaggradige ontsteking en immuunstress centraal staan bij veel complicaties. Deze studie onderzoekt een ander soort diabetescontrole: met geavanceerde microscopie en computeranalyse kijken naar hoe DNA is verpakt in immuuncellen, met als doel een eenvoudige, schaalbare test te ontwikkelen die vroege veranderingen kan signaleren wanneer mensen van gezond via prediabetes naar diabetes gaan.
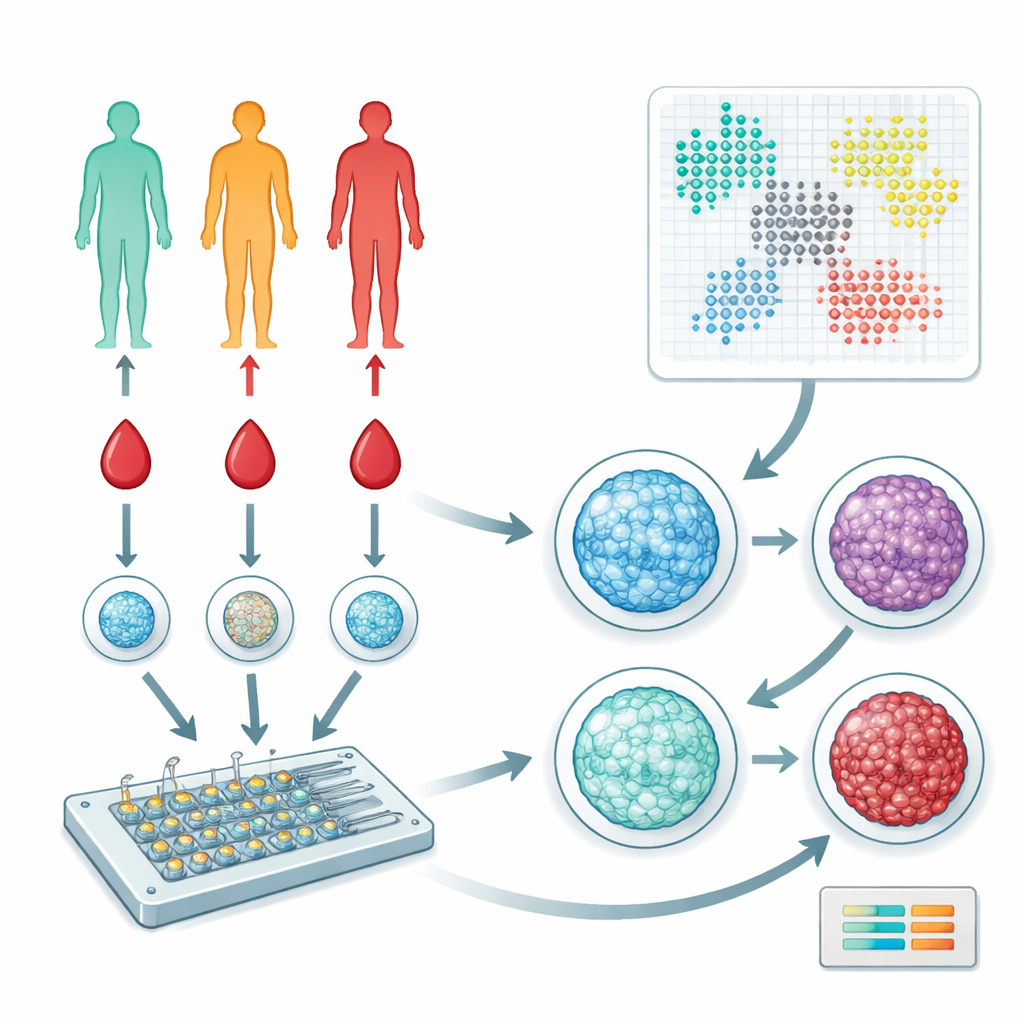
Bloedcellen op een nieuwe manier bekijken
De onderzoekers concentreerden zich op perifere mononucleaire bloedcellen (PBMC's), een gemengde groep immuuncellen die in ons bloed circuleren en helpen bij het coördineren van reacties door het hele lichaam. Ze verzamelden bloed van 57 personen verspreid over gezonde, prediabetische en type 2-diabetische stadia. In plaats van genen te sequencen of tientallen eiwitten te meten, gebruikte het team een microfluïdisch apparaat en fluorescente kleurstoffen om te beelden hoe DNA in de celkern is gerangschikt. Dit DNA–eiwitcomplex, chromatine genoemd, kan meer open of meer gecondenseerd zijn, en de organisatie ervan weerspiegelt subtiel hoe een cel functioneert en welke signalen hij heeft ontvangen.
Afbeeldingen omzetten in patronen
Om orde te scheppen in tienduizenden kernbeelden gebruikte het team een type kunstmatige intelligentie dat een variational autoencoder wordt genoemd. Deze software comprimeert elk beeld tot een set numerieke kenmerken die kernmaat, -vorm en de fijnmazige textuur van chromatine vastleggen. Vervolgens pasten ze grafgebaseerde clusteringmethoden toe om kernen te groeperen in onderscheidende "toestanden" die overeenkomen met verschillende immuuncelsubpopulaties of activatieniveaus. Parallelle analyses met zorgvuldig ontworpen vorm- en textuurmetingen (handgemaakte features) leverden een onafhankelijke check op de op AI gebaseerde resultaten, en beide benaderingen convergeerden op een reeks chromatinepatronen die bij meerdere individuen terugkeren.
Distincte celtoestanden volgen het ziektestadium
Wanneer de auteurs deze op chromatine gebaseerde clusters vergeleken tussen gezond, prediabetes en diabetes, traden duidelijke verschuivingen op. Bepaalde kerntoestanden waren verrijkt bij gezonde individuen, andere bij mensen met prediabetes en weer andere bij mensen met diabetes. Kenmerken die beschreven waar dichte chromatine-ophopingen zich binnen de kern bevonden — dicht bij de rand of naar binnen verschoven, dicht gegroepeerd of meer gespreid — bleken bijzonder informatief. Alleen met het aandeel van iemands cellen dat in elk cluster viel, kon een standaard machine-learningmodel diabetici onderscheiden van gezonde donoren en, met nog hogere nauwkeurigheid, diabetici van prediabetische donoren. Deze voorspellingen hielden stand in tests op achtergehouden en onafhankelijk opgesplitste subsets van de cohorte, wat suggereert dat chromatineorganisatie robuuste informatie over ziekteprogressie bevat op het niveau van individuele patiënten.
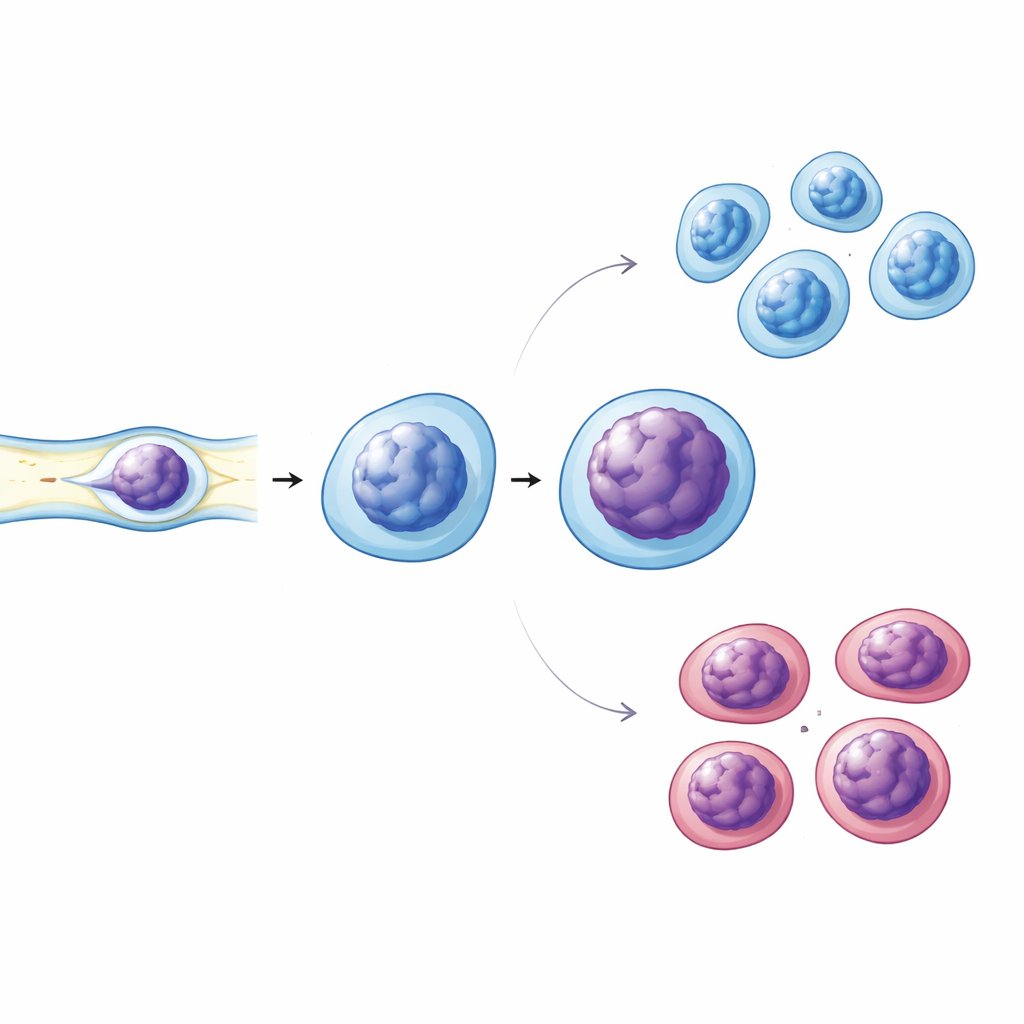
Mechanische stress onthult subtiele kwetsbaarheden
Immuuncellen worden voortdurend samengedrukt wanneer ze door nauwe ruimtes in bloedvaten en weefsels bewegen, dus vroeg het team zich ook af of hun mechanisch gedrag verandert bij diabetes. Ze gebruikten smalle microkanalen om levende immuuncellen zachtjes samen te drukken terwijl ze hun kernen beeldden. Diabetische cellen toonden sterker uitgesproken kernvervormingen en aanwijzingen voor veranderde chromatinecondensatie vergeleken met cellen van gezonde en prediabetische donoren. Vervolgkleuringsexperimenten lieten zien dat diabetische kernen minder van een belangrijk structureel eiwit, Lamin A/C, hadden, dat bijdraagt aan de stijfheid en vorm van de kern, en dat ze iets hogere niveaus van dichtgepakt chromatinemerkten vertoonden. Het aandeel cellen met een activatiemarker op het oppervlak was ook hoger bij diabetes, waarmee deze kernveranderingen werden gekoppeld aan verhoogde immuunactivatie.
Van laboratoriuminzicht naar toekomstig klinisch instrument
Gezamenlijk tonen de resultaten aan dat eenvoudige fluorescente beeldvorming van chromatine in routinematige bloedmonsters betekenisvolle, patiëntspecifieke veranderingen in het immuunsysteem kan vastleggen naarmate type 2-diabetes vordert. Hoewel deze benadering nog geen vervanging is voor standaard glucose- of HbA1c-tests, biedt ze een aanvullende maat voor immuunstress en celfunctie — informatie die de huidige klinische markers grotendeels missen. Omdat de assay steunt op relatief goedkope kleurstoffen en microfluïdische apparaten, betogen de auteurs dat deze uiteindelijk opgeschaald en geautomatiseerd kan worden voor klinisch gebruik, waardoor meer gepersonaliseerde monitoring van diabetes en diens complicaties mogelijk wordt.
Bronvermelding: Afarani, M.M., Gupta, R., Uhler, C. et al. Detecting chromatin state alterations in PBMCs associated with Type 2 Diabetes Mellitus. Commun Med 6, 268 (2026). https://doi.org/10.1038/s43856-026-01513-w
Trefwoorden: type 2 diabetes, immuuncellen, chromatine-imaging, biomarkers, machine learning