Clear Sky Science · de
Erkennung von Veränderungen des Chromatinzustands in PBMCs im Zusammenhang mit Typ-2-Diabetes
Ein neues Fenster auf Diabetes durch Blutzellen
Typ-2-Diabetes wird üblicherweise anhand von Blutzuckerwerten und Langzeitmessgrößen wie HbA1c überwacht. Diese Tests geben jedoch wenig Aufschluss darüber, wie das Immunsystem mit der Erkrankung zurechtkommt, obwohl niedriggradige Entzündung und Immunstress zentral für viele Komplikationen sind. Diese Studie untersucht eine andere Art von Diabetes-Check: Mit fortgeschrittener Mikroskopie und Computeranalyse wird untersucht, wie DNA in Immunzellen verpackt ist, mit dem Ziel, einen einfachen, skalierbaren Test zu entwickeln, der frühe Veränderungen erkennt, wenn Menschen von gesund zu Prädiabetes und weiter zu Diabetes übergehen.
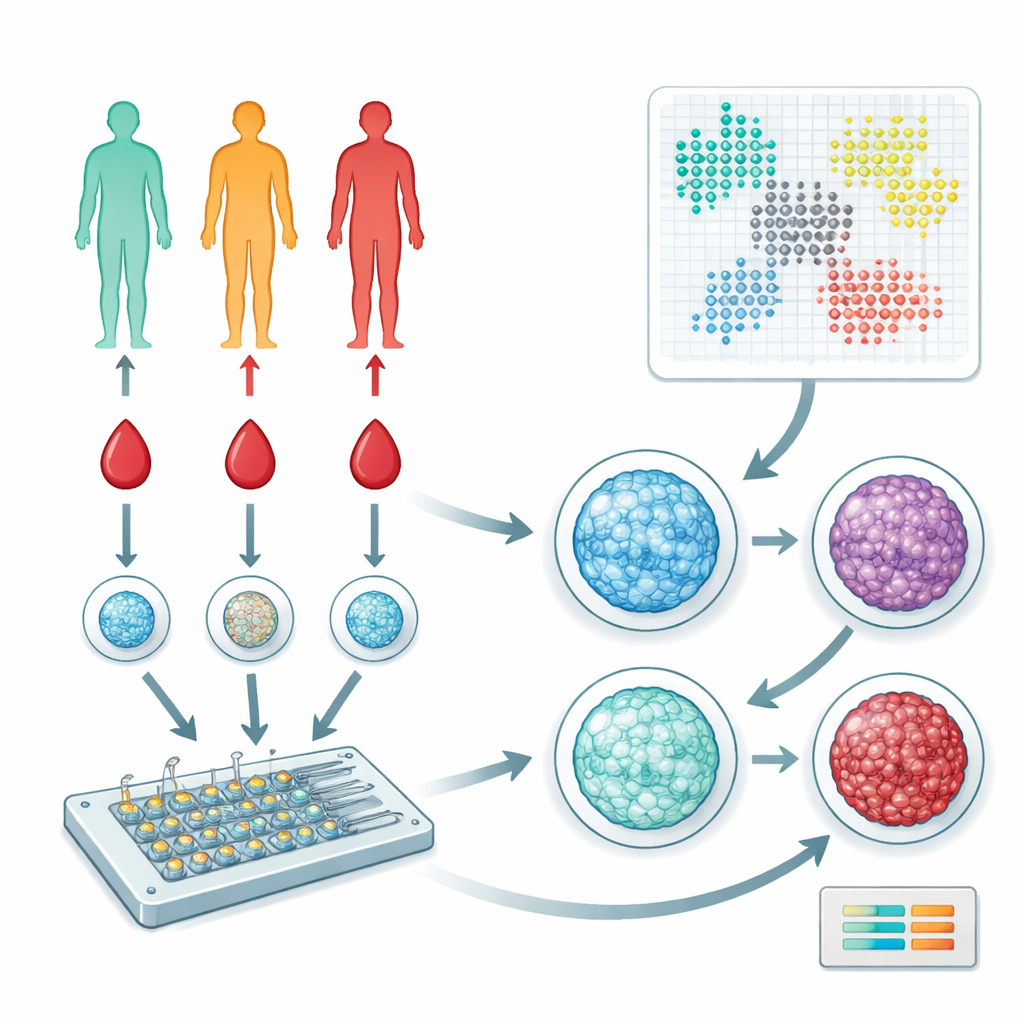
Blutzellen auf neue Weise betrachten
Die Forschenden konzentrierten sich auf periphere mononukleäre Blutzellen (PBMCs), eine gemischte Gruppe von Immunzellen, die im Blut zirkulieren und die Reaktionen im ganzen Körper koordinieren. Sie gewannen Blutproben von 57 Personen aus den Bereichen gesund, prädiabetisch und Typ-2-diabetisch. Anstatt Gene zu sequenzieren oder Dutzende Proteine zu messen, nutzte das Team ein mikrofluidisches Gerät und fluoreszierende Farbstoffe, um zu bildlich darzustellen, wie DNA im Zellkern angeordnet ist. Dieses DNA–Protein-Komplex, das Chromatin genannt wird, kann offener oder dichter gepackt sein, und seine Organisation spiegelt subtil wider, wie eine Zelle funktioniert und welche Signale sie empfangen hat.
Bilder in Muster übersetzen
Um Zehntausende von Kernbildern zu analysieren, verwendete das Team eine Form der künstlichen Intelligenz, einen variationalen Autoencoder. Diese Software komprimiert jedes Bild in eine Reihe numerischer Merkmale, die Kerngröße, -form und die feine Textur des Chromatins erfassen. Anschließend wendeten sie graphbasierte Clustering-Methoden an, um Kerne in unterschiedliche „Zustände“ zu gruppieren, die verschiedenen Immunzellsubpopulationen oder Aktivierungsniveaus entsprechen. Parallele Analysen mit sorgfältig konzipierten Form- und Texturmaßen (manuell entwickelte Merkmale) lieferten eine unabhängige Kontrolle der KI-basierten Ergebnisse, und beide Ansätze konvergierten auf einen Satz von Chromatinmustern, die sich über Individuen hinweg wiederholen.
Unterschiedliche Zellzustände korrelieren mit Krankheitsstadium
Beim Vergleich dieser chromatinbasierten Cluster zwischen gesund, Prädiabetes und Diabetes traten klare Verschiebungen zutage. Bestimmte Kernzustände waren bei gesunden Personen angereichert, andere bei prädiabetischen und wiederum andere bei diabetischen Personen. Merkmale, die beschrieben, wo sich dichte Chromatinbereiche im Kern befinden – nahe dem Rand oder nach innen verschoben, eng zusammenliegend oder stärker getrennt – waren besonders aufschlussreich. Allein mit dem Anteil der Zellen einer Person in jedem Cluster konnte ein gängiges maschinelles Lernmodell zwischen diabetischen und gesunden Spendern unterscheiden und mit noch höherer Genauigkeit diabetische von prädiabetischen Personen trennen. Diese Vorhersagen hielten in Tests mit zurückbehaltenen und unabhängig gesplitteten Teilmengen der Kohorte Stand, was darauf hindeutet, dass die Chromatinorganisation robuste Informationen über den Krankheitsverlauf auf Ebene einzelner Patienten trägt.
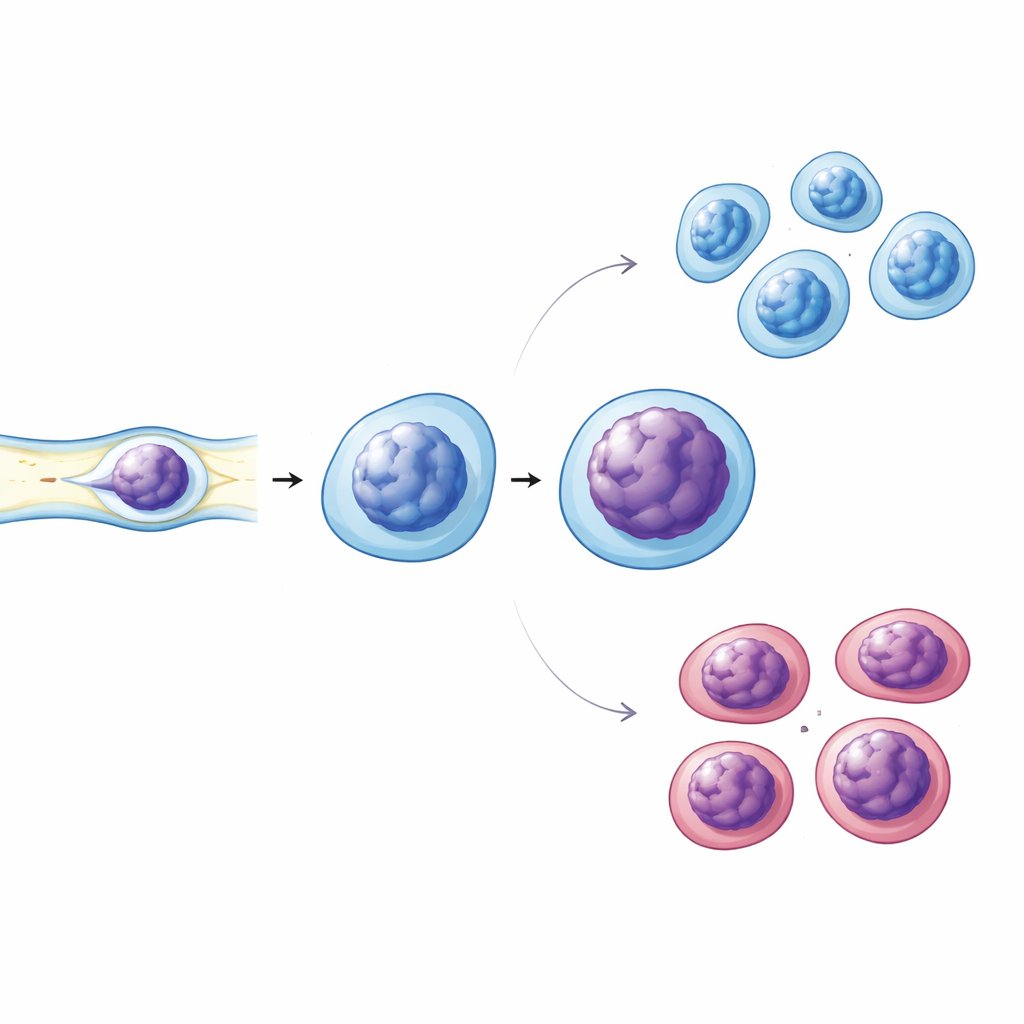
Mechanischer Stress enthüllt subtile Schwächen
Immunzellen quetschen sich ständig durch enge Passagen in Blutgefäßen und Geweben, daher prüfte das Team auch, ob sich ihr mechanisches Verhalten bei Diabetes ändert. Sie verwendeten enge Mikrokanäle, um lebende Immunzellen sanft zu komprimieren, während sie deren Kerne bildlich erfassten. Diabetische Zellen zeigten ausgeprägtere Kernverformungen und Anzeichen veränderter Chromatindichte im Vergleich zu Zellen von gesunden und prädiabetischen Spendern. Nachfolgende Färbeexperimente zeigten, dass diabetische Kerne weniger eines wichtigen Strukturproteins, Lamin A/C, aufwiesen, das zur Aufrechterhaltung der Kernsteifigkeit und -form beiträgt, und sie zeigten leicht erhöhte Mengen an Markern für eng gepacktes Chromatin. Der Anteil der Zellen mit einem Aktivierungsmarker an der Oberfläche war in Diabetes ebenfalls höher, was diese Kernveränderungen mit erhöhter Immunaktivierung verknüpft.
Vom Laborbefund zum zukünftigen klinischen Werkzeug
Insgesamt zeigt die Arbeit, dass einfache fluoreszenzbasierte Bildgebung des Chromatins in Routinematerial aus Blut aussagekräftige, patientenspezifische Veränderungen des Immunsystems abbilden kann, während sich Typ-2-Diabetes entwickelt. Zwar ersetzt dieser Ansatz noch nicht Standardtests für Glukose oder HbA1c, bietet aber eine komplementäre Messgröße für Immunstress und Zellfunktion – Informationen, die heutige klinische Marker weitgehend übersehen. Da der Test auf vergleichsweise kostengünstigen Farbstoffen und mikrofluidischen Geräten basiert, argumentieren die Autorinnen und Autoren, dass er sich schließlich für den klinischen Einsatz skalieren und automatisieren ließe, um eine individuellere Überwachung von Diabetes und dessen Komplikationen zu ermöglichen.
Zitation: Afarani, M.M., Gupta, R., Uhler, C. et al. Detecting chromatin state alterations in PBMCs associated with Type 2 Diabetes Mellitus. Commun Med 6, 268 (2026). https://doi.org/10.1038/s43856-026-01513-w
Schlüsselwörter: Typ-2-Diabetes, Immunzellen, Chromatinbildgebung, Biomarker, maschinelles Lernen