Clear Sky Science · es
Detección de alteraciones del estado de la cromatina en PBMC asociadas con la diabetes mellitus tipo 2
Una nueva ventana a la diabetes a través de las células sanguíneas
La diabetes tipo 2 suele monitorizarse con cifras de glucemia y medidas a largo plazo como la HbA1c. Pero estas pruebas aportan poca información sobre cómo está respondiendo el sistema inmunitario a la enfermedad, pese a que la inflamación crónica de bajo grado y el estrés inmunitario son fundamentales en muchas complicaciones. Este estudio explora otro tipo de chequeo de la diabetes: usar microscopía avanzada y análisis computacional para observar cómo se empaña el ADN dentro de las células inmunitarias, con el objetivo de crear una prueba sencilla y escalable que pueda señalar cambios precoces a medida que las personas pasan de la salud a la prediabetes y a la diabetes.
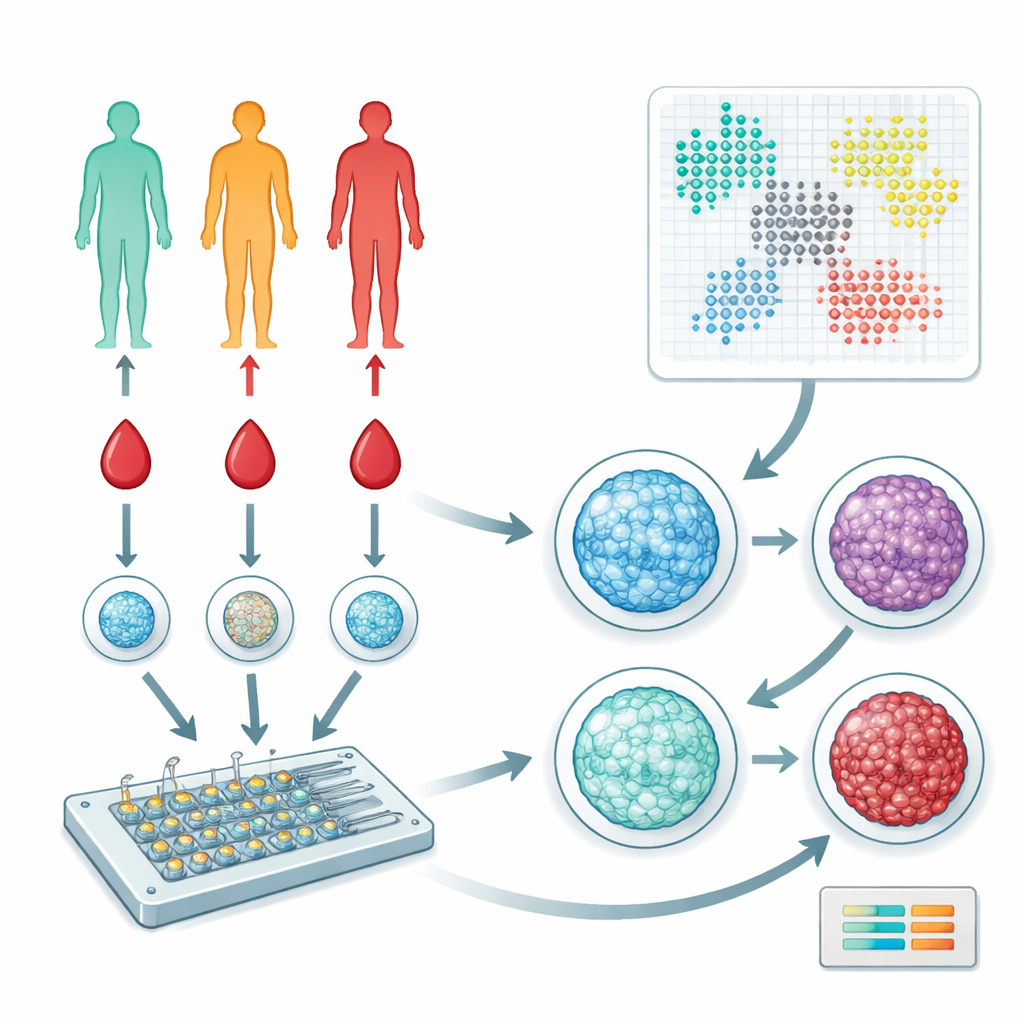
Mirar las células sanguíneas de un modo nuevo
Los investigadores se centraron en las células mononucleares periféricas de la sangre (PBMC), un grupo mixto de células inmunitarias que circulan en la sangre y ayudan a coordinar respuestas en todo el organismo. Recolectaron sangre de 57 personas que abarcaban los estadios de sanos, prediabéticos y con diabetes tipo 2. En lugar de secuenciar genes o medir docenas de proteínas, el equipo empleó un dispositivo microfluídico y tintes fluorescentes para captar imágenes de cómo se dispone el ADN dentro del núcleo celular. Este complejo ADN–proteína, llamado cromatina, puede estar más abierto o más condensado, y su organización refleja sutilmente cómo funciona una célula y qué señales ha recibido.
Convertir imágenes en patrones
Para interpretar decenas de miles de imágenes nucleares, el equipo usó un tipo de inteligencia artificial llamada autocodificador variacional. Este software comprime cada imagen en un conjunto de características numéricas que capturan el tamaño y la forma del núcleo y la textura fina de la cromatina. Luego aplicaron métodos de agrupamiento basados en grafos para agrupar núcleos en “estados” distintos que corresponden a diferentes subpoblaciones de células inmunitarias o niveles de activación. Análisis paralelos con medidas de forma y textura diseñadas a mano (características manuales) ofrecieron una comprobación independiente de los resultados basados en IA, y ambos enfoques convergieron en un conjunto de patrones de cromatina recurrentes entre individuos.
Estados celulares distintos siguen la etapa de la enfermedad
Cuando los autores compararon estos clústeres basados en cromatina entre sanos, prediabéticos y diabéticos, surgieron cambios claros. Ciertos estados nucleares estaban enriquecidos en individuos sanos, otros en personas con prediabetes y otros en las personas con diabetes. Las características que describían dónde se ubicaban los bolsillos de cromatina densa dentro del núcleo —cerca del borde o desplazados hacia el interior, agrupados de forma compacta o más separados— resultaron especialmente informativas. Usando solo la fracción de células de cada persona que caían en cada clúster, un modelo estándar de aprendizaje automático pudo distinguir donantes diabéticos de sanos y, con aún mayor precisión, diabéticos de prediabéticos. Estas predicciones se mantuvieron en pruebas sobre subconjuntos reservados e independientes de la cohorte, lo que sugiere que la organización de la cromatina aporta información robusta sobre la progresión de la enfermedad a nivel de pacientes individuales.
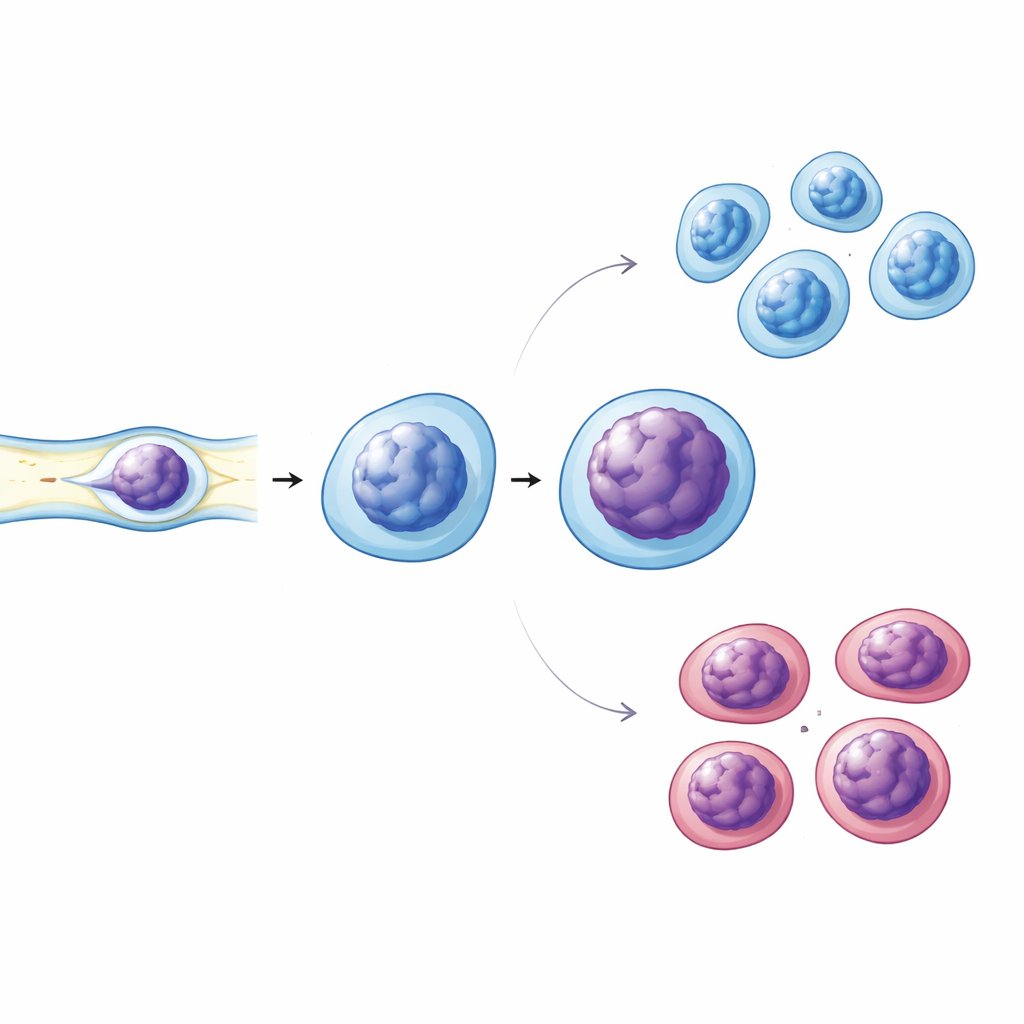
El estrés mecánico revela debilidades sutiles
Las células inmunitarias se comprimen continuamente al atravesar espacios estrechos en vasos sanguíneos y tejidos, por lo que el equipo también investigó si su comportamiento mecánico cambia en la diabetes. Usaron microcanales estrechos para comprimir suavemente células inmunitarias vivas mientras imaginaban sus núcleos. Las células diabéticas mostraron deformaciones nucleares más pronunciadas y signos de alteración en la condensación de la cromatina en comparación con células de donantes sanos y prediabéticos. Experimentos de tinción posteriores revelaron que los núcleos diabéticos contenían menos de una proteína estructural clave, Lamin A/C, que ayuda a mantener la rigidez y la forma nuclear, y mostraban niveles ligeramente más altos de marcas de cromatina muy compacta. La fracción de células que presentaban un marcador de activación en su superficie también fue mayor en la diabetes, vinculando estos cambios nucleares con una mayor activación inmunitaria.
De la visión de laboratorio a una herramienta clínica futura
En conjunto, el trabajo muestra que la imagen fluorescente sencilla de la cromatina en muestras de sangre rutinarias puede capturar cambios significativos y específicos por paciente en el sistema inmunitario a medida que progresa la diabetes tipo 2. Aunque este enfoque no sustituye todavía las pruebas estándar de glucosa o HbA1c, ofrece una lectura complementaria del estrés inmunitario y de la función celular, información que los marcadores clínicos actuales pierden en gran medida. Dado que el ensayo se basa en tintes y dispositivos microfluídicos de coste relativamente bajo, los autores sostienen que podría escalarse y automatizarse para uso clínico, permitiendo un seguimiento más personalizado de la diabetes y sus complicaciones.
Cita: Afarani, M.M., Gupta, R., Uhler, C. et al. Detecting chromatin state alterations in PBMCs associated with Type 2 Diabetes Mellitus. Commun Med 6, 268 (2026). https://doi.org/10.1038/s43856-026-01513-w
Palabras clave: diabetes tipo 2, células inmunitarias, imagen de la cromatina, biomarcadores, aprendizaje automático