Clear Sky Science · it
Rilevazione delle alterazioni dello stato della cromatina nei PBMC associate al diabete mellito di tipo 2
Una nuova finestra sul diabete attraverso le cellule del sangue
Il diabete di tipo 2 viene solitamente monitorato con i valori della glicemia e con misure a lungo termine come l’HbA1c. Tuttavia questi test dicono poco su come il sistema immunitario stia affrontando la malattia, nonostante l’infiammazione di basso grado e lo stress immunitario siano centrali in molte complicazioni. Questo studio esplora un diverso tipo di controllo del diabete: utilizzare microscopia avanzata e analisi computazionale per osservare come il DNA è confezionato all’interno delle cellule immunitarie, con l’obiettivo di creare un test semplice e scalabile che possa segnalare cambiamenti precoci mentre le persone passano dalla salute alla prediabete e al diabete.
Osservare le cellule del sangue in modo nuovo
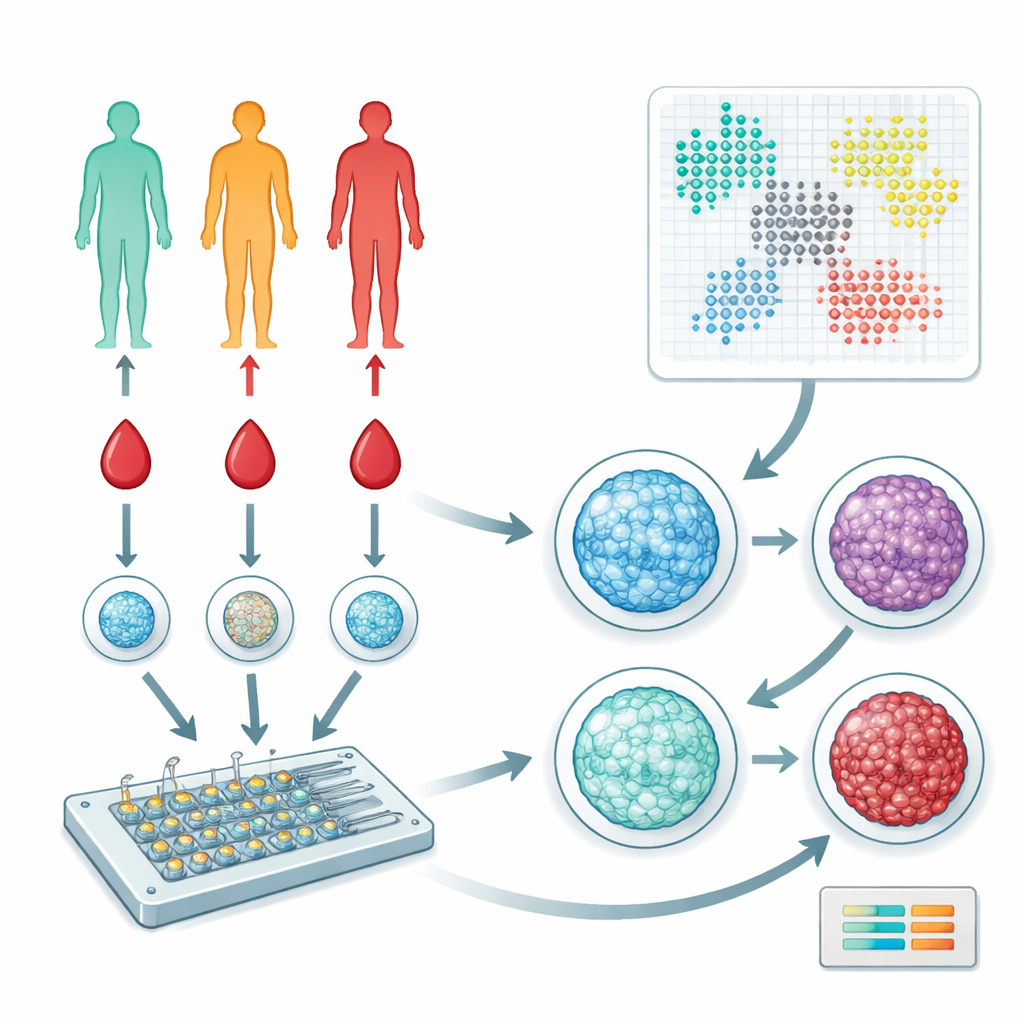
I ricercatori si sono concentrati sui monociti e sui linfociti mononucleati del sangue periferico (PBMC), un gruppo misto di cellule immunitarie che circolano nel sangue e aiutano a coordinare le risposte in tutto il corpo. Hanno raccolto campioni da 57 persone lungo lo spettro tra sani, prediabetici e soggetti con diabete di tipo 2. Invece di eseguire il sequenziamento genico o misurare dozzine di proteine, il gruppo ha utilizzato un dispositivo microfluidico e coloranti fluorescenti per acquisire immagini di come il DNA è organizzato all’interno del nucleo cellulare. Questo complesso DNA‑proteina, chiamato cromatina, può essere più aperto o più condensato, e la sua organizzazione riflette sottilmente il funzionamento della cellula e i segnali che ha ricevuto.
Trasformare le immagini in pattern
Per interpretare decine di migliaia di immagini nucleari, il team ha impiegato un tipo di intelligenza artificiale chiamata autoencoder variazionale. Questo software comprime ogni immagine in un insieme di caratteristiche numeriche che catturano dimensione nucleare, forma e la texture fine della cromatina. Hanno poi applicato metodi di clustering basati su grafi per raggruppare i nuclei in “stati” distinti che corrispondono a differenti sottopopolazioni di cellule immunitarie o livelli di attivazione. Analisi parallele con misure di forma e texture progettate a mano (caratteristiche artigianali) hanno fornito un controllo indipendente sui risultati basati sull’IA, e entrambi gli approcci hanno convergono su un insieme di pattern di cromatina ricorrenti tra gli individui.
Stati cellulari distinti seguono la fase della malattia
Quando gli autori hanno confrontato questi cluster basati sulla cromatina tra sani, prediabetici e diabetici, sono emersi spostamenti chiari. Alcuni stati nucleari risultavano arricchiti nei soggetti sani, altri nelle persone con prediabete e altri ancora in quelle con diabete. Le caratteristiche che descrivevano la posizione delle zone di cromatina densa all’interno del nucleo — vicino al bordo o più spostate verso l’interno, strettamente raggruppate o più separate — si sono rivelate particolarmente informative. Utilizzando solo la frazione di cellule di una persona che ricadeva in ciascun cluster, un modello standard di apprendimento automatico è stato in grado di distinguere i donatori diabetici da quelli sani e, con accuratezza ancora maggiore, i diabetici dai prediabetici. Queste predizioni si sono mantenute anche nei test su sottoinsiemi tenuti da parte e su divisioni indipendenti della coorte, suggerendo che l’organizzazione della cromatina porta informazioni robuste sul progredire della malattia a livello del singolo paziente.
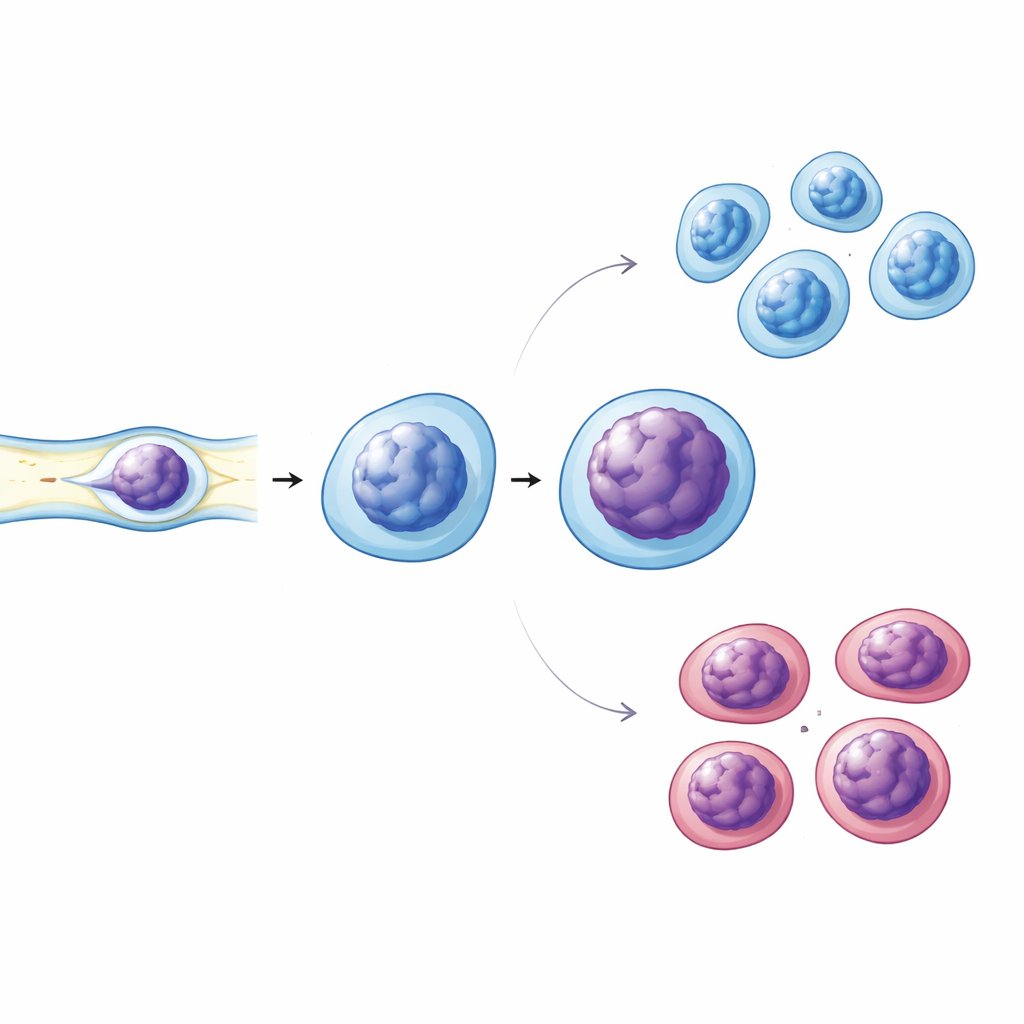
Lo stress meccanico rivela debolezze sottili
Le cellule immunitarie si comprimono costantemente per passare attraverso spazi stretti nei vasi e nei tessuti, quindi il team ha indagato anche se il loro comportamento meccanico cambi in presenza di diabete. Hanno impiegato microcanali stretti per comprimere delicatamente le cellule immunitarie vive mentre ne acquisivano le immagini nucleari. Le cellule diabetiche hanno mostrato una deformazione nucleare più pronunciata e segni di alterata condensazione della cromatina rispetto alle cellule provenienti da donatori sani e prediabetici. Esperimenti di colorazione successivi hanno rivelato che i nuclei dei diabetici avevano quantità ridotte di una proteina strutturale chiave, Lamin A/C, che contribuisce a mantenere rigidità e forma del nucleo, e presentavano leggermente livelli più alti di marcatori di cromatina fortemente impacchettata. Anche la frazione di cellule che esprimeva un marcatore di attivazione sulla superficie era maggiore nel diabete, collegando questi cambiamenti nucleari a una maggiore attivazione immunitaria.
Dal laboratorio a uno strumento clinico futuro
Nel complesso, il lavoro mostra che una semplice imaging fluorescente della cromatina in campioni di sangue di routine può catturare cambiamenti significativi e specifici per il paziente nel sistema immunitario man mano che il diabete di tipo 2 progredisce. Pur non sostituendo ancora i test standard della glicemia o dell’HbA1c, questo approccio offre una lettura complementare dello stress immunitario e della funzione cellulare — informazioni che i marcatori clinici attuali in gran parte non rilevano. Poiché il saggio si basa su coloranti e dispositivi microfluidici relativamente a basso costo, gli autori sostengono che potrebbe in futuro essere scalato e automatizzato per l’uso clinico, permettendo un monitoraggio più personalizzato del diabete e delle sue complicazioni.
Citazione: Afarani, M.M., Gupta, R., Uhler, C. et al. Detecting chromatin state alterations in PBMCs associated with Type 2 Diabetes Mellitus. Commun Med 6, 268 (2026). https://doi.org/10.1038/s43856-026-01513-w
Parole chiave: diabete di tipo 2, cellule immunitarie, imaging della cromatina, biomarcatori, apprendimento automatico