Clear Sky Science · fr
Détecter les altérations de l’état de la chromatine dans les PBMC associées au diabète de type 2
Une nouvelle fenêtre sur le diabète via les cellules sanguines
Le diabète de type 2 est généralement suivi par des mesures de la glycémie et des indicateurs à long terme comme l’HbA1c. Mais ces tests disent peu de choses sur la façon dont le système immunitaire d’une personne supporte la maladie, alors que l’inflammation de bas grade et le stress immunitaire sont au cœur de nombreuses complications. Cette étude explore un autre type de bilan du diabète : utiliser une microscopie avancée et une analyse informatique pour observer la façon dont l’ADN est empaqueté à l’intérieur des cellules immunitaires, dans l’objectif de créer un test simple et extensible capable de signaler les changements précoces lorsque les personnes passent de la santé au prédiabète puis au diabète.
Regarder les cellules sanguines autrement
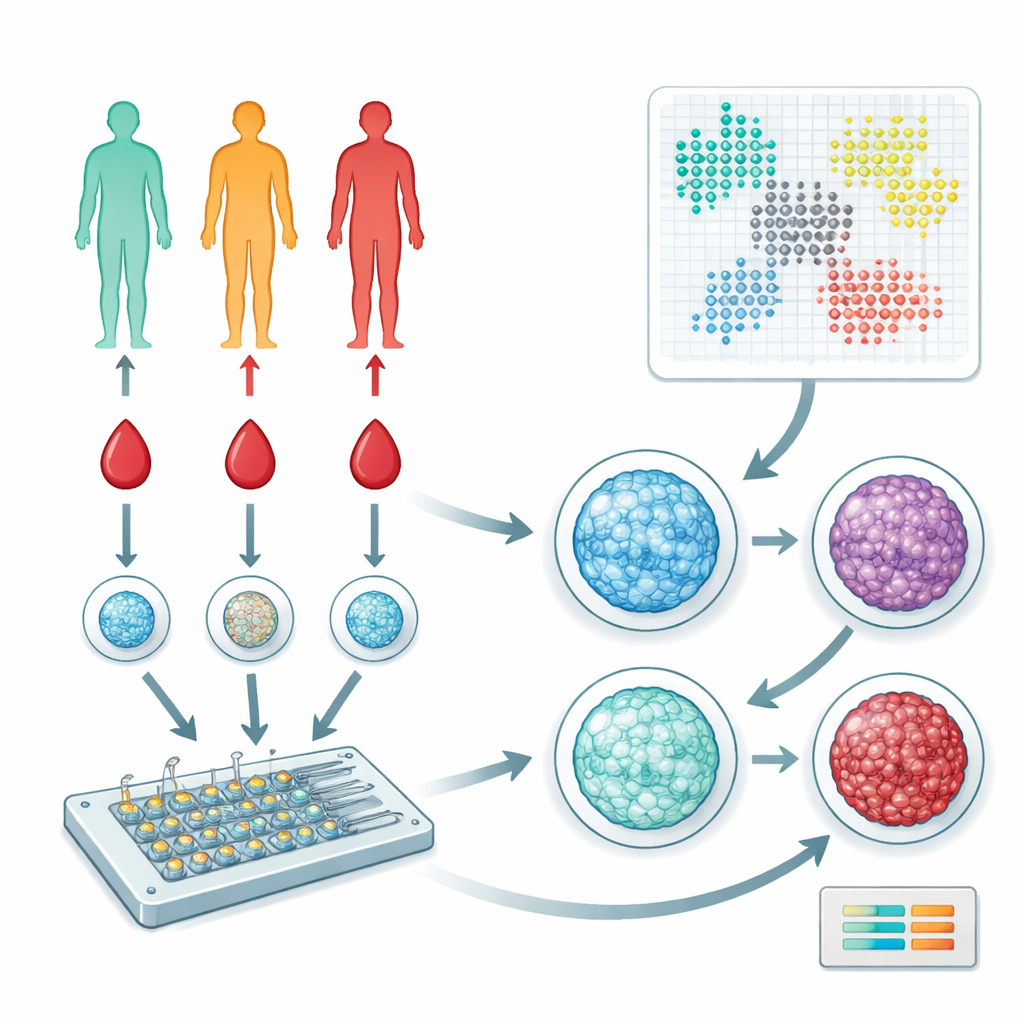
Les chercheurs se sont concentrés sur les cellules mononucléées du sang périphérique (PBMC), un ensemble mixte de cellules immunitaires qui circulent dans le sang et contribuent à coordonner les réponses dans tout l’organisme. Ils ont prélevé du sang de 57 personnes couvrant les stades sain, prédiabète et diabète de type 2. Plutôt que de séquencer des gènes ou de mesurer des dizaines de protéines, l’équipe a utilisé un dispositif microfluidique et des colorants fluorescents pour imager la répartition de l’ADN à l’intérieur du noyau cellulaire. Ce complexe ADN–protéines, appelé chromatine, peut être plus lâche ou plus condensé, et son organisation reflète subtilement le fonctionnement d’une cellule et les signaux qu’elle a reçus.
Transformer des images en motifs
Pour interpréter des dizaines de milliers d’images de noyaux, l’équipe a utilisé un type d’intelligence artificielle appelé autoencodeur variationnel. Ce logiciel compresse chaque image en un ensemble de caractéristiques numériques qui décrivent la taille et la forme du noyau ainsi que la texture fine de la chromatine. Les chercheurs ont ensuite appliqué des méthodes de regroupement fondées sur des graphes pour classer les noyaux en « états » distincts correspondant à différentes sous-populations de cellules immunitaires ou à des niveaux d’activation. Des analyses parallèles basées sur des mesures de forme et de texture soigneusement conçues (caractéristiques manuelles) ont fourni une vérification indépendante des résultats issus de l’IA, et les deux approches ont convergé vers un ensemble de motifs de chromatine récurrents chez les individus.
Des états cellulaires distincts suivent le stade de la maladie
Lorsque les auteurs ont comparé ces clusters basés sur la chromatine entre la santé, le prédiabète et le diabète, des décalages nets sont apparus. Certains états nucléaires étaient enrichis chez les individus sains, d’autres chez les personnes prédiabétiques, et d’autres encore chez les personnes diabétiques. Les caractéristiques décrivant la localisation des poches de chromatine dense dans le noyau — près du bord ou déplacées vers l’intérieur, fortement groupées ou plus séparées — se sont révélées particulièrement informatives. En n’utilisant que la fraction des cellules d’une personne appartenant à chaque cluster, un modèle d’apprentissage automatique standard pouvait distinguer les donneurs diabétiques des donneurs sains et, avec une précision encore plus grande, les diabétiques des prédiabétiques. Ces prédictions ont été confirmées sur des sous-ensembles mis de côté et scindés indépendamment de la cohorte, suggérant que l’organisation de la chromatine porte une information robuste sur la progression de la maladie au niveau des patients individuels.
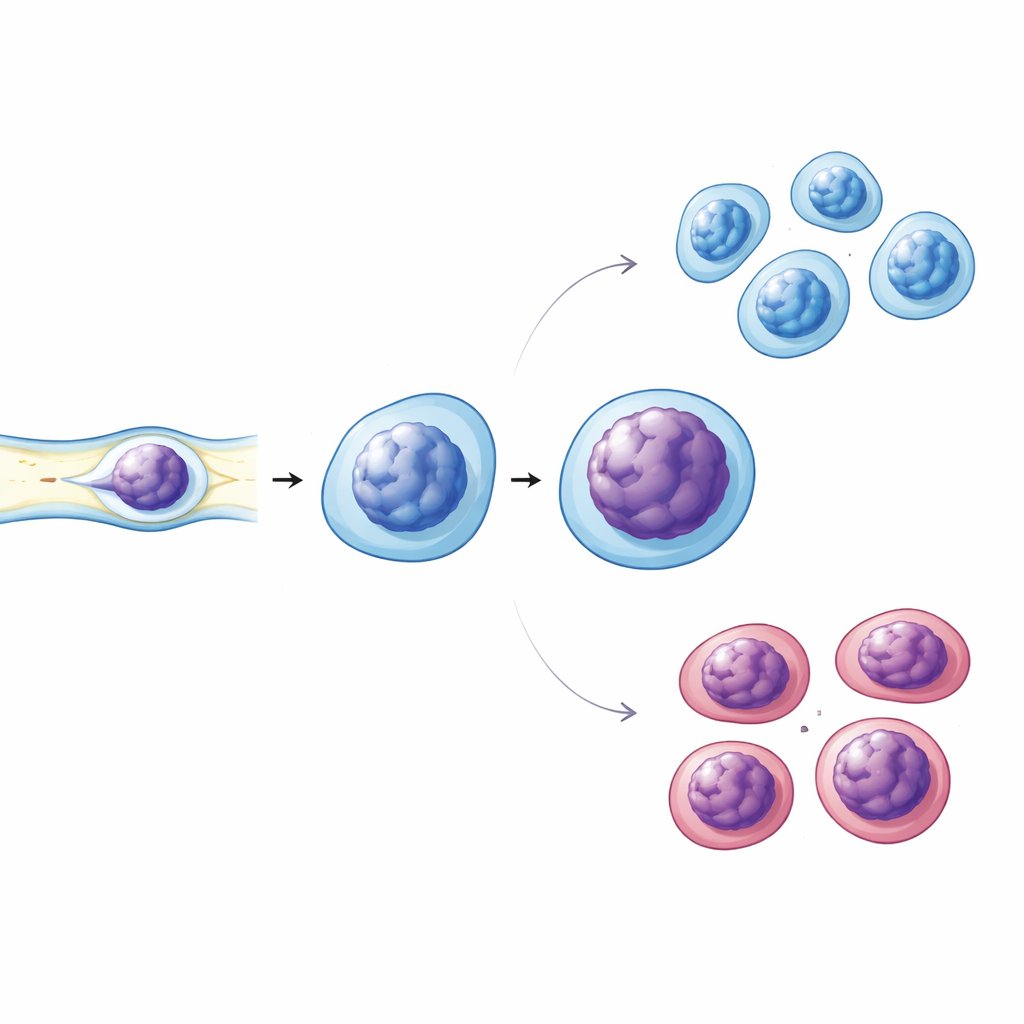
Le stress mécanique révèle des faiblesses subtiles
Les cellules immunitaires se faufilent constamment à travers des espaces étroits dans les vaisseaux et les tissus, aussi l’équipe a-t-elle examiné si leur comportement mécanique change en cas de diabète. Ils ont utilisé de fins microcanaux pour comprimer doucement des cellules immunitaires vivantes tout en imageant leurs noyaux. Les cellules diabétiques ont présenté une déformation nucléaire plus marquée et des signes d’altération de la condensation de la chromatine comparées aux cellules de donneurs sains et prédiabétiques. Des expériences de marquage complémentaires ont révélé que les noyaux diabétiques contenaient moins d’une protéine structurale clé, la Lamin A/C, qui contribue à maintenir la rigidité et la forme du noyau, et présentaient un niveau légèrement plus élevé de marques associées à la chromatine fortement compactée. La fraction de cellules portant un marqueur d’activation à leur surface était également plus élevée en cas de diabète, reliant ces changements nucléaires à une activation immunitaire accrue.
De l’éclairage en laboratoire à un futur outil clinique
Pris ensemble, ces travaux montrent que l’imagerie fluorescente simple de la chromatine sur des échantillons sanguins de routine peut capturer des changements significatifs et spécifiques au patient dans le système immunitaire à mesure que le diabète de type 2 progresse. Si cette approche ne remplace pas encore les tests standards de glucose ou d’HbA1c, elle offre une lecture complémentaire du stress immunitaire et du fonctionnement cellulaire — des informations que les marqueurs cliniques actuels fournissent en grande partie pas. Parce que le test repose sur des colorants et des dispositifs microfluidiques relativement peu coûteux, les auteurs estiment qu’il pourrait éventuellement être mis à l’échelle et automatisé pour un usage clinique, permettant un suivi du diabète et de ses complications plus personnalisé.
Citation: Afarani, M.M., Gupta, R., Uhler, C. et al. Detecting chromatin state alterations in PBMCs associated with Type 2 Diabetes Mellitus. Commun Med 6, 268 (2026). https://doi.org/10.1038/s43856-026-01513-w
Mots-clés: diabète de type 2, cellules immunitaires, imagerie de la chromatine, biomarqueurs, apprentissage automatique