Clear Sky Science · nl
Evaluatie van deep learning-modellen voor sepsisvoorspelling op intensive cares bij verdelingsverschuiving: een multicentrische retrospectieve cohortstudie
Waarom vroegtijdige waarschuwing bij infectie belangrijk is
Sepsis is een snel voortschrijdende, levensbedreigende reactie op een infectie en een van de belangrijkste doodsoorzaken op intensive cares. Ziekenhuizen wenden zich tot kunstmatige intelligentie om subtiele waarschuwingssignalen in monitoren en laboratoriumtests uren eerder te detecteren dan artsen dat kunnen. Er is echter een complicatie: een algoritme dat goed werkt in het ene ziekenhuis presteert vaak minder goed in een ander, omdat patiënten, apparatuur en administratie per locatie verschillen. Deze studie stelt een praktische vraag voor de klinische praktijk: gegeven die verschillen, wat is de slimste manier om een sepsisvoorspellingsmodel opnieuw te gebruiken of aan te passen wanneer het in een nieuwe IC wordt ingezet?
Hoe ziekenhuisdata ongemerkt kunnen veranderen
De onderzoekers begonnen door te laten zien hoe verschillend intensive care-data tussen ziekenhuizen kunnen zijn. Ze vergeleken drie grote IC-databases uit de Verenigde Staten en Zwitserland, allemaal zorgvuldig geharmoniseerd om dezelfde vitale functies en laboratoriumresultaten in de tijd bij te houden. Zelfs na harmonisatie vertoonden veel van de 48 gemeten signalen — zoals bloeddruk, zuurstofwaarden en bepaalde bloedtellingenz — duidelijke verschillen tussen locaties. Statistische tests toonden aan dat in elk paar ziekenhuizen tientallen variabelen afwijkende verdelingen hadden, en sommige kenmerken zich uniek gedroegen in elk dataset. Globaal leken de twee Amerikaanse datasets meer op elkaar dan op de Zwitserse, wat benadrukt dat nationale praktijkpatronen en meetgewoonten een duidelijke stempel op de data zetten die algoritmen moeten interpreteren.
AI testen over meerdere intensive cares
Met die verschillen vastgesteld, trainde het team drie typen deep learning-modellen om sepsis ongeveer zes uur voordat deze formeel werd gediagnosticeerd te voorspellen. Vervolgens testten ze wat er gebeurt wanneer een model dat in één IC is getraind, direct in een andere wordt gebruikt. In het algemeen transfereren modellen redelijk goed, vooral wanneer de doel-IC weinig eigen data heeft. Bijvoorbeeld: wanneer slechts een klein deel van lokale dossiers beschikbaar was, presteerde het gebruik van een vooraf getraind model beter dan het vanaf nul trainen van een nieuw model. Convolutionele neurale netwerken bleken het meest stabiel tussen locaties. Naarmate er meer lokale data werden toegevoegd, nam de prestatie gestaag toe en bereikte uiteindelijk een plateau, waarbij sommige ziekenhuizen (in het bijzonder de grote Amerikaanse multicenter-dataset) gemakkelijker te modelleren waren dan andere.
Verschillende manieren om een model over te dragen
Vervolgens vergeleken de auteurs praktische strategieën voor het inzetten van deze modellen wanneer een ziekenhuis geleidelijk zijn eigen data verzamelt. Ze onderzochten vijf opties: het originele model simpelweg hergebruiken zoals het is; alleen de laatste lagen fijn afstemmen; alle lagen volledig hertrainen met lokale data; een geheel nieuw model trainen op alleen lokale data; en twee vormen van "domeinaanpassing" die de interne kenmerken van bron- en doelziekenhuizen expliciet op elkaar afstemmen. Ze rangschikten doelziekenhuizen naar kleine, middelgrote en grote dataregimes en herhaalden de vergelijking voor meerdere bron–doelparen en modeltypen. Deze systematische aanpak bootste realistische uitrolscenario’s na, van een kleine landelijke IC met een handvol gevallen tot een nationaal netwerk dat tienduizenden opnames bundelt.
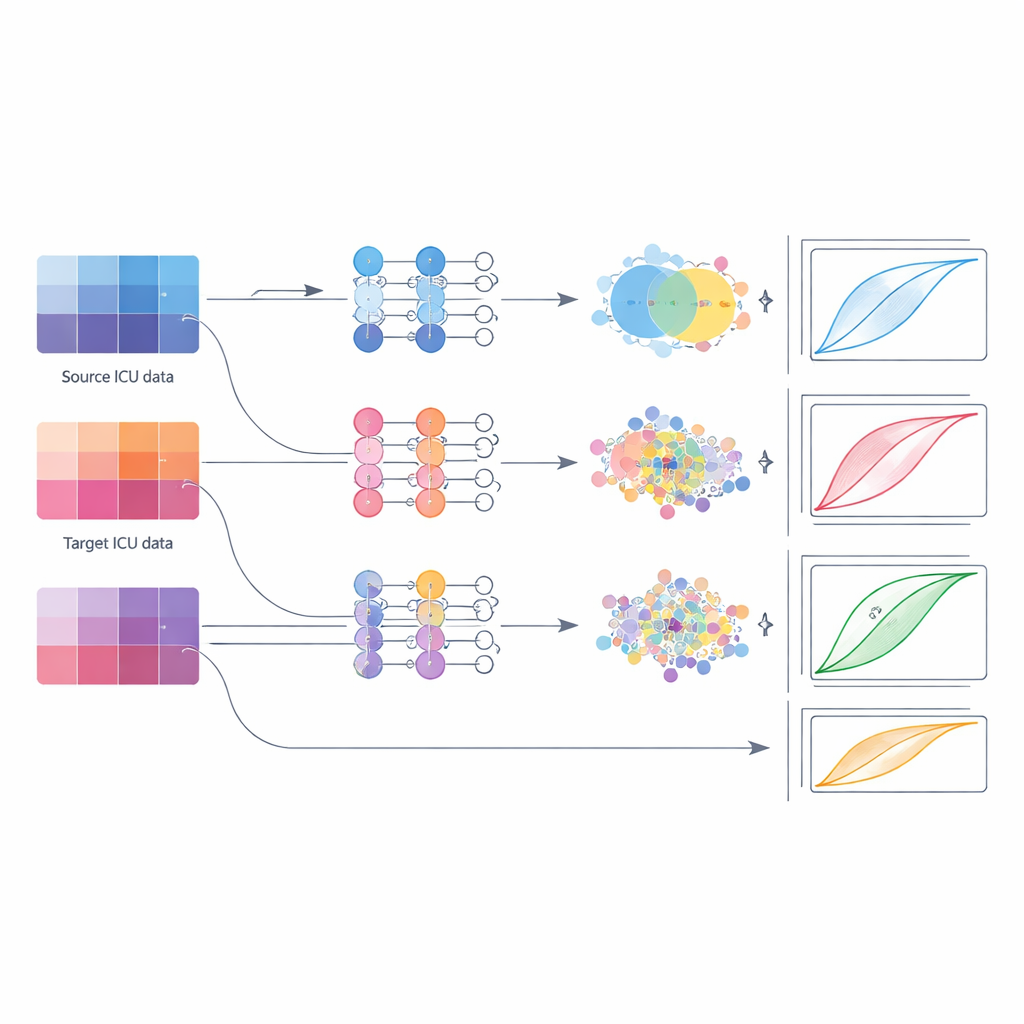
Wat het beste werkt op verschillende dataschalen
De resultaten dagen de gebruikelijke gewoonte uit om te vertrouwen op eenvoudige fijnslijping. In veel situaties liep fijn afstemmen meestal achter andere methoden aan. Wanneer de doel-IC slechts een klein aantal gevallen had, was de beste keuze om te starten vanaf het externe model en vervolgens alle lagen grondig te hertrainen op de lokale data; het samenvoegen van bron- en doeldata in één trainingspool (fusie) kwam dicht in de buurt. Voor middelgrote datasets gaven domeinaanpassingsmethoden — technieken die het model ertoe aanzetten dat kenmerkpatronen van beide ziekenhuizen meer overlappen — de meest betrouwbare winst, met verbeterde discriminatiemetrics en lage variabiliteit. Zodra de doel-IC over een grote dataset beschikte, presteerden modellen die volledig of grotendeels op die lokale data waren getraind, soms met extra fusie, net zo goed of beter dan alle op transfer gebaseerde benaderingen.
Wat dit betekent voor de patiëntenzorg
Voor niet-specialisten is de kernboodschap dat er geen universele manier is om AI voor sepsis tussen ziekenhuizen uit te rollen. Omdat elke IC zijn eigen "data-accent" heeft, kan het simpelweg importeren van een model en het bijsturen van alleen de laatste laag — een veelgebruikte snelkoppeling — prestaties onbenut laten of zelfs clinici misleiden. De studie stelt in plaats daarvan een helder handelingskader voor: in zeer data-arme omgevingen begin je met een extern model en hertrain je dit grondig; naarmate er meer lokale gevallen bij komen, schakel je over op domeinbewuste training die verschillen tussen ziekenhuizen respecteert; en wanneer er grote lokale datasets beschikbaar zijn, geef je prioriteit aan modellen die vooral op die lokale ervaring zijn gebouwd. Het volgen van deze principes kan ziekenhuizen helpen sepsisvoorspellingshulpmiddelen sneller in gebruik te nemen, terwijl de meldingen betrouwbaarder en beter afgestemd op hun eigen patiënten blijven.
Bronvermelding: Tranchellini, F., Farag, Y., Jutzeler, C. et al. Evaluating deep learning sepsis prediction models in ICUs under distribution shift: a multi-centre retrospective cohort study. npj Digit. Med. 9, 306 (2026). https://doi.org/10.1038/s41746-026-02364-4
Trefwoorden: sepsisvoorspelling, intensive care, deep learning, domeinaanpassing, verdelingsverschuiving