Clear Sky Science · nl
Pseudolysogenie-gemedieerde evolutionaire afwegingen bevorderen fagentherapie door antibioticaresistentie en virulentie bij Cutibacterium acnes te beperken
Waarom dit belangrijk is voor mensen met acne
Acne is een van de meest voorkomende huidproblemen en veel mensen ervaren bijwerkingen en afnemend effect bij langdurig antibioticagebruik. Deze studie onderzoekt een andere aanpak: het benutten van van nature voorkomende virussen die zich voeden met acneveroorzakende bacteriën. De auteurs tonen aan dat een bepaald type virus, dat een ongewone "half-slapende" strategie in bacteriën gebruikt, zowel acne kan verminderen als de bacterie verzwakt en minder geneesmiddelresistent maakt — zonder de rest van de huidmicrobiota te verstoren.
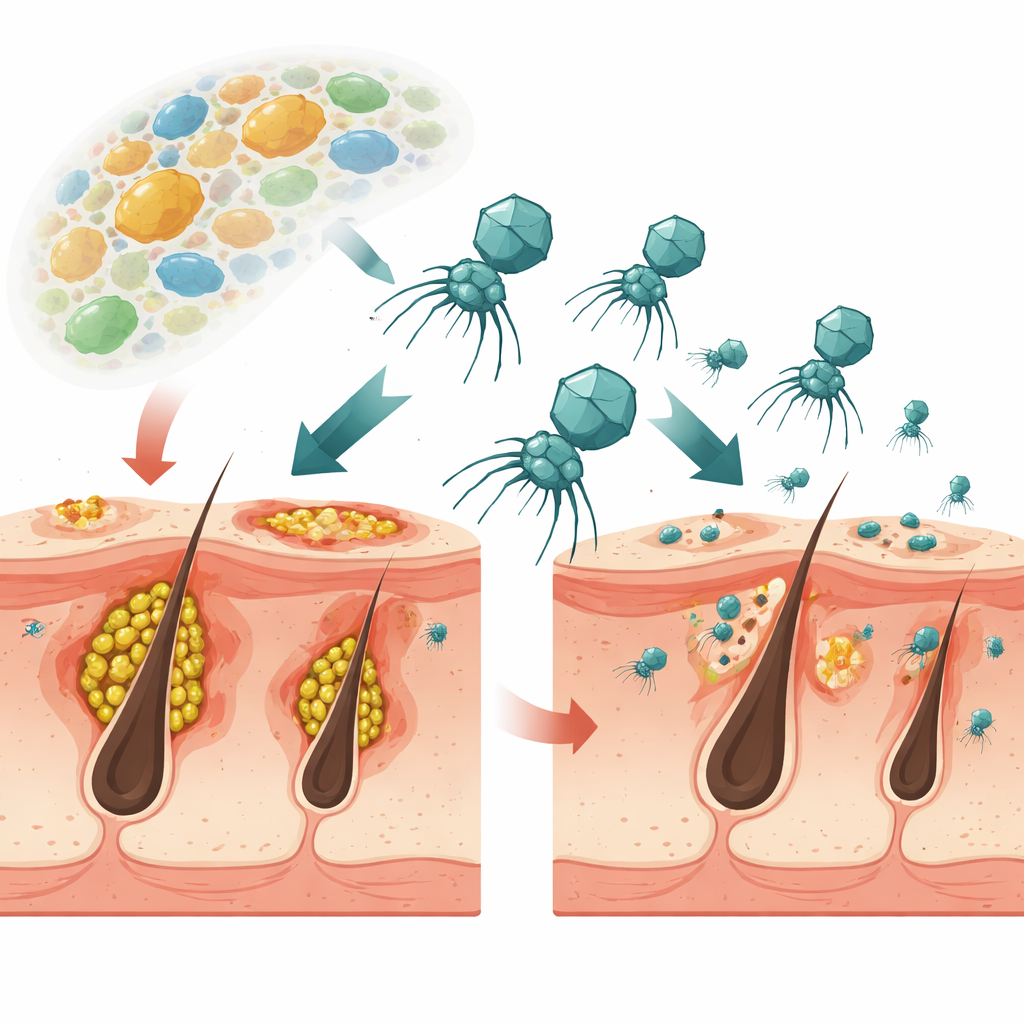
Een nieuw soort virusgebaseerde behandeling voor acne
Het onderzoek richt zich op Cutibacterium acnes, de belangrijkste bacterie die met acne geassocieerd wordt, en op de virussen die deze infecteren, fagen genoemd. In tegenstelling tot standaardantibiotica die veel verschillende bacteriën tegelijk treffen, zijn deze fagen zeer doelgericht. Het team isoleerde meerdere fagen van de huid van gezonde mensen en koos er één, ΦCaCom2 genoemd, omdat deze veel verschillende C. acnes-stammen kon doden, stabiel bleef bij kamertemperatuur en zeer goed was in het afbreken van kleverige bacterielaagjes die biofilms worden genoemd. In laboratoriumtests onderdrukte deze faag de groei van C. acnes en vernietigde biofilms effectiever dan het veelgebruikte antibioticum clindamycine, zelfs wanneer de bacteriën al resistent waren tegen dat middel.
Hoe een half-slapend virus zijn bacteriële gastheer verzwakt
ΦCaCom2 gebruikt een strategie die pseudolysogenie wordt genoemd: in plaats van permanent met het bacteriële DNA te versmelten of de cel meteen te laten barsten, kan het als een circulair stuk genetisch materiaal in de bacterie blijven bestaan. Bacteriën die deze virale cirkel dragen worden tijdelijk beschermd tegen verdere aanvallen door dezelfde faag, maar betalen een prijs. De studie toont aan dat deze "pseudolysogene" bacteriën langzamer groeien, dunnere en zwakkere biofilms vormen en hun concurrentievoordeel verliezen wanneer ze samen worden gekweekt met andere veelvoorkomende huidmicroben. Met andere woorden: als C. acnes probeert aan de faag te ontsnappen door in deze staat te gaan, wordt het een slechtere concurrent in de drukbevolkte wereld van de huid.
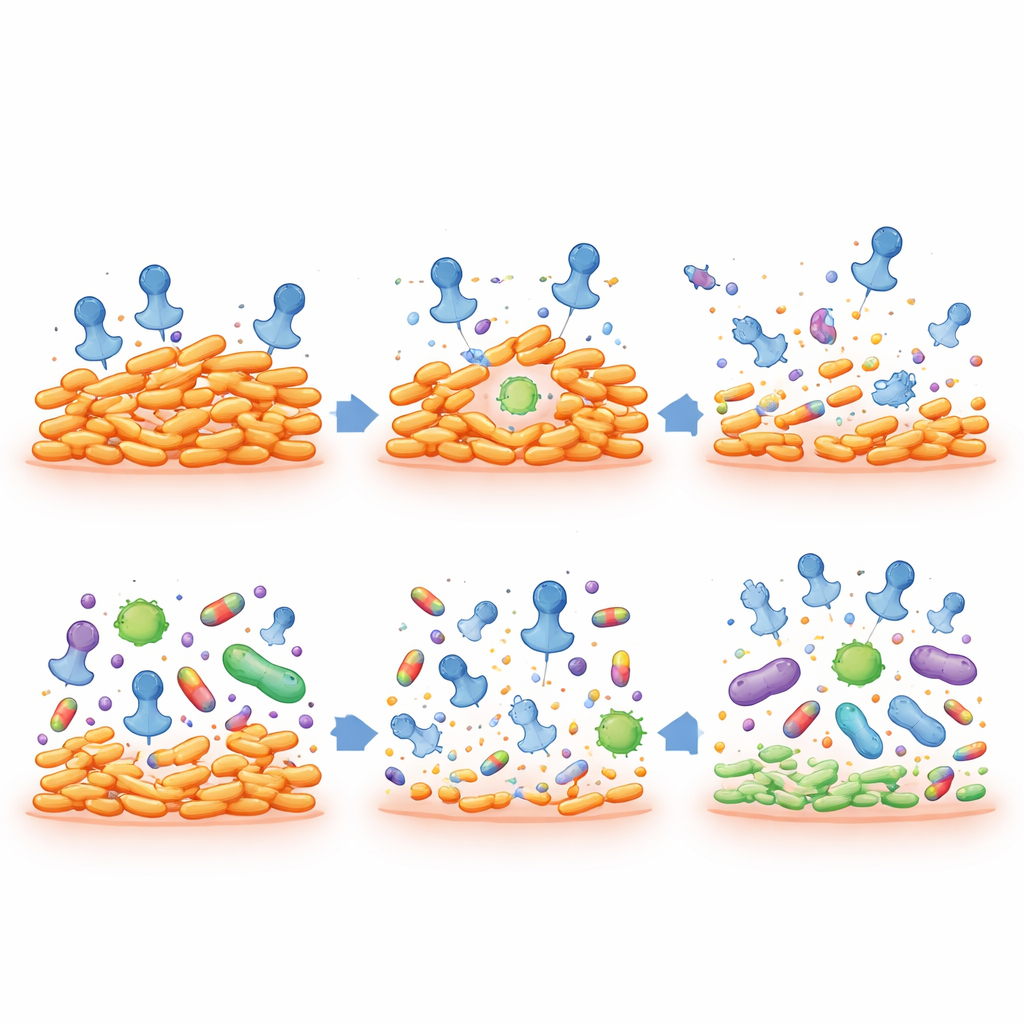
Antibioticaresistentie terugdringen terwijl het microbioom gespaard blijft
De meest opmerkelijke bevinding is dat wanneer geneesmiddelresistente C. acnes-stammen pseudolysogenen worden, ze hun resistentie tegen belangrijke acne-antibiotica, waaronder clindamycine en erytromycine, verliezen. Deze verzwakte bacteriën worden makkelijker te doden, zelfs bij lage medicatiedoses. Tegelijkertijd lijkt de faag zelf geen genen voor antibioticaresistentie te verspreiden: zijn genoom mist de benodigde machinerie hiervoor en directe experimenten vonden geen overdracht van resistentie tussen stammen. In celkweektests met menselijke huidcellen toonde de faagpreparatie geen betekenisvolle toxiciteit, zelfs niet bij zeer hoge doses.
Resultaten van een kleine humane studie
Om te zien hoe dit op echte huid werkt, voerden de onderzoekers een drie maanden durende proof-of-conceptstudie uit bij 18 volwassenen met milde tot matige acne die niet goed hadden gereageerd op standaardbehandelingen. Deelnemers sprayden eenmaal per dag een oplossing met de ΦCaCom2-faag op hun gezicht. Over 12 weken werden zowel rode, ontstoken laesies als verstopte poriën gemiddeld met ongeveer twee derde verminderd. Bacteriële monsters toonden aan dat de hoeveelheid C. acnes op de huid met ongeveer een derde daalde en zelfs twee weken na het stoppen van de behandeling lager bleef. Belangrijk is dat de niveaus van Staphylococcus-soorten — andere belangrijke huidbacteriën — niet toenamen, wat suggereert dat de behandeling het bredere huidmicrobioom niet ontregelde. Er werden geen duidelijke faagresistente C. acnes-klonen gedetecteerd bij de vrijwilligers en de fagen zelf bleven op de huid aanwezig, wat wijst op een aanhoudende milde druk op de doelbacterie.
Wat dit kan betekenen voor toekomstige acnezorg
Samengevat suggereert het werk dat pseudolysogene fagen zoals ΦCaCom2 meer kunnen doen dan alleen acnebacteriën doden. Door C. acnes te dwingen tot een evolutionaire afweging — tijdelijke virale bescherming in ruil voor zwakkere groei, dunnere biofilms en verloren antibioticaresistentie — helpen ze de bacterie onder controle te houden en maken ze deze makkelijker behandelbaar zonder de rest van de huidmicroben te schaden. Hoewel grotere klinische onderzoeken en diepgaandere microbioomstudies nog nodig zijn, wijst deze strategie in de richting van virusgebaseerde acnebehandelingen die ontsteking verminderen, de opkomst van medicijnresistentie beperken en samenwerken met het natuurlijke ecosysteem van de huid in plaats van ertegenin te gaan.
Bronvermelding: Trejo-Hernández, A., Checa, A., Quijada-Ibarra, R. et al. Pseudolysogeny-mediated evolutionary trade-offs favor phage therapy by limiting antibiotic resistance and virulence in Cutibacterium acnes. Sci Rep 16, 10184 (2026). https://doi.org/10.1038/s41598-026-40701-5
Trefwoorden: acne fagentherapie, Cutibacterium acnes, antibioticaresistentie, huidmicrobioom, pseudolysogenie