Clear Sky Science · es
Los intercambios evolutivos mediados por seudolisogenia favorecen la terapia con fagos al limitar la resistencia a antibióticos y la virulencia en Cutibacterium acnes
Por qué esto importa a las personas con acné
El acné es uno de los problemas de piel más comunes, y muchas personas lidian con efectos secundarios y pérdida de eficacia tras el uso prolongado de antibióticos. Este estudio explora un enfoque distinto: aprovechar virus naturales que atacan las bacterias causantes del acné. Los autores muestran que un tipo particular de virus, que emplea una estrategia inusual de “semi-dormir” dentro de la bacteria, puede tanto calmar el acné como debilitar a la bacteria y reducir su resistencia a los fármacos, sin alterar el resto de la comunidad microbiana de la piel.
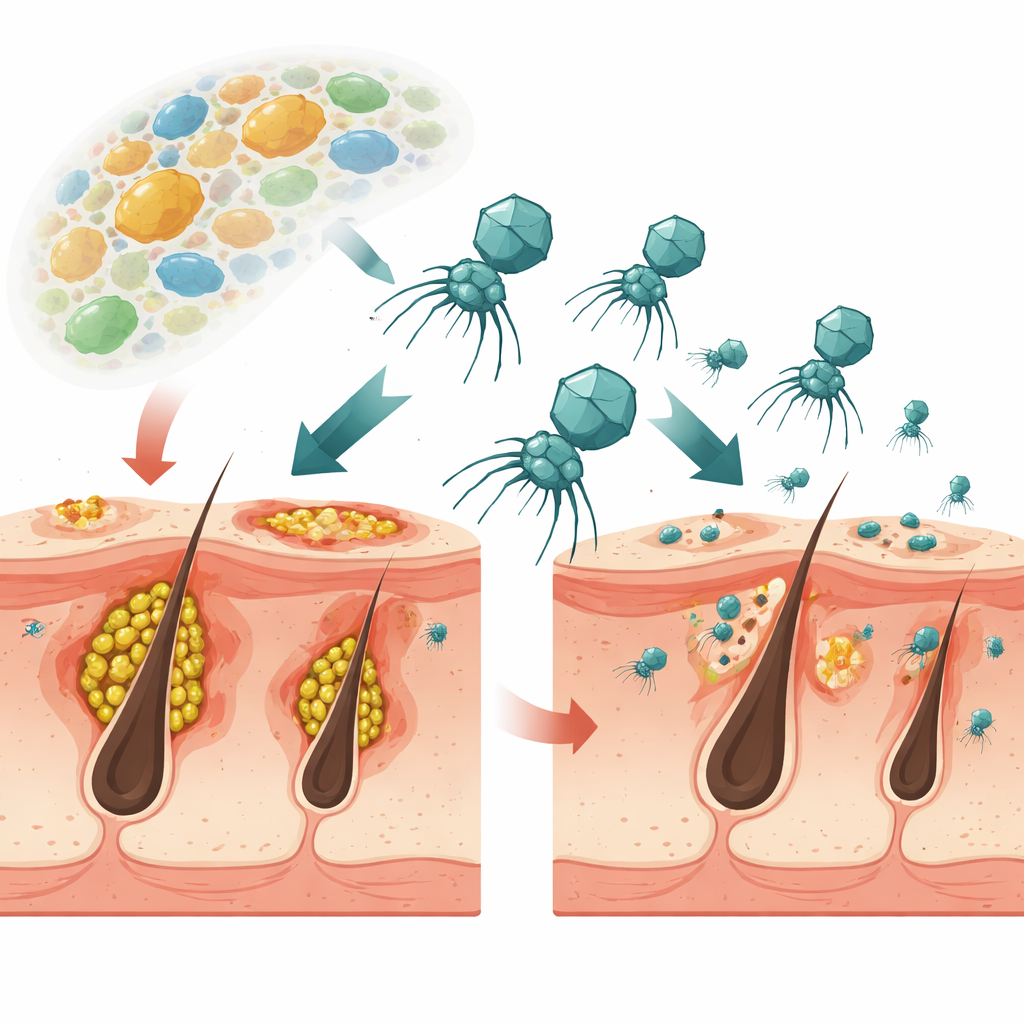
Un nuevo tipo de tratamiento a base de virus para el acné
La investigación se centra en Cutibacterium acnes, la principal bacteria vinculada al acné, y en los virus que la infectan, llamados fagos. A diferencia de los antibióticos convencionales que afectan a muchas bacterias a la vez, estos fagos son muy selectivos. El equipo aisló varios fagos de la piel de personas sanas y eligió uno, denominado ΦCaCom2, porque podía matar muchas cepas diferentes de C. acnes, se mantenía estable a temperatura ambiente y era muy eficaz rompiendo las capas bacterianas pegajosas conocidas como biopelículas. En pruebas de laboratorio, este fago suprimió el crecimiento de C. acnes y destruyó biopelículas con mayor eficacia que el antibiótico clindamicina, incluso cuando las bacterias ya eran resistentes a ese fármaco.
Cómo un virus semi-dormido debilita a su huésped bacteriano
ΦCaCom2 emplea una estrategia llamada seudolisogenia: en lugar de integrarse permanentemente al ADN bacteriano o lisar inmediatamente la célula, puede persistir dentro de la bacteria como un fragmento circular de material genético. Las bacterias que portan este círculo viral quedan temporalmente protegidas contra ataques adicionales del mismo fago, pero lo hacen a costa de un precio. El estudio muestra que estas bacterias “seudolisógenas” crecen más despacio, forman biopelículas más delgadas y débiles, y pierden su ventaja competitiva cuando se cultivan junto con otros microbios cutáneos comunes. En otras palabras, si C. acnes intenta esconderse del fago entrando en este estado, se convierte en un competidor peor en el ambiente concurrido de la piel.
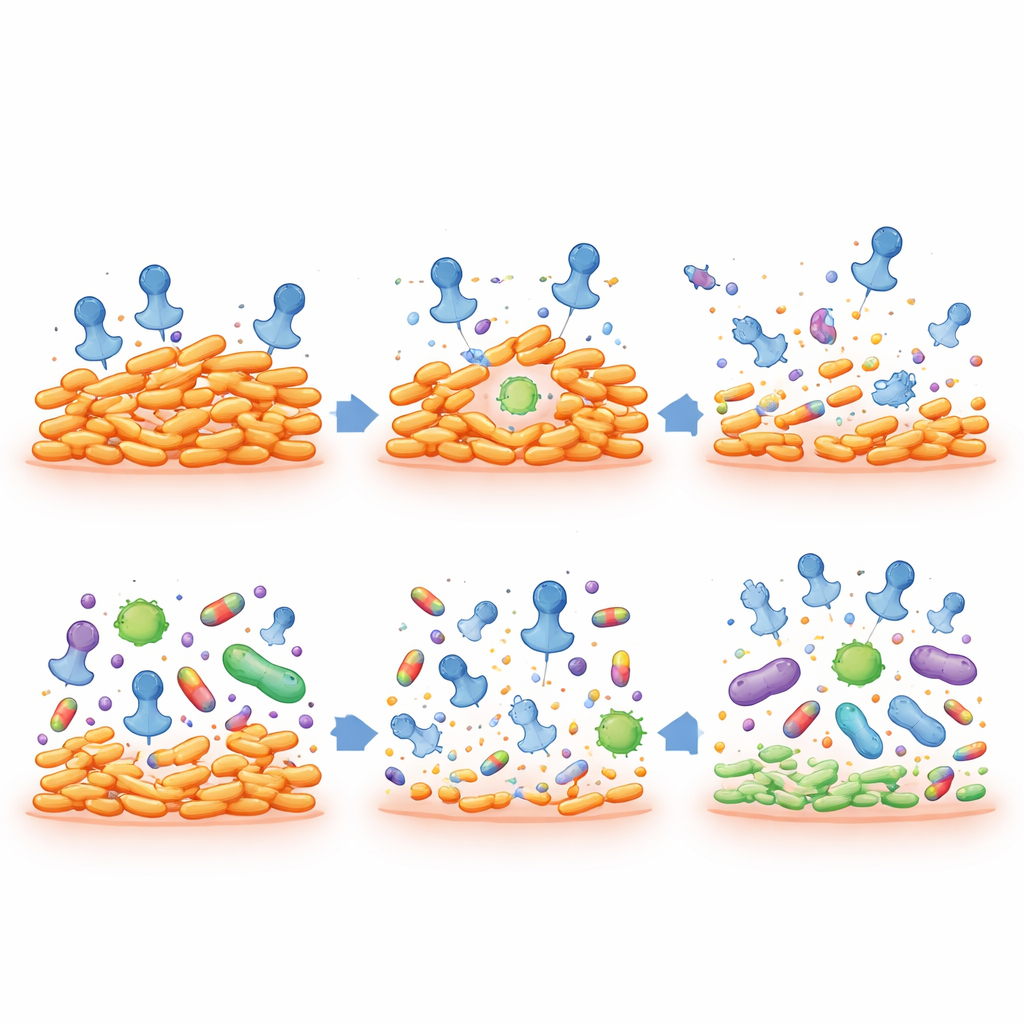
Revertir la resistencia a antibióticos sin dañar el resto del microbioma
El hallazgo más llamativo es que cuando cepas de C. acnes resistentes a fármacos se vuelven seudolisógenas, pierden su resistencia a antibióticos clave para el acné, incluidos clindamicina y eritromicina. Estas bacterias debilitadas pasan a ser más fáciles de eliminar, incluso con dosis bajas de fármaco. Al mismo tiempo, el propio fago no parece propagar genes de resistencia a antibióticos: su genoma carece de la maquinaria necesaria para ello, y experimentos directos no encontraron transferencia de resistencia entre cepas. En ensayos en cultivo celular con células de piel humana, la preparación de fagos no mostró toxicidad significativa, ni siquiera a dosis muy altas.
Resultados de un pequeño estudio en humanos
Para ver cómo funciona en piel real, los investigadores llevaron a cabo un ensayo de prueba de concepto de tres meses en 18 adultos con acné leve a moderado que no habían respondido bien a tratamientos estándar. Los participantes se rociaron una solución que contenía el fago ΦCaCom2 en la cara una vez al día. A lo largo de 12 semanas, tanto las lesiones rojas e inflamadas como los poros obstruidos se redujeron en aproximadamente dos tercios, en promedio. El muestreo bacteriano mostró que la cantidad de C. acnes en la piel se redujo en torno a un tercio y se mantuvo más baja incluso dos semanas después de suspender el tratamiento. Es importante que los niveles de especies de Staphylococcus—otras bacterias cutáneas relevantes—no aumentaron, lo que sugiere que el tratamiento no desequilibró el microbioma cutáneo más amplio. No se detectaron clones claramente resistentes al fago en los voluntarios, y los fagos mismos persistieron en la piel, indicando una presión continua y suave sobre las bacterias objetivo.
Qué podría significar esto para el cuidado futuro del acné
En conjunto, el trabajo sugiere que fagos seudolisógenos como ΦCaCom2 pueden hacer más que simplemente matar bacterias del acné. Al forzar a C. acnes a un intercambio evolutivo—protección viral temporal a cambio de crecimiento más débil, biopelículas más finas y pérdida de resistencia a antibióticos—ayudan a mantener a la bacteria bajo control y facilitan su tratamiento sin dañar el resto de los microbios de la piel. Aunque se necesitan ensayos clínicos más amplios y estudios microbiómicos más profundos, esta estrategia apunta hacia tratamientos para el acné basados en virus que reducen la inflamación, limitan la aparición de resistencia a fármacos y trabajan en consonancia con el ecosistema natural de la piel en lugar de ir contra él.
Cita: Trejo-Hernández, A., Checa, A., Quijada-Ibarra, R. et al. Pseudolysogeny-mediated evolutionary trade-offs favor phage therapy by limiting antibiotic resistance and virulence in Cutibacterium acnes. Sci Rep 16, 10184 (2026). https://doi.org/10.1038/s41598-026-40701-5
Palabras clave: terapia con fagos para el acné, Cutibacterium acnes, resistencia a antibióticos, microbioma cutáneo, seudolisogenia