Clear Sky Science · fr
Les compromis évolutifs médiés par la pseudolysogénie favorisent la phagothérapie en limitant la résistance aux antibiotiques et la virulence de Cutibacterium acnes
Pourquoi cela importe pour les personnes souffrant d’acné
L’acné est l’un des problèmes de peau les plus fréquents, et beaucoup de personnes subissent des effets secondaires et une perte d’efficacité liés à l’usage prolongé d’antibiotiques. Cette étude explore une approche différente : exploiter des virus naturellement présents qui ciblent les bactéries responsables de l’acné. Les auteurs montrent qu’un type particulier de virus, utilisant une stratégie inhabituelle de « demi-sommeil » à l’intérieur des bactéries, peut à la fois calmer l’acné et affaiblir les bactéries en réduisant leur résistance aux médicaments — sans perturber le reste de la communauté microbienne cutanée.
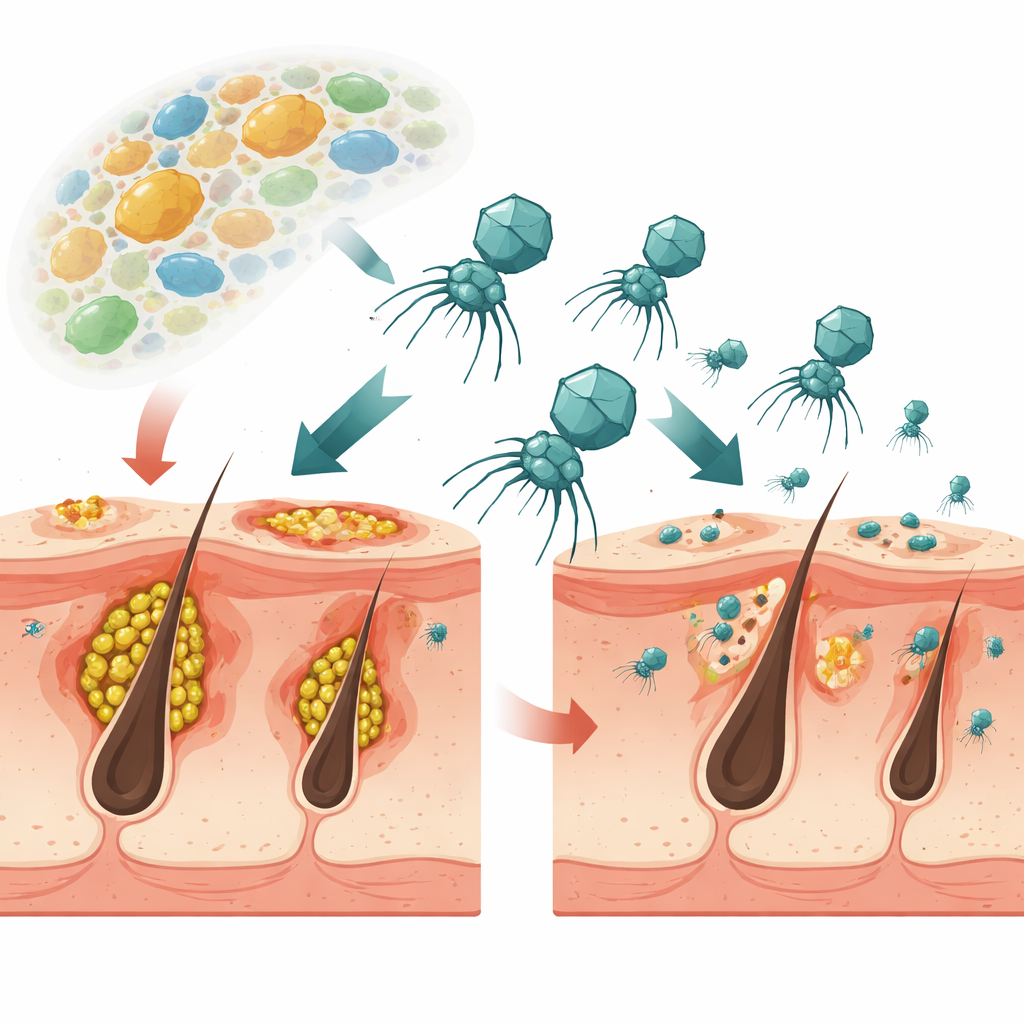
Un nouveau traitement à base de virus pour l’acné
Les chercheurs se sont intéressés à Cutibacterium acnes, la principale bactérie impliquée dans l’acné, et aux virus qui l’infectent, appelés phages. Contrairement aux antibiotiques classiques qui touchent de nombreuses bactéries à la fois, ces phages sont très ciblés. L’équipe a isolé plusieurs phages sur la peau de personnes en bonne santé et en a choisi un, nommé ΦCaCom2, parce qu’il pouvait tuer de nombreuses souches de C. acnes, restait stable à température ambiante et était très efficace pour dégrader les couches bactériennes adhésives appelées biofilms. En laboratoire, ce phage a supprimé la croissance de C. acnes et détruit les biofilms plus efficacement que la clindamycine, un antibiotique couramment utilisé, même lorsque les bactéries étaient déjà résistantes à ce médicament.
Comment un virus « à moitié endormi » affaiblit son hôte bactérien
ΦCaCom2 utilise une stratégie appelée pseudolysogénie : au lieu de s’intégrer définitivement à l’ADN bactérien ou de faire immédiatement éclater la cellule, il peut persister à l’intérieur de la bactérie sous forme d’un élément génétique circulaire. Les bactéries qui portent ce cercle viral deviennent temporairement protégées contre de nouvelles attaques par le même phage, mais elles en paient le prix. L’étude montre que ces bactéries « pseudolysogènes » croissent plus lentement, forment des biofilms plus fins et plus faibles, et perdent leur avantage compétitif lorsqu’elles sont cultivées avec d’autres microbes cutanés courants. Autrement dit, si C. acnes tente d’échapper au phage en entrant dans cet état, il devient un concurrent plus faible dans l’écosystème encombré de la peau.
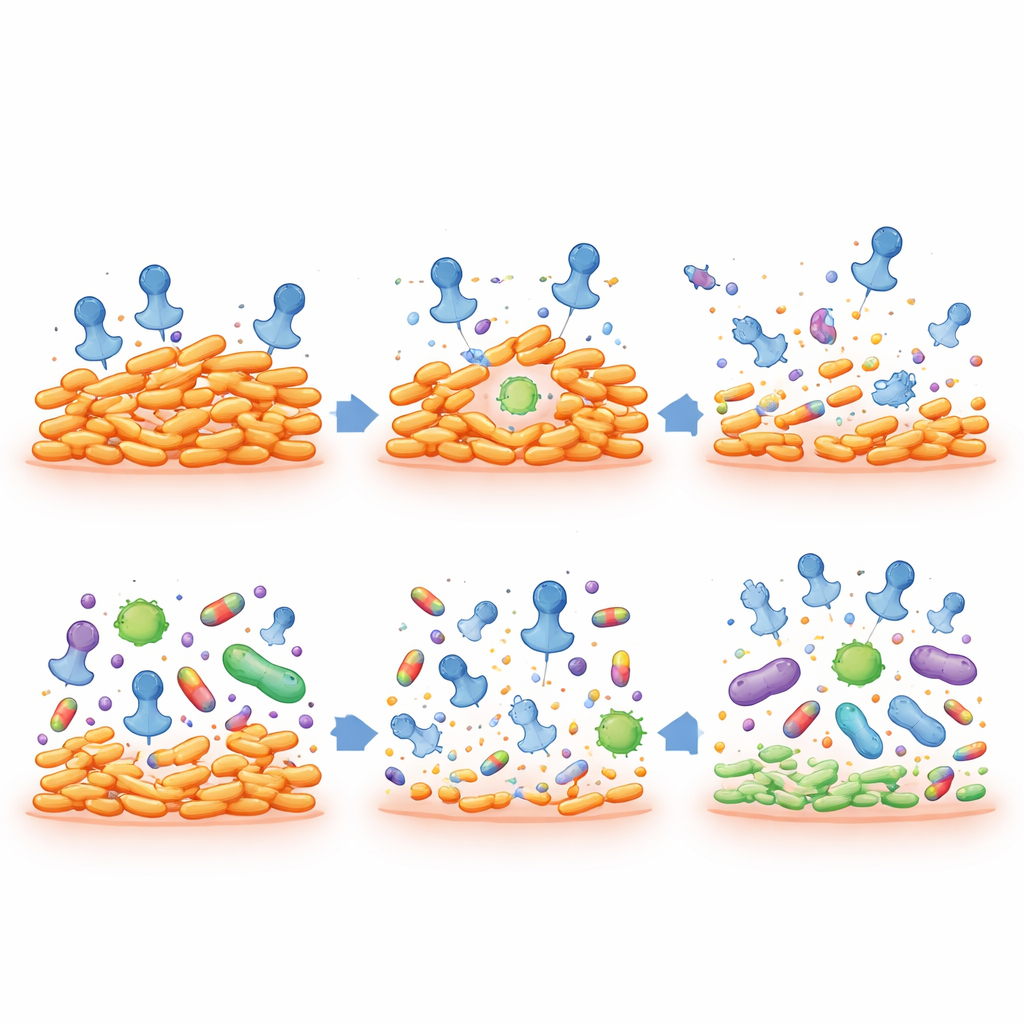
Faire reculer la résistance aux antibiotiques tout en préservant le microbiome
La constatation la plus frappante est que lorsque des souches de C. acnes résistantes aux médicaments deviennent pseudolysogènes, elles perdent leur résistance aux principaux antibiotiques contre l’acné, notamment la clindamycine et l’érythromycine. Ces bactéries affaiblies deviennent plus faciles à éliminer, même à faibles doses de médicament. Parallèlement, le phage lui-même ne semble pas propager de gènes de résistance aux antibiotiques : son génome ne contient pas les éléments nécessaires pour cela, et des expériences directes n’ont montré aucun transfert de résistance entre souches. Dans des tests sur cellules cutanées humaines en culture, la préparation de phages n’a montré aucune toxicité significative, même à des doses très élevées.
Résultats d’une petite étude chez l’humain
Pour tester l’effet sur la peau réelle, les chercheurs ont mené un essai de preuve de concept de trois mois auprès de 18 adultes souffrant d’une acné légère à modérée qui n’avaient pas bien répondu aux traitements standards. Les participants ont pulvérisé une solution contenant le phage ΦCaCom2 sur leur visage une fois par jour. Sur 12 semaines, les lésions rouges et inflammatoires ainsi que les pores obstrués ont été réduits d’environ deux tiers en moyenne. Les prélèvements bactériens ont montré que la quantité de C. acnes sur la peau a diminué d’environ un tiers et est restée plus faible même deux semaines après l’arrêt du traitement. Fait important, les niveaux d’espèces de Staphylococcus — d’autres bactéries cutanées importantes — n’ont pas augmenté, ce qui suggère que le traitement n’a pas déséquilibré le microbiome cutané au sens large. Aucune clone clairement résistant au phage de C. acnes n’a été détecté chez les volontaires, et les phages eux-mêmes ont persisté sur la peau, indiquant une pression continue et douce sur les bactéries ciblées.
Ce que cela pourrait signifier pour les soins futurs de l’acné
Pris ensemble, ces travaux suggèrent que des phages pseudolysogènes comme ΦCaCom2 peuvent faire plus que simplement tuer les bactéries de l’acné. En forçant C. acnes à un compromis évolutif — une protection virale temporaire en échange d’une croissance plus faible, de biofilms plus fins et d’une perte de résistance aux antibiotiques — ils contribuent à maintenir la bactérie sous contrôle et facilitent le traitement sans nuire au reste des microbes de la peau. Bien que des essais cliniques plus larges et des études microbiomiques approfondies soient encore nécessaires, cette stratégie ouvre la voie à des traitements antiviraux de l’acné qui réduisent l’inflammation, limitent l’émergence de résistances et fonctionnent en harmonie avec l’écosystème naturel de la peau plutôt que contre lui.
Citation: Trejo-Hernández, A., Checa, A., Quijada-Ibarra, R. et al. Pseudolysogeny-mediated evolutionary trade-offs favor phage therapy by limiting antibiotic resistance and virulence in Cutibacterium acnes. Sci Rep 16, 10184 (2026). https://doi.org/10.1038/s41598-026-40701-5
Mots-clés: phagothérapie contre l’acné, Cutibacterium acnes, résistance aux antibiotiques, microbiome cutané, pseudolysogénie