Clear Sky Science · de
Pseudolysogenie-vermittelte evolutionäre Zielkonflikte begünstigen Phagentherapie, indem sie Antibiotikaresistenz und Virulenz bei Cutibacterium acnes begrenzen
Warum das für Menschen mit Akne wichtig ist
Akne ist eines der häufigsten Hautprobleme, und viele Menschen kämpfen mit Nebenwirkungen und nachlassender Wirksamkeit bei langfristiger Antibiotikaanwendung. Diese Studie untersucht einen anderen Ansatz: die Nutzung natürlicher Viren, die die akneverursachenden Bakterien befällen. Die Autor:innen zeigen, dass ein bestimmter Virustyp, der eine ungewöhnliche „halb-schlafende“ Strategie innerhalb von Bakterien nutzt, sowohl die Akne abschwächen als auch die Bakterien schwächen und weniger medikamentenresistent machen kann — ohne die übrige mikrobielle Gemeinschaft der Haut zu stören.
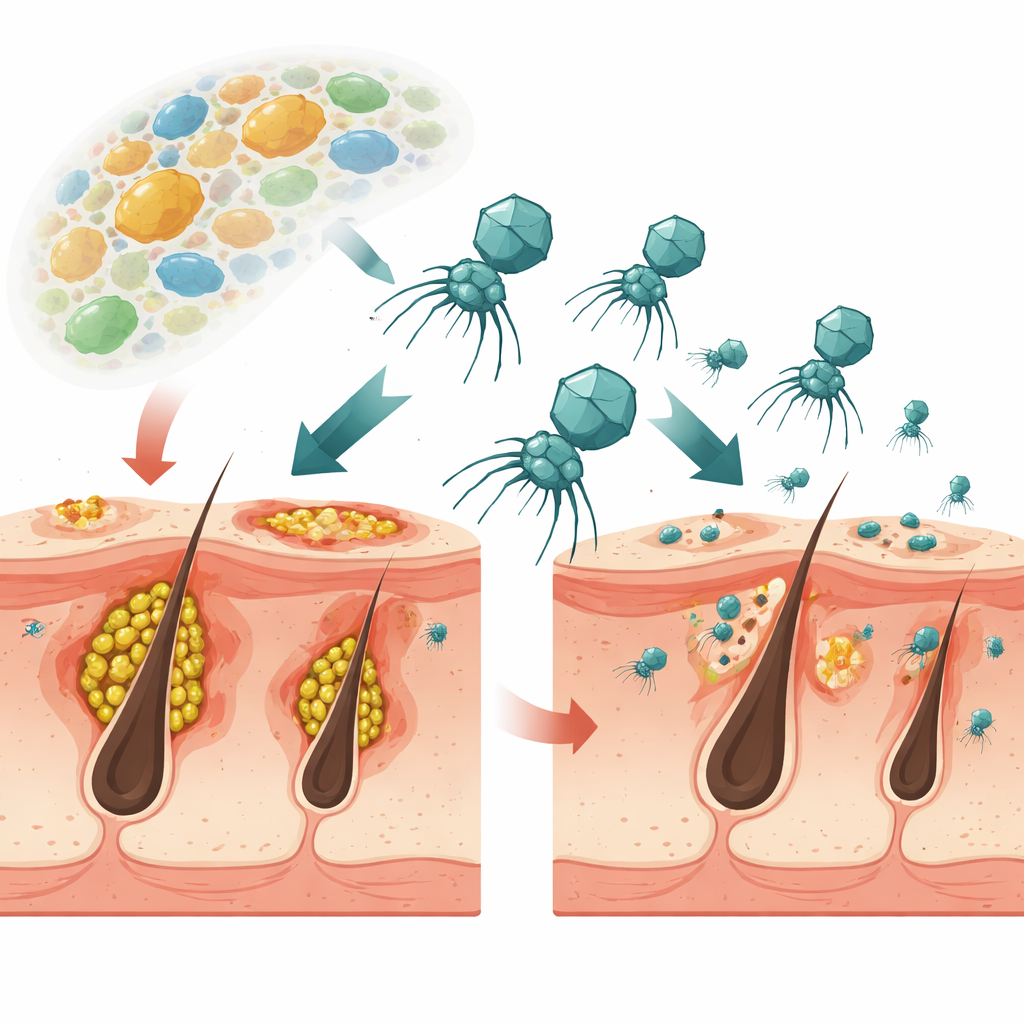
Eine neue, virusbasierte Behandlung gegen Akne
Die Forschung konzentriert sich auf Cutibacterium acnes, das wichtigste mit Akne verknüpfte Bakterium, und auf die Viren, die es infizieren, sogenannte Phagen. Anders als Standardantibiotika, die viele Bakterien gleichzeitig treffen, sind diese Phagen sehr gezielt. Das Team isolierte mehrere Phagen von der Haut gesunder Menschen und wählte einen mit dem Namen ΦCaCom2 aus, weil er viele verschiedene C.-acnes-Stämme abtöten konnte, bei Raumtemperatur stabil blieb und sehr gut klebrige bakterielle Schichten, sogenannte Biofilme, aufbrechen konnte. In Labortests unterdrückte dieser Phage das Wachstum von C. acnes und zerstörte Biofilme wirkungsvoller als das häufig verwendete Antibiotikum Clindamycin, selbst wenn die Bakterien bereits gegen dieses Mittel resistent waren.
Wie ein halb-schlafender Phage seinen bakteriellen Wirt schwächt
ΦCaCom2 verwendet eine Strategie namens Pseudolysogenie: Anstatt dauerhaft mit der bakteriellen DNA zu verschmelzen oder die Zelle sofort zum Platzen zu bringen, kann er im Bakterium als kreisförmiges Stück genetischen Materials persistieren. Bakterien, die diesen viralen Kreis tragen, sind vorübergehend gegen einen erneuten Angriff desselben Phagen geschützt, zahlen dafür aber einen Preis. Die Studie zeigt, dass diese „Pseudolysogen“-Bakterien langsamer wachsen, dünnere, schwächere Biofilme bilden und ihren Wettbewerbsvorteil verlieren, wenn sie zusammen mit anderen häufigen Hautmikroben kultiviert werden. Mit anderen Worten: Wenn sich C. acnes vor dem Phagen schützt, indem es in diesen Zustand geht, wird es in der dicht besiedelten Hautumgebung zum schlechteren Konkurrenten.
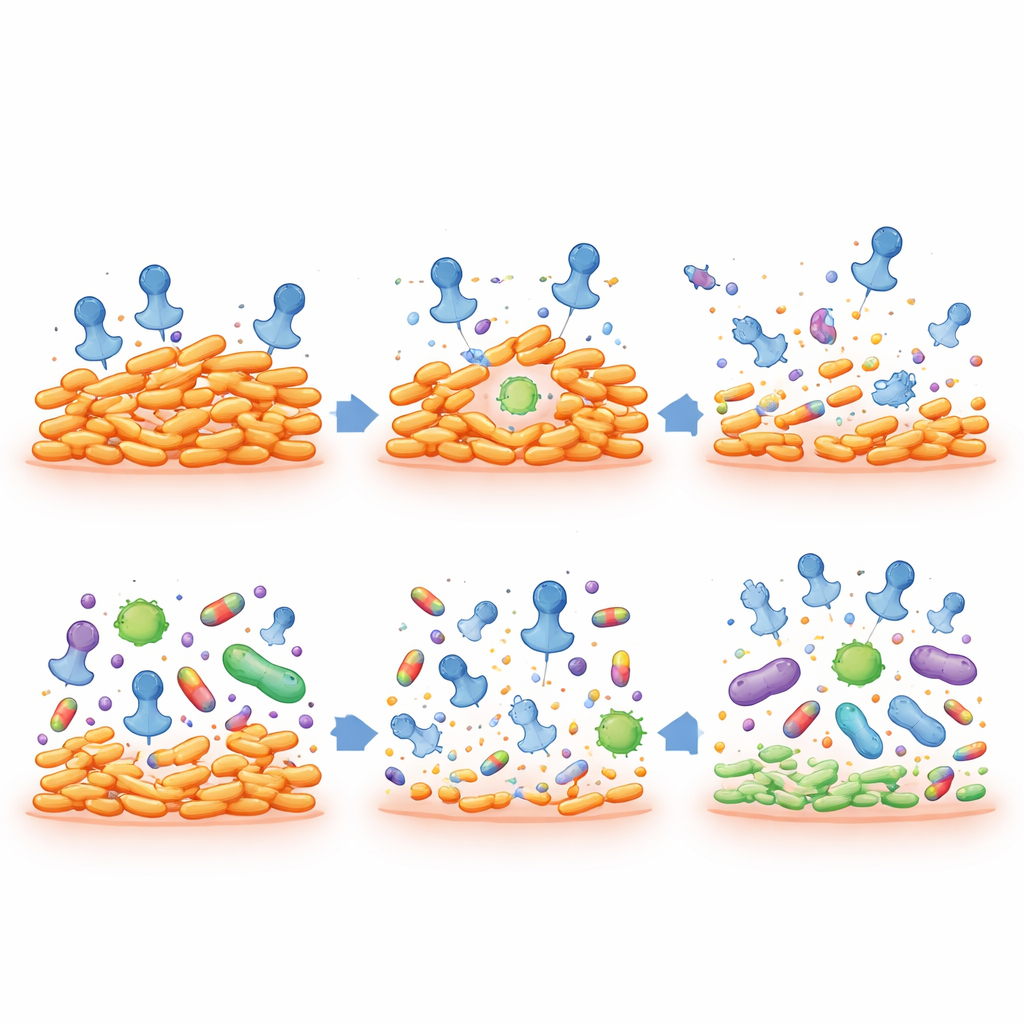
Antibiotikaresistenz zurückdrehen und gleichzeitig das übrige Mikrobiom schonen
Das auffälligste Ergebnis ist, dass sich antibiotikaresistente C.-acnes-Stämme beim Übergang zu Pseudolysogenen ihre Resistenz gegen wichtige Akne-Antibiotika, darunter Clindamycin und Erythromycin, verlieren. Diese geschwächten Bakterien werden leichter zu töten, selbst bei niedrigen Wirkstoffdosen. Zugleich scheint der Phage selbst keine Antibiotikaresistenzgene zu verbreiten: Sein Genom enthält nicht die dafür nötige Maschinerie, und direkte Experimente zeigten keine Übertragung von Resistenz zwischen Stämmen. In Zellkulturtests mit menschlichen Hautzellen zeigte die Phagenpräparation selbst bei sehr hohen Dosen keine relevante Toxizität.
Ergebnisse aus einer kleinen Humanstudie
Um zu prüfen, wie das auf tatsächlicher Haut funktioniert, führten die Forschenden eine dreimonatige Proof-of-Concept-Studie mit 18 Erwachsenen mit leichter bis mäßiger Akne durch, die auf Standardbehandlungen nicht gut angesprochen hatten. Die Teilnehmenden sprühten einmal täglich eine Lösung mit dem Phagen ΦCaCom2 ins Gesicht. Über 12 Wochen wurden sowohl rote, entzündete Läsionen als auch verstopfte Poren im Durchschnitt um etwa zwei Drittel reduziert. Bakterielle Proben zeigten, dass die Menge an C. acnes auf der Haut um ungefähr ein Drittel zurückging und auch zwei Wochen nach Beendigung der Behandlung niedriger blieb. Wichtig ist, dass die Mengen an Staphylococcus-Arten — anderen wichtigen Hautbakterien — nicht anstiegen, was darauf hindeutet, dass die Behandlung das breitere Hautmikrobiom nicht aus dem Gleichgewicht brachte. Bei den Freiwilligen wurden keine klaren phagenresistenten C.-acnes-Klone nachgewiesen, und Phagen selbst blieben auf der Haut nachweisbar, was auf anhaltenden, milden Druck auf die Zielbakterien hinweist.
Was das für die zukünftige Akneversorgung bedeuten könnte
Insgesamt deutet die Arbeit darauf hin, dass pseudolysogene Phagen wie ΦCaCom2 mehr leisten können als nur Akne-Bakterien abzutöten. Indem sie C. acnes in einen evolutionären Zielkonflikt zwingen — vorübergehender Virenschutz im Tausch gegen schwächeres Wachstum, dünnere Biofilme und verlorene Antibiotikaresistenz — helfen sie, das Bakterium in Schach zu halten und machen es leichter behandelbar, ohne die übrigen Hautmikroben zu schädigen. Obwohl größere klinische Studien und tiefere Mikrobiom-Analysen noch erforderlich sind, weist diese Strategie auf virusbasierte Aknebehandlungen hin, die Entzündungen verringern, die Entstehung von Resistenzen begrenzen und mit dem natürlichen Ökosystem der Haut zusammenwirken statt gegen es zu arbeiten.
Zitation: Trejo-Hernández, A., Checa, A., Quijada-Ibarra, R. et al. Pseudolysogeny-mediated evolutionary trade-offs favor phage therapy by limiting antibiotic resistance and virulence in Cutibacterium acnes. Sci Rep 16, 10184 (2026). https://doi.org/10.1038/s41598-026-40701-5
Schlüsselwörter: Akne-Phagentherapie, Cutibacterium acnes, Antibiotikaresistenz, Hautmikrobiom, Pseudolysogenie