Clear Sky Science · nl
Door immuun opgewekte TCR‑achtige antilichamen regelen specifieke T‑celreacties bij muizen
Waarom sommige immuunreacties zichzelf stilletjes dempen
Ons immuunsysteem moet een delicate balans bewaren: het moet indringers zoals virussen en bacteriën aanvallen, maar tegelijk vermijden dat het het eigen weefsel beschadigt. Dit artikel onthult een tot nu toe onderkende zelfremmende eigenschap binnen dat systeem: speciale antilichamen die dezelfde moleculaire doelen herkennen als bepaalde T‑cellen en deze selectief kunnen kalmeren. Inzicht in deze ingebouwde rem kan nieuwe, zeer gerichte manieren openen om auto‑immuunziekten te behandelen zonder de algemene immuniteit te verzwakken.
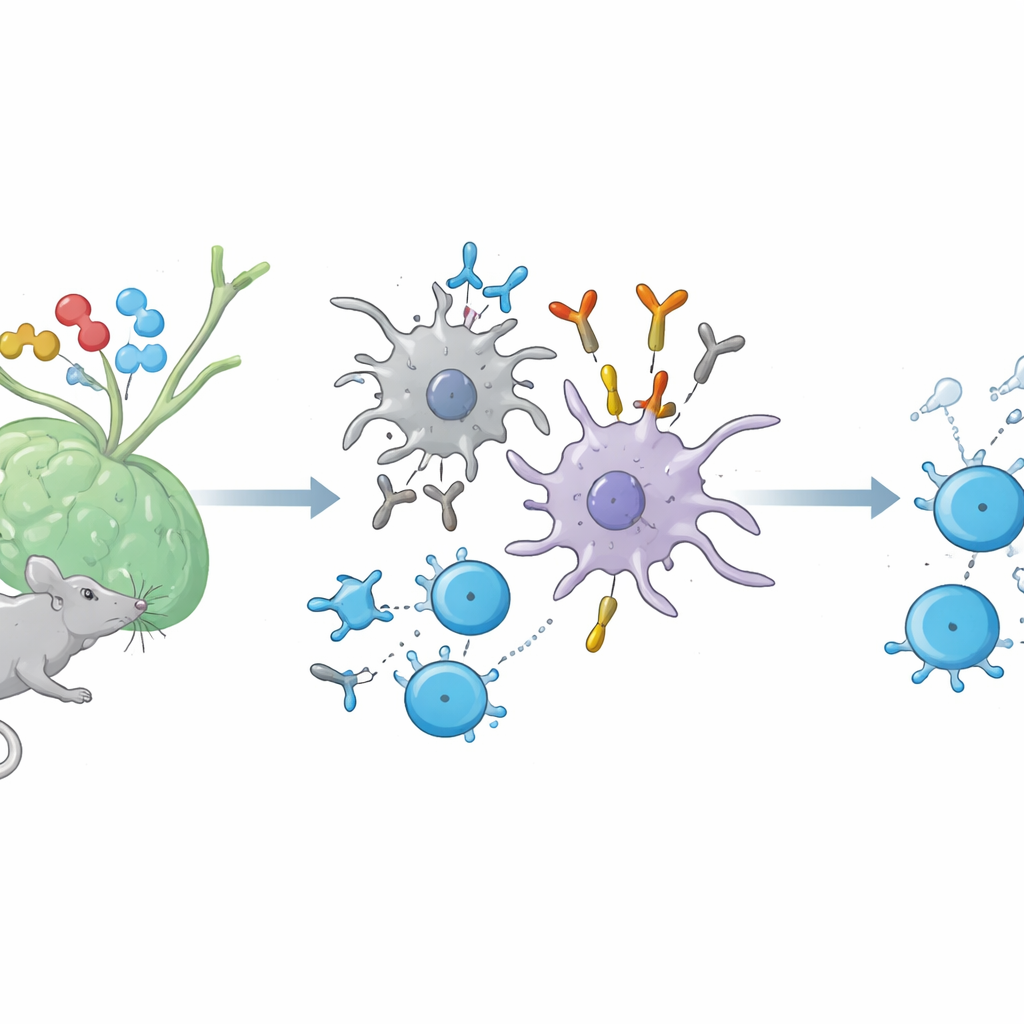
Een verborgen gesprek tussen antilichamen en helper‑T‑cellen
Als we worden gevaccineerd met een eiwit, worden twee belangrijke krachten in gang gezet. B‑cellen maken antilichamen tegen het vreemde eiwit, terwijl helper‑T‑cellen kleine fragmenten van dat eiwit herkennen die op het oppervlak van immuuncellen worden gepresenteerd door moleculen die MHC klasse II heten. Tot nu toe dachten wetenschappers dat antilichamen die deze gecombineerde "fragment plus MHC"‑structuur herkennen—net zoals een T‑celreceptor doet—alleen in kunstmatige labopstellingen voorkomen. Bij muizen laten de auteurs zien dat dergelijke TCR‑achtige antilichamen in feite op natuurlijke wijze worden geproduceerd tijdens gewone immuunreacties tegen verschillende eiwitten, waaronder kippenei‑lysozym, ovalbumine en een zenuwschede‑eiwit dat gerelateerd is aan multiple sclerose.
Hoe peptide‑"staarten" deze speciale antilichamen inschakelen
Om te begrijpen wanneer deze ongebruikelijke antilichamen ontstaan, vergeleken de onderzoekers immuunreacties op korte peptidefragmenten versus iets langere versies die extra aminozuur"staarten" aan één kant dragen, bekend als flankresiduen. Beide versies kunnen door MHC klasse II worden gepresenteerd en door T‑cellen worden gezien, maar ze verschillen in hoeveel extra sequentie er uitsteekt. Het team ontdekte dat alleen peptiden met zulke flankresiduen betrouwbaar het verschijnen van de nieuwe antilichamen uitlokten, die zij immune‑induced TCR‑like antibodies of iTabs noemden. Deze iTabs herkenden niet simpelweg het peptide of het MHC‑molecuul afzonderlijk; ze herkenden de precieze driedimensionale combinatie van een specifiek peptide, diens flankende stuk en een bepaald MHC‑type—en weerspiegelden daarmee de fijne specificiteit van een T‑celreceptor.
Antilichaamremmen op overactieve helper‑T‑cellen
Eens aanwezig fungeerden iTabs als zeer selectieve remmen op helper‑T‑cellen. In kweekexperimenten binden iTabs aan peptide–MHC‑complexen en blokkeerden ze T‑celreceptor‑fusieproteïnen en reporter‑T‑cellen om hun doel te bereiken. Ze verminderden ook de productie van IL‑2, een sleutel signaal voor T‑celgroei, en dempten een klassieke T‑celgedreven huidzwelling in levende muizen. Structureel werk met hoog‑resolutie cryo‑elektronenmicroscopie toonde waarom: het bindingsgebied van een iTab klemt zich vast aan zowel het MHC‑oppervlak als de peptide‑staart, waardoor een nauwe passing ontstaat die fysiek de toegang van T‑cellen belemmert. Sommige iTabs konden ook antigeen‑presenterende B‑cellen markeren voor vernietiging via de gebruikelijke "staart"‑functies van antilichamen, wat een extra manier bood om een lopende reactie te laten bedaren.
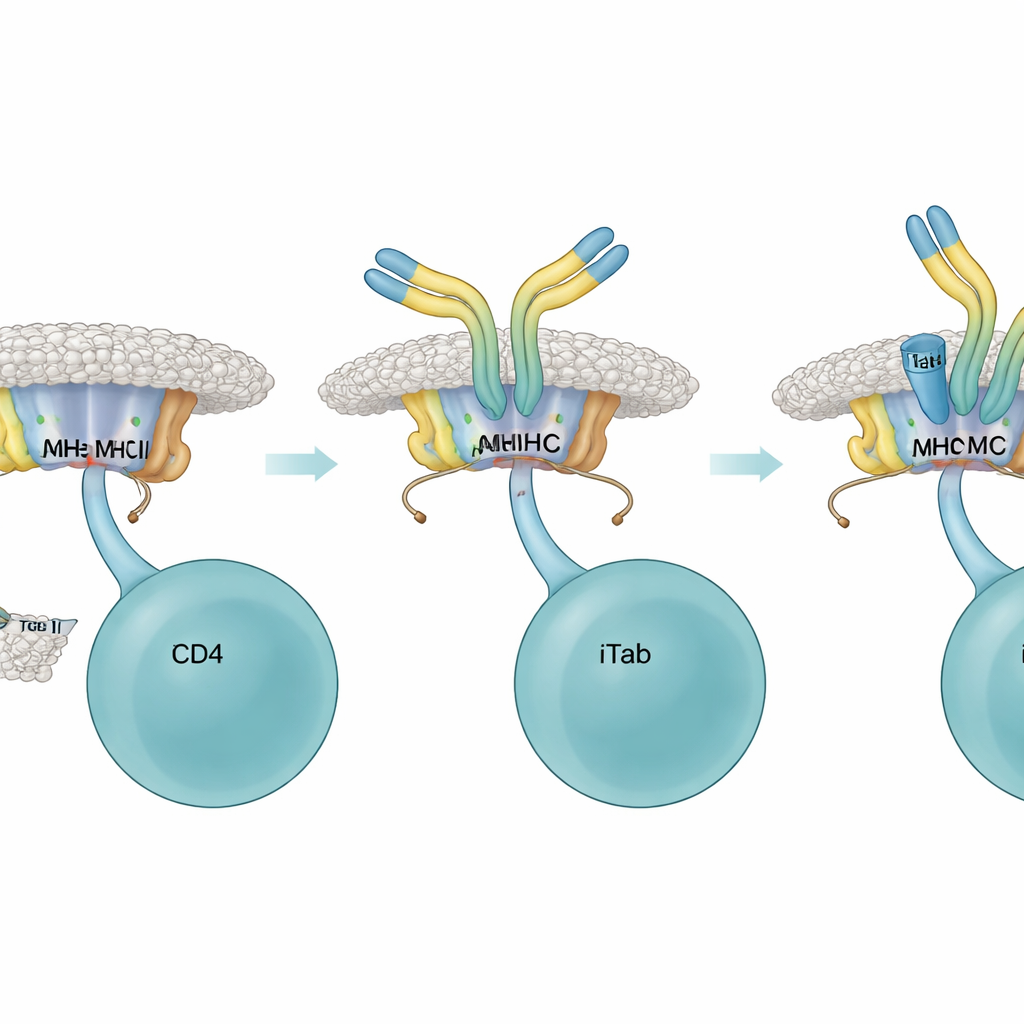
iTabs inzetten tegen auto‑immuniteit
Gesteund door deze kennis vroegen de onderzoekers of iTabs benut konden worden om schadelijke zelf‑reactieve T‑cellen te temmen in een muismodel van multiple sclerose, experimentele auto‑immuunencefalomyelitis genoemd. Ze ontwierpen peptiden van een myeline‑eiwit die flankresiduen bevatten en in sommige versies subtiele wijzigingen die voorkomen dat ze ziekte‑veroorzakende T‑cellen activeren, terwijl ze toch iTab‑inductie mogelijk maken. Het immuniseren van muizen met deze op maat gemaakte peptiden genereerde iTabs die ziekte‑relevante peptide–MHC‑complexen herkenden en de meeste geteste pathogene T‑celreceptoren blokkeerden. Behandelen van muizen met dergelijke iTabs, of ze vooraf immuniseren met iTab‑inductieve peptiden voordat de ziekte werd geactiveerd, leidde tot mildere symptomen en vertraagde of verminderde ziekteprogressie, zelfs wanneer de totale antilichaamniveaus tegen het peptide vergelijkbaar waren.
Wat dit betekent voor toekomstige precisietherapieën
Al met al onthult de studie iTabs als een natuurlijke, voorbijgaande laag van immuunregulatie: antilichamen die T‑celreceptoren imiteren, zich vastklampen aan precies die peptide–MHC‑complexen die door bepaalde helper‑T‑cellen worden herkend, en die reacties selectief temperen. Door zorgvuldig peptiden met de juiste flanksequenties te kiezen, zou het mogelijk kunnen zijn om opzettelijk iTabs op te wekken die alleen schadelijke autoreactieve T‑cellen richten, terwijl beschermende immuniteit intact blijft. Hoewel deze bevindingen bij muizen zijn gedaan en vertaling naar mensen complex zal zijn, schetsen ze een pad naar "ontworpen remmen" voor auto‑immuun‑ en allergische ziektes—behandelingen die niet werken door het immuunsysteem breed te onderdrukken, maar door stilletjes de moleculaire gesprekken te blokkeren die ongewenste aanvallen aansturen.
Bronvermelding: Kishida, K., Kawakami, K., Tanabe, H. et al. Immune-induced TCR-like antibodies regulate specific T cell response in mice. Nat Commun 17, 3227 (2026). https://doi.org/10.1038/s41467-026-71384-1
Trefwoorden: autoimmuniteit, helper‑T‑cellen, MHC klasse II, regulerende antilichamen, peptide flankresiduen