Clear Sky Science · ar
أجسام مضادة شبيهة بمُستقبلات الخلايا التائية تحفّزها المناعة وتُنظّم استجابة خلايا T محددة في الفئران
لماذا تنخفض بعض الاستجابات المناعية بهدوء من تلقاء نفسها
يجب أن يحافظ جهازنا المناعي على توازن دقيق: عليه مهاجمة الدخلاء مثل الفيروسات والبكتيريا، وفي الوقت نفسه تجنّب إلحاق الضرر بأنسجة الجسم نفسه. تكشف هذه الورقة ميزة كبح ذاتي داخل النظام لم تُنتبه إليها سابقًا — أجسام مضادة خاصة تتعرّف على نفس الأهداف الجزيئية التي تتعرف عليها أنواع معينة من خلايا T وقادرة على تهدئتها بشكل انتقائي. قد يفتح فهم هذا الكبح الداخلي طرقًا جديدة مستهدفة للغاية لعلاج الأمراض المناعية الذاتية من دون إضعاف المناعة عامةً.
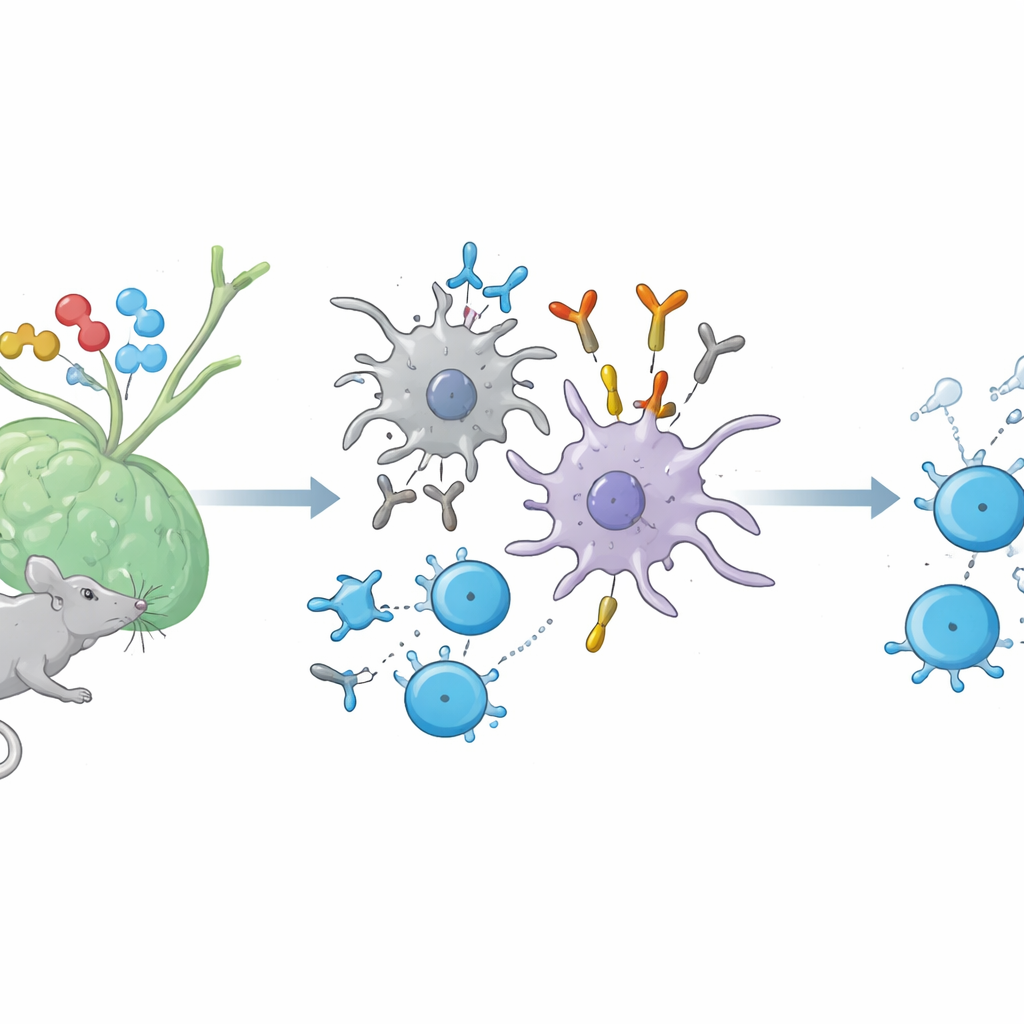
حوار مخفي بين الأجسام المضادة وخلايا T المساعدة
عند تلقيحنا ببروتين، تنشط قوتان رئيسيتان. تنتج خلايا B أجسامًا مضادة ضد البروتين الغريب، بينما تتعرف خلايا T المساعدة على شظايا صغيرة من ذلك البروتين المعروضة على سطح خلايا الجهاز المناعي بواسطة جزيئات تُسمى MHC من الصنف الثاني. حتى الآن، كان العلماء يعتقدون أن الأجسام المضادة التي تتعرف على هذا التركيب المركب «الشظية زائد MHC» — بطريقة تشبه مستقبل خلية T — تظهر فقط في إعدادات مخبرية صناعية. في الفئران، يبيّن المؤلفون أن مثل هذه الأجسام المضادة الشبيهة بمستقبلات الخلايا التائية تتكوّن فعليًا بصورة طبيعية خلال الاستجابات المناعية الاعتيادية لعدة بروتينات، بما في ذلك ليزومايز صفار البيض، وأوفالبيومين، وبروتين غمد عصبي ذي صلة بالتصلب المتعدد.
كيف تُشغّل «ذيول» الببتيد هذه الأجسام المضادة الخاصة
لفهم متى تنشأ هذه الأجسام المضادة الشاذة، قارن الباحثون الاستجابات المناعية لشظايا ببتيدية قصيرة مقابل نسخ أطول قليلًا تحمل «ذيولًا» أمينية عند أحد الطرفين، تُعرف ببقايا المطاوي. كلا النسختين يمكن لجزيئات MHC من الصنف الثاني عرضهما ورؤيتهما من قبل خلايا T، لكنهما يختلفان في مقدار التسلسل الإضافي المتدلي عن الأطراف. وجد الفريق أن الببتيدات التي تحمل مثل هذه البقايا المطاوية فقط هي التي حفّزت بثبات ظهور الأجسام المضادة الجديدة، التي سمّوها أجسامًا مضادة محرضة بالمناعة شبيهة بمستقبلات الخلايا التائية، أو iTabs. لم تقتصر iTabs على التعرّف للببتيد أو لجزيء MHC بمفرده؛ بل تعرّفت على التركيب الثلاثي الأبعاد الدقيق المكوّن من ببتيد محدد، وتمتدته المطاوية، ونوع MHC معيّن — مما يعكس خصوصية دقيقة تشبه خصوصية مستقبل خلية T.
أجهزة كبح الأجسام المضادة على خلايا T المساعدة المفرطة النشاط
بمجرد تواجدها، عملت iTabs كفرامل انتقائية للغاية على خلايا T المساعدة. في تجارب مزروعة خلويا، ارتبطت iTabs بمجمعات الببتيد–MHC ومنعت بروتينات اندماج مستقبلات الخلايا التائية وخلايا T المقرِّبة المبلّغة من الالتحام بأهدافها. كما خفّضت إنتاج IL‑2، وهو إشارة نمو رئيسية للخلايا التائية، وكبتت استجابة تقليدية لتورم الجلد يقودها T في الفئران الحية. كشفت أعمال هيكلية باستخدام الميكروسكوب الإلكتروني بالتبريد عالي الدقة عن السبب: منطقة ارتباط iTab تثبّت على سطح MHC وذيول الببتيد معًا، مكوّنةً توافقًا محكماً يتداخل ماديًا مع وصول الخلايا التائية. بعض iTabs كان بإمكانها أيضًا تعليم خلايا B العارضة للمستضد أن تُدمَّر بواسطة وظائف «الذيل» المعتادة للأجسام المضادة، مضيفةً مسارًا آخر لتهدئة استجابة جارية.
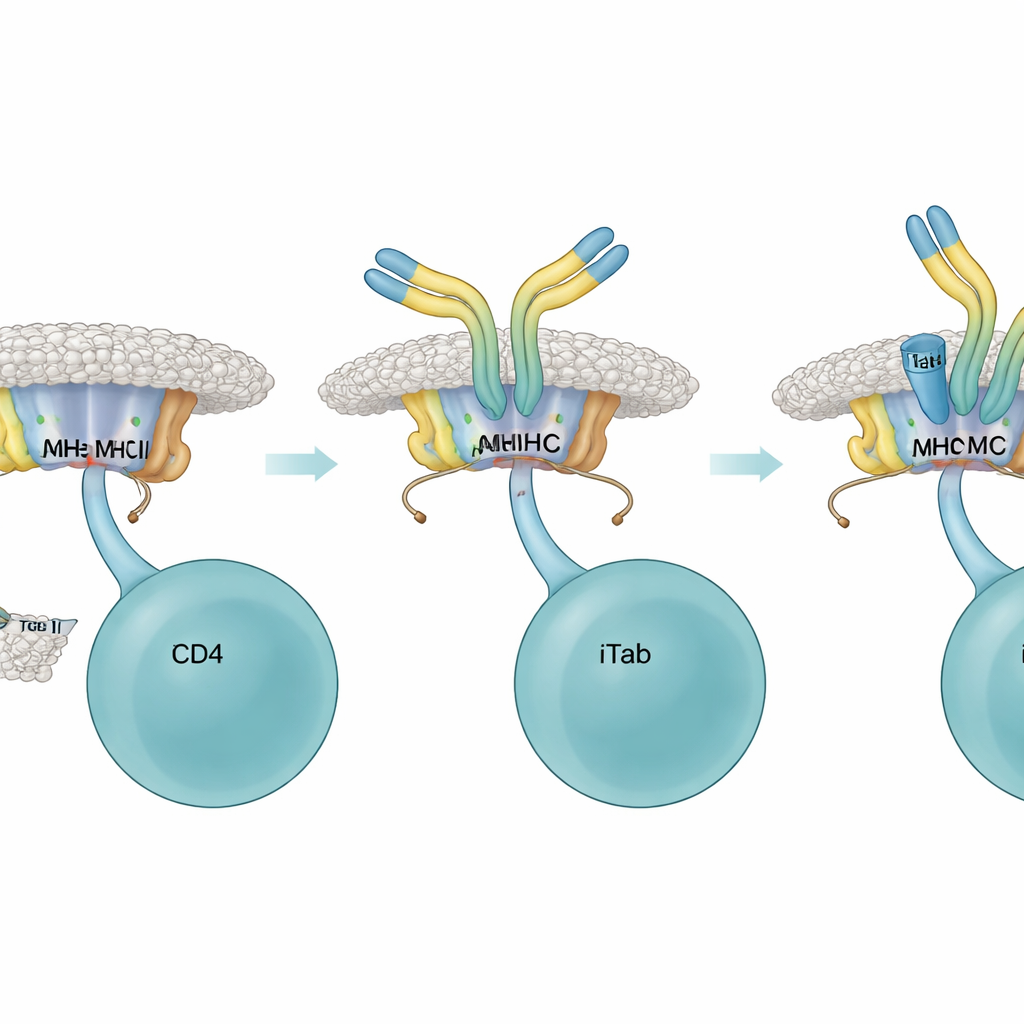
تحويل iTabs إلى أدوات ضد المناعة الذاتية
مسلحين بهذا الفهم، تساءل الباحثون عما إذا كان يمكن تسخير iTabs لكبح خلايا T الذاتية المؤذية في نموذج فأري للتصلب المتعدد يُسمى الاعتلال الدماغي الشوكي التجريبي المناعي الذاتي. صمموا ببتيدات من بروتين المايلين شملت بقايا مطاوية وفي بعض النسخ تغييرات دقيقة تمنع تنشيط خلايا T المسببة للمرض بينما تظل قادرة على تحفيز تكوين iTab. ولّد تلقيح الفئران بهذه الببتيدات المصممة iTabs تعرّفت على مجمعات الببتيد–MHC ذات الصلة بالمرض وعرقلت معظم مستقبلات الخلايا التائية المرضية التي اختُبرت. أدى علاج الفئران بهذه iTabs، أو تحصينها مسبقًا بببتيدات محفزة لـ iTab قبل تحريض المرض، إلى أعراض أخف وتأخر أو انخفاض في تقدم المرض، رغم أن مستويات الأجسام المضادة الكلية ضد الببتيد كانت متشابهة.
ماذا يعني هذا لعينات العلاج الدقيق المستقبلية
بشكل عام، تكشف الدراسة عن iTabs كطبقة تنظيمية طبيعية ومؤقتة للمناعة: أجسام مضادة تحاكي مستقبلات الخلايا التائية، تتشبث بمجمعات الببتيد–MHC التي تتعرف عليها خلايا T المساعدة المعينة، وتخفّف تلك الاستجابات بشكل انتقائي. عن طريق اختيار الببتيدات ذات سلاسل المطاوي الصحيحة بعناية، قد يصبح من الممكن تحفيز iTabs تستهدف خلايا T الذاتية الضارة فقط، مع إبقاء المناعة الواقية سليمة. في حين أن هذه الاكتشافات أجريت في الفئران وأن ترجمتها إلى البشر ستكون معقدة، فهي ترسم مسارًا نحو «فرامل مصممة» لأمراض المناعة الذاتية والحساسية — علاجات لا تعمل عن طريق كبت الجهاز المناعي بصورة عامة، بل عن طريق حجب الحوارات الجزيئية التي تدفع الهجمات غير المرغوب فيها.
الاستشهاد: Kishida, K., Kawakami, K., Tanabe, H. et al. Immune-induced TCR-like antibodies regulate specific T cell response in mice. Nat Commun 17, 3227 (2026). https://doi.org/10.1038/s41467-026-71384-1
الكلمات المفتاحية: الاستجابة الذاتية, خلايا T المساعدة, جزيئات MHC من الصنف الثاني, أجسام مضادة تنظيمية, بواقي المطاوي الببتيدية