Clear Sky Science · it
Anticorpi TCR-simili indotti dal sistema immunitario regolano risposte T specifiche nei topi
Perché alcune risposte immunitarie si attenuano da sole
Il nostro sistema immunitario deve trovare un equilibrio delicato: deve attaccare invasori come virus e batteri, ma evitare di danneggiare i tessuti dell’organismo. Questo articolo rivela una caratteristica autoregolatrice finora trascurata del sistema—anticorpi speciali che riconoscono gli stessi bersagli molecolari di alcuni linfociti T e possono calmarli selettivamente. Comprendere questo freno interno potrebbe aprire strade nuove e molto mirate per trattare le malattie autoimmuni senza indebolire l’immunità in modo generale.
Una conversazione nascosta tra anticorpi e linfociti T helper
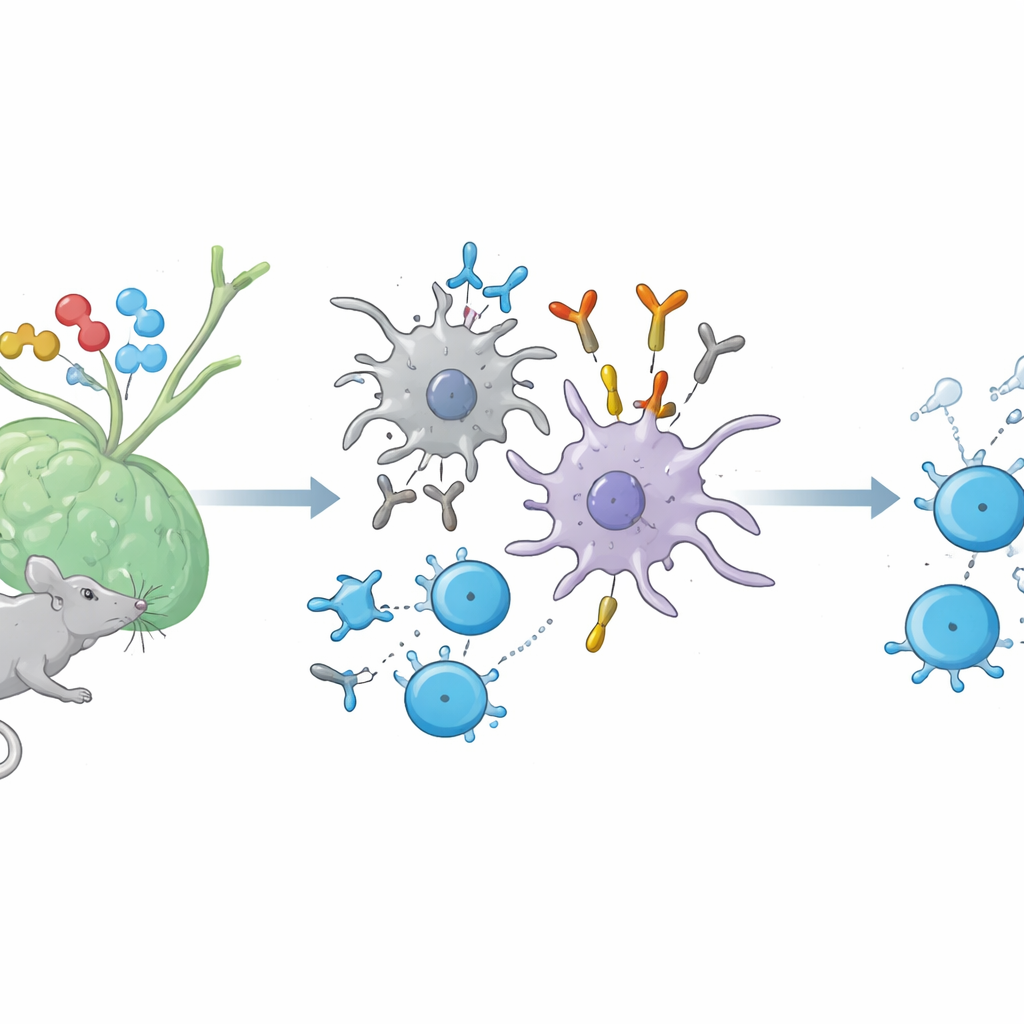
Quando veniamo immunizzati con una proteina, si attivano due forze principali. Le cellule B producono anticorpi contro la proteina estranea, mentre i linfociti T helper riconoscono minuscoli frammenti di quella proteina esposti sulla superficie delle cellule immunitarie da molecole chiamate MHC di classe II. Finora si riteneva che anticorpi in grado di riconoscere questa struttura combinata «frammento più MHC»—in modo simile al recettore delle cellule T—comparissero solo in allestimenti sperimentali artificiali. Nei topi, gli autori dimostrano che tali anticorpi TCR‑simili vengono effettivamente generati in modo naturale durante risposte immunitarie ordinarie a diverse proteine, tra cui la lisozima d’uovo, l’ovalbumina e una proteina della guaina nervosa correlata alla sclerosi multipla.
Come le “code” del peptide attivano questi anticorpi speciali
Per capire quando sorgono questi anticorpi insoliti, i ricercatori hanno confrontato le risposte immunitarie a brevi frammenti peptidici rispetto a versioni leggermente più lunghe che portano alla loro estremità «code» di amminoacidi aggiuntive, note come residui flangia. Entrambe le versioni possono essere presentate dall’MHC di classe II e riconosciute dalle cellule T, ma differiscono per la quantità di sequenza in più che sporge dalle estremità. Il gruppo ha scoperto che solo i peptidi con tali residui flangia inducevano in modo affidabile la comparsa dei nuovi anticorpi, che hanno chiamato anticorpi TCR‑simili indotti dal sistema immunitario, o iTab. Questi iTab non riconoscevano semplicemente il peptide o la molecola MHC da soli; riconoscevano la precisa combinazione tridimensionale di uno specifico peptide, la sua porzione flangia e un particolare tipo di MHC—rispecchiando la fine specificità di un recettore delle cellule T.
Freni anticorpali sui linfociti T helper iperattivi
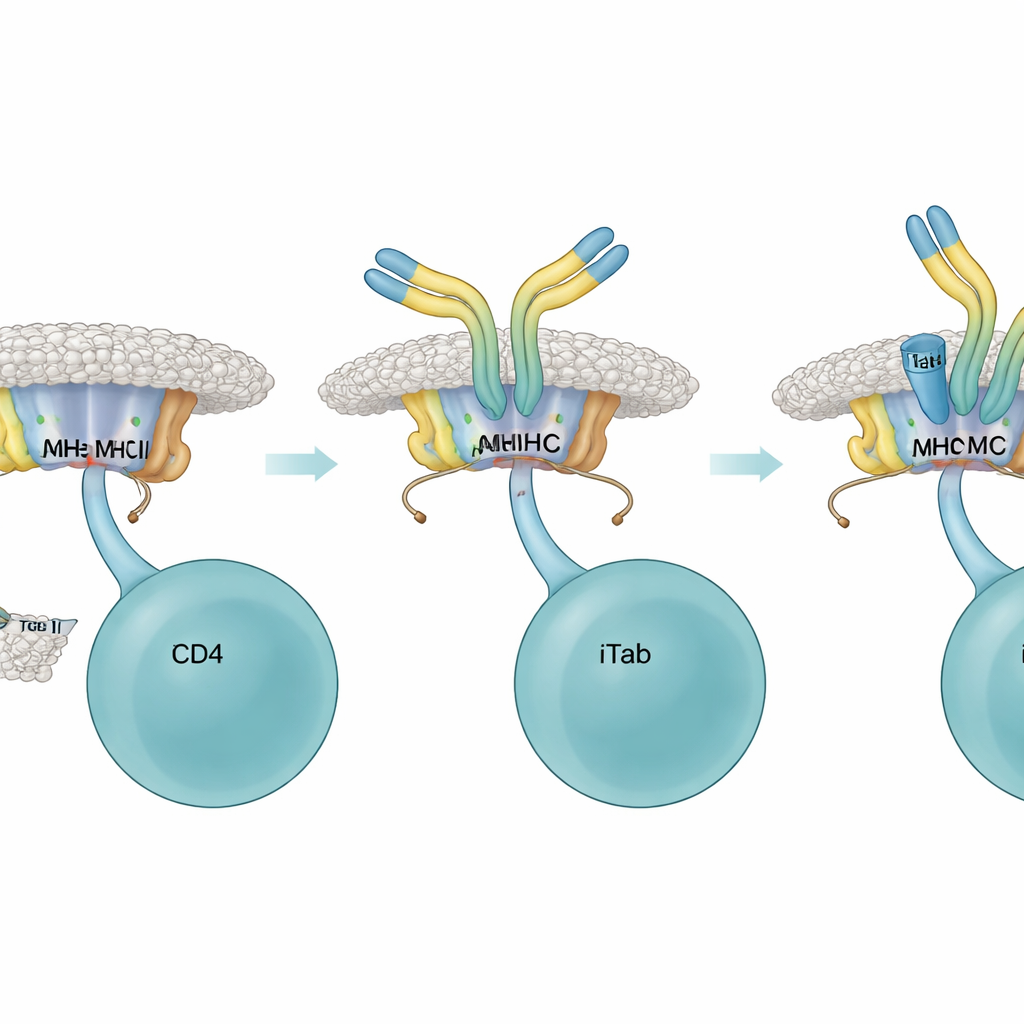
Una volta presenti, gli iTab agivano come freni altamente selettivi sui linfociti T helper. Nei saggi in coltura cellulare, gli iTab si legavano ai complessi peptide–MHC e impedivano a proteine di fusione del recettore T e a linfociti T reporter di ingaggiare i loro bersagli. Riducevano anche la produzione di IL‑2, un segnale chiave per la crescita delle cellule T, e attenuavano una classica reazione di gonfiore cutaneo mediata da cellule T nei topi viventi. Lavori strutturali con microscopia crio‑elettronica ad alta risoluzione hanno spiegato il motivo: la regione di legame di un iTab abbraccia sia la superficie dell’MHC sia la coda del peptide, creando un ancoraggio che interferisce fisicamente con l’accesso delle cellule T. Alcuni iTab potevano anche marcare le cellule B che presentano l’antigene per la distruzione tramite le normali funzioni «tail» degli anticorpi, aggiungendo un ulteriore percorso per attenuare una risposta in corso.
Trasformare gli iTab in strumenti contro l’autoimmunità
Muniti di questa conoscenza, i ricercatori hanno chiesto se gli iTab potessero essere sfruttati per domare i linfociti T autoreattivi dannosi in un modello murino di sclerosi multipla chiamato encefalomielite autoimmune sperimentale. Hanno progettato peptidi derivati da una proteina della mielina che includevano residui flangia e, in alcune versioni, modifiche sottili che impedivano l’attivazione dei linfociti T responsabili della malattia pur consentendo l’induzione degli iTab. Immunizzando i topi con questi peptidi su misura si generarono iTab che riconoscevano complessi peptide–MHC rilevanti per la malattia e bloccavano la maggior parte dei recettori T patogenici testati. Trattare i topi con tali iTab, o pre‑immunizzarli con peptidi che inducono iTab prima dell’innesco della malattia, portò a sintomi più lievi e a un ritardo o riduzione della progressione della patologia, nonostante i livelli complessivi di anticorpi contro il peptide fossero simili.
Cosa significa per terapie di precisione future
Nel complesso, lo studio identifica gli iTab come uno strato naturale e transitorio di regolazione immunitaria: anticorpi che mimano i recettori T, si agganciano ai precisi complessi peptide–MHC riconosciuti da certi linfociti T helper e attenuano selettivamente quelle risposte. Scegliendo con cura peptidi con le giuste sequenze flangia, potrebbe essere possibile indurre deliberatamente iTab che bersagliano solo i linfociti T autoreattivi dannosi, lasciando intatta l’immunità protettiva. Pur essendo riscontri ottenuti nei topi e richiedendo una transizione complessa nell’uomo, questi risultati tracciano un percorso verso «freni su misura» per malattie autoimmuni e allergiche—terapie che non sopprimono l’immunità in modo diffuso, ma bloccano con discrezione le conversazioni molecolari che guidano attacchi indesiderati.
Citazione: Kishida, K., Kawakami, K., Tanabe, H. et al. Immune-induced TCR-like antibodies regulate specific T cell response in mice. Nat Commun 17, 3227 (2026). https://doi.org/10.1038/s41467-026-71384-1
Parole chiave: autoimmunità, linfociti T helper, MHC di classe II, anticorpi regolatori, residui flangia del peptide