Clear Sky Science · fr
Des anticorps de type TCR induits par l’immunité régulent des réponses T spécifiques chez la souris
Pourquoi certaines réponses immunitaires s’atténuent d’elles‑mêmes
Notre système immunitaire doit trouver un équilibre délicat : il doit attaquer les envahisseurs comme les virus et les bactéries, tout en évitant d’endommager les tissus de l’organisme. Cet article révèle un mécanisme d’auto‑régulation jusque‑là négligé au sein de ce système — des anticorps spéciaux qui reconnaissent les mêmes cibles moléculaires que certaines cellules T et sont capables de les calmer sélectivement. Comprendre ce frein intégré pourrait ouvrir des voies nouvelles et très ciblées pour traiter les maladies auto‑immunes sans affaiblir l’immunité de manière générale.
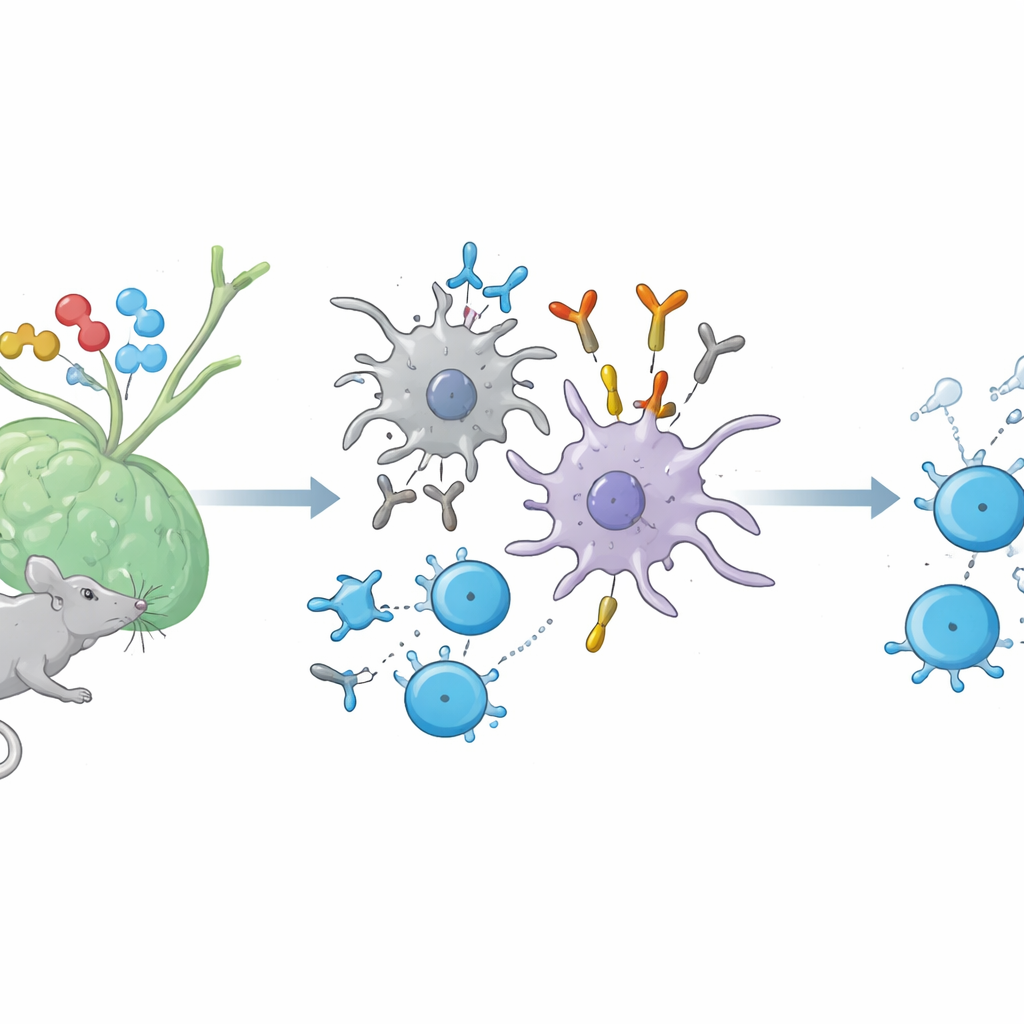
Une conversation cachée entre anticorps et cellules T auxiliaires
Lorsqu’on nous immunise avec une protéine, deux forces majeures entrent en jeu. Les cellules B fabriquent des anticorps dirigés contre la protéine étrangère, tandis que les cellules T auxiliaires reconnaissent de petits fragments de cette protéine présentés à la surface des cellules immunitaires par des molécules appelées CMH de classe II. Jusqu’à présent, on pensait que les anticorps reconnaissant cette structure combinée « fragment plus CMH » — à la manière d’un récepteur de cellule T — n’apparaissaient que dans des conditions expérimentales artificielles. Chez la souris, les auteurs montrent que de tels anticorps de type TCR sont en réalité générés naturellement lors de réponses immunitaires ordinaires à plusieurs protéines, dont la lysozyme d’œuf, l’ovalbumine et une protéine de la gaine nerveuse liée à la sclérose en plaques.
Comment les « queues » peptidiques activent ces anticorps particuliers
Pour comprendre quand ces anticorps inhabituels apparaissent, les chercheurs ont comparé les réponses immunitaires à des peptides courts et à des versions légèrement plus longues portant des « queues » d’acides aminés à une extrémité, appelées résidus d’enchâssement. Les deux versions peuvent être présentées par le CMH de classe II et vues par les cellules T, mais elles diffèrent par la séquence supplémentaire qui dépasse aux extrémités. L’équipe a constaté que seules les peptides munis de ces résidus d’enchâssement déclenchaient de manière fiable l’apparition des nouveaux anticorps, qu’ils ont nommés anticorps de type TCR induits par l’immunité, ou iTabs. Ces iTabs ne reconnaissaient pas simplement le peptide ni la molécule de CMH isolément ; ils reconnaissaient la combinaison tridimensionnelle précise d’un peptide spécifique, de sa portion d’enchâssement et d’un type particulier de CMH — reflétant la spécificité fine d’un récepteur de cellule T.
Des freins anticorps sur les cellules T auxiliaires hyperactives
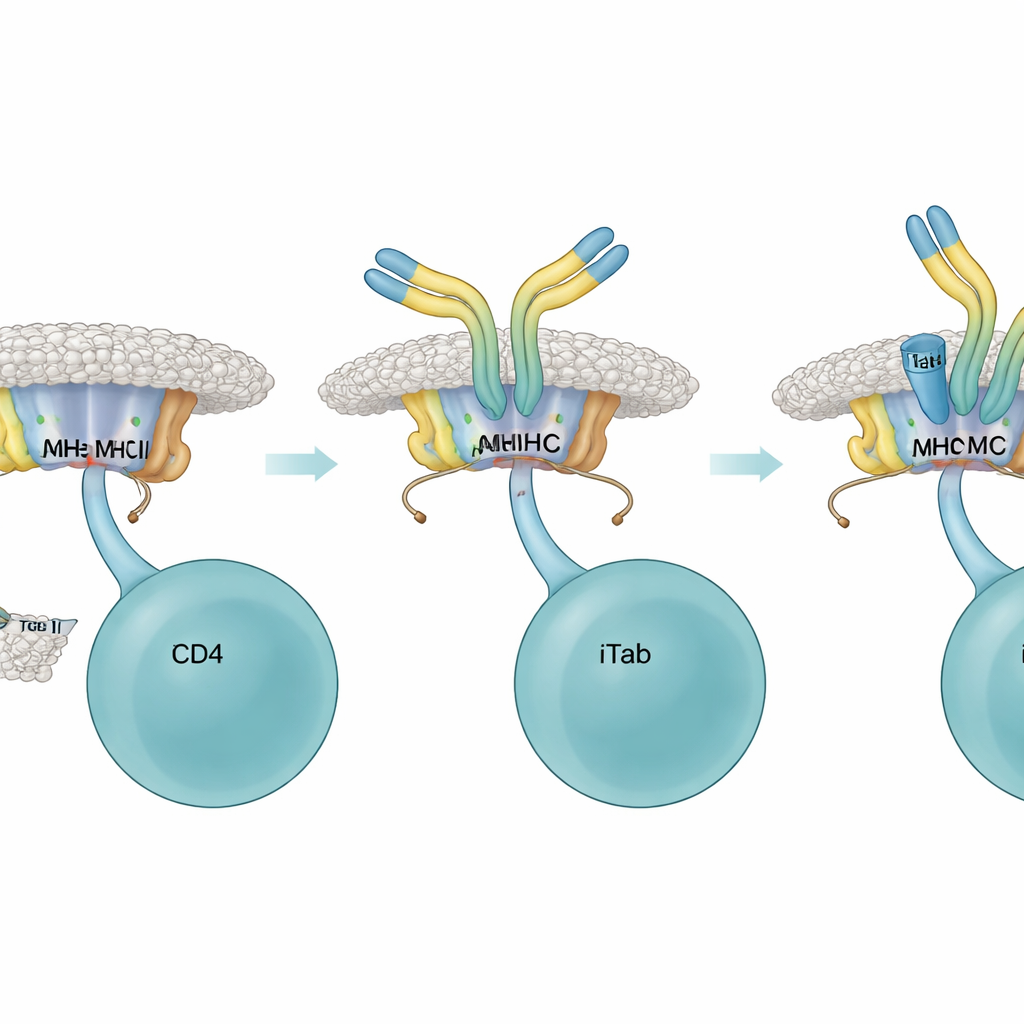
Une fois présents, les iTabs agissaient comme des freins hautement sélectifs sur les cellules T auxiliaires. Dans des essais en culture cellulaire, les iTabs se liaient aux complexes peptide–CMH et empêchaient des protéines de fusion réceptrices de cellules T et des cellules T rapporteurs d’engager leurs cibles. Ils réduisaient également la production d’IL‑2, un signal clé de croissance pour les cellules T, et atténuaient une classique réponse de gonflement cutané dépendante des cellules T chez des souris vivantes. Des études structurales par cryo‑microscopie électronique à haute résolution ont expliqué pourquoi : la zone de liaison d’un iTab s’agrippe à la fois à la surface du CMH et à la « queue » du peptide, créant un ajustement serré qui gêne physiquement l’accès des cellules T. Certains iTabs pouvaient aussi marquer les cellules B présentatrices d’antigène pour destruction via les fonctions effectrices classiques de la « queue » des anticorps, offrant ainsi une autre voie pour calmer une réponse en cours.
Transformer les iTabs en outils contre l’auto‑immunité
Forts de ces connaissances, les chercheurs ont testé si les iTabs pouvaient être exploités pour maîtriser des cellules T auto‑réactives nuisibles dans un modèle murin de sclérose en plaques, l’encéphalomyélite auto‑immune expérimentale. Ils ont conçu des peptides d’une protéine de la myéline incluant des résidus d’enchâssement et, dans certaines versions, des modifications subtiles empêchant l’activation des cellules T pathogènes tout en permettant toujours l’induction d’iTabs. Immuniser les souris avec ces peptides sur mesure générait des iTabs reconnaissant les complexes peptide–CMH pertinents pour la maladie et bloquant la plupart des récepteurs T pathogènes testés. Traiter les souris avec ces iTabs, ou les pré‑immuniser avec des peptides inducteurs d’iTab avant le déclenchement de la maladie, entraînait des symptômes plus bénins et retardait ou réduisait la progression de la maladie, bien que les niveaux globaux d’anticorps dirigés contre le peptide fussent similaires.
Ce que cela signifie pour des thérapies de précision à l’avenir
Dans l’ensemble, l’étude révèle les iTabs comme une couche naturelle et transitoire de régulation immunitaire : des anticorps qui imitent les récepteurs de cellules T, se fixent sur les complexes peptide–CMH exacts reconnus par certaines cellules T auxiliaires et atténuent sélectivement ces réponses. En choisissant soigneusement des peptides avec des séquences d’enchâssement appropriées, il pourrait être possible d’induire délibérément des iTabs ciblant uniquement les cellules T auto‑réactives nuisibles, tout en préservant l’immunité protectrice. Si ces résultats reposent sur des modèles murins et que leur traduction à l’homme sera complexe, ils tracent néanmoins la voie vers des « freins sur mesure » pour les maladies auto‑immunes et allergiques — des traitements qui n’agissent pas en supprimant largement le système immunitaire, mais en bloquant discrètement les conversations moléculaires qui provoquent des attaques indésirables.
Citation: Kishida, K., Kawakami, K., Tanabe, H. et al. Immune-induced TCR-like antibodies regulate specific T cell response in mice. Nat Commun 17, 3227 (2026). https://doi.org/10.1038/s41467-026-71384-1
Mots-clés: auto-immunité, cellules T auxiliaires, CMH de classe II, anticorps régulateurs, résidus d’enchâssement peptidique