Clear Sky Science · de
Immune‑induzierte TCR‑ähnliche Antikörper regulieren spezifische T‑Zell‑Antworten bei Mäusen
Warum sich manche Immunreaktionen von selbst herunterfahren
Unser Immunsystem muss eine feine Balance halten: Es muss Eindringlinge wie Viren und Bakterien angreifen, aber zugleich vermeiden, eigenes Gewebe zu schädigen. Diese Arbeit beschreibt ein zuvor übersehenes Selbstbrems‑Element in diesem System – spezielle Antikörper, die dieselben molekularen Ziele erkennen wie bestimmte T‑Zellen und diese gezielt beruhigen können. Das Verständnis dieser eingebauten Bremse könnte neue, sehr gezielte Behandlungswege für Autoimmunerkrankungen eröffnen, ohne die Immunabwehr insgesamt zu schwächen.
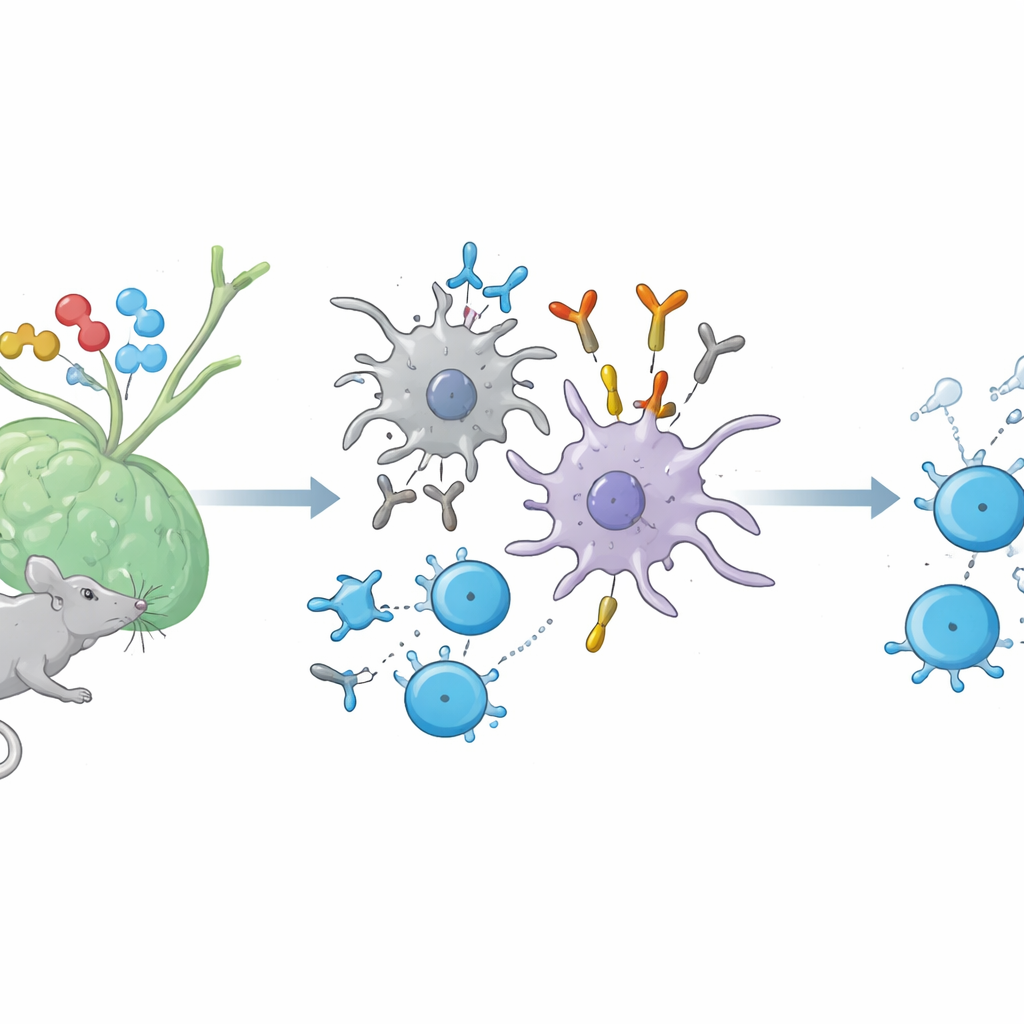
Ein verborgenes Gespräch zwischen Antikörpern und Helfer‑T‑Zellen
Bei einer Impfung mit einem Protein werden zwei Hauptkräfte in Gang gesetzt. B‑Zellen produzieren Antikörper gegen das fremde Protein, während Helfer‑T‑Zellen winzige Fragmente dieses Proteins erkennen, die von MHC‑Klasse‑II‑Molekülen auf der Oberfläche von Immunzellen präsentiert werden. Bislang ging man davon aus, dass Antikörper, die diese kombinierte „Fragment plus MHC“‑Struktur erkennen – ähnlich wie ein T‑Zell‑Rezeptor – nur in künstlichen Laborbedingungen auftauchen. Die Autoren zeigen jedoch, dass solche TCR‑ähnlichen Antikörper bei Mäusen tatsächlich während gewöhnlicher Immunantworten gegen mehrere Proteine natürlich entstehen, darunter Hühnerei‑Lysozym, Ovalbumin und ein Nervenhaut‑Protein, das mit Multipler Sklerose in Verbindung steht.
Wie Peptid‑„Schwänze“ diese speziellen Antikörper einschalten
Um zu verstehen, wann diese ungewöhnlichen Antikörper entstehen, verglichen die Forscher Immunantworten auf kurze Peptid‑Fragmente mit etwas längeren Versionen, die an einem Ende zusätzliche Aminosäure‑„Schwänze“ tragen, genannt flankierende Reste. Beide Versionen können von MHC‑Klasse‑II präsentiert und von T‑Zellen gesehen werden, unterscheiden sich jedoch darin, wie viel zusätzliche Sequenz über die Enden hinausragt. Das Team fand, dass nur Peptide mit solchen flankierenden Resten verlässlich das Auftreten der neuen Antikörper auslösten, die sie immune‑induzierte TCR‑ähnliche Antikörper oder iTabs nannten. Diese iTabs erkannten nicht einfach das Peptid oder das MHC‑Molekül allein; sie erkannten die präzise dreidimensionale Kombination aus einem spezifischen Peptid, dessen flankierendem Abschnitt und einem bestimmten MHC‑Typ – und spiegelten damit die feine Spezifität eines T‑Zell‑Rezeptors wider.
Antikörperbremsen gegen überaktive Helfer‑T‑Zellen
Einmal vorhanden wirkten iTabs als hochselektive Bremsen auf Helfer‑T‑Zellen. In Zellkultur‑Assays banden iTabs an Peptid–MHC‑Komplexe und verhinderten, dass Fusionsproteine von T‑Zell‑Rezeptoren und Reporter‑T‑Zellen ihre Ziele erreichen. Sie reduzierten außerdem die Produktion von IL‑2, einem wichtigen Wachstums‑Signal für T‑Zellen, und dämpften eine klassische T‑Zell‑vermittelte Hautschwellungsreaktion in lebenden Mäusen. Strukturarbeiten mittels hochauflösender Kryo‑Elektronenmikroskopie zeigten, warum: Die Bindungsregion eines iTab klammert sich sowohl an die MHC‑Oberfläche als auch an den Peptid‑Schwanz, wodurch eine enge Passung entsteht, die physisch den Zugang von T‑Zellen behindert. Einige iTabs konnten antigenpräsentierende B‑Zellen zudem durch die üblichen Antikörper‑„Schwanz“‑Funktionen zur Zerstörung markieren und boten so einen zusätzlichen Weg, eine laufende Antwort zu beruhigen.
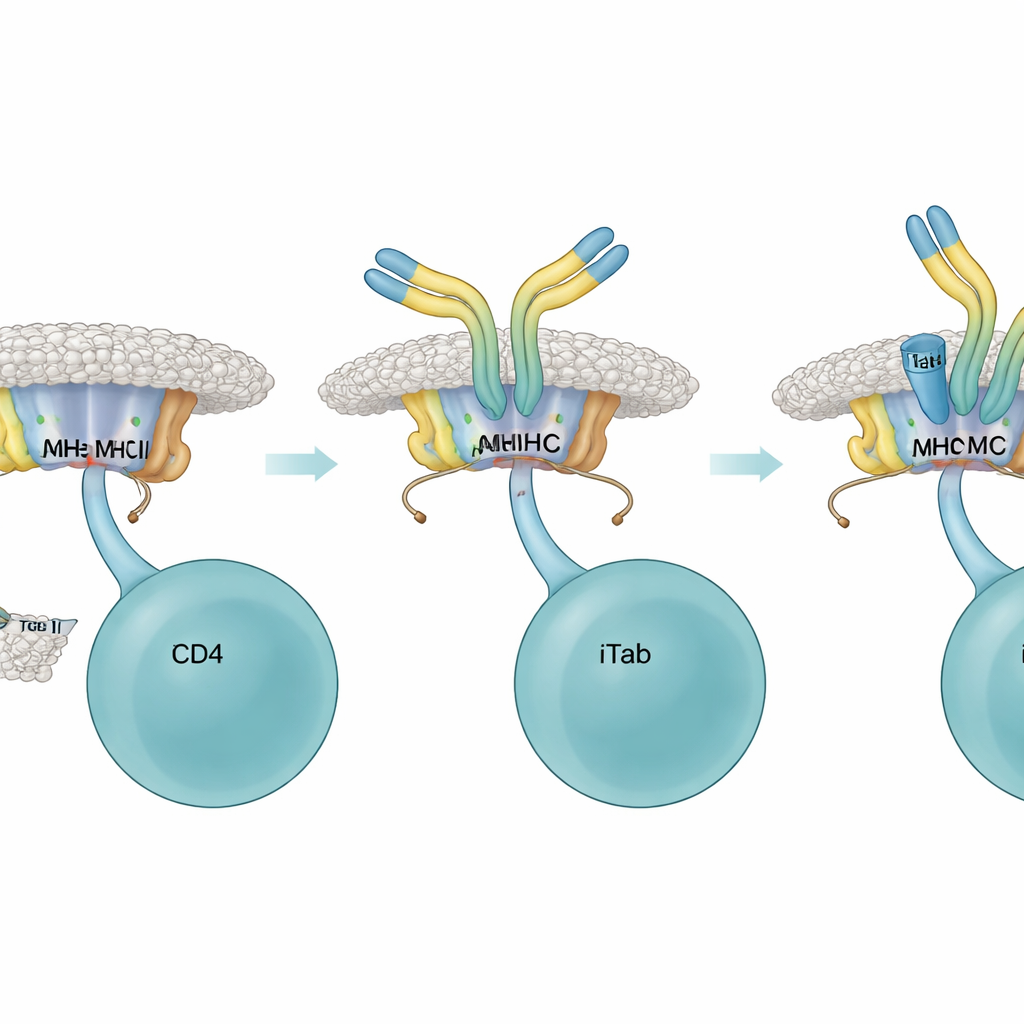
iTabs als Werkzeuge gegen Autoimmunität
Mit diesem Wissen fragten die Forscher, ob iTabs genutzt werden könnten, um schädliche selbstreaktive T‑Zellen in einem Mausmodell der Multiplen Sklerose, der experimentellen autoimmunen Enzephalomyelitis, zu zähmen. Sie entwarfen Peptide aus einem Myelinprotein, die flankierende Reste enthielten und in einigen Varianten subtile Änderungen, die verhindern, dass krankheitsverursachende T‑Zellen aktiviert werden, aber dennoch die Induktion von iTabs erlauben. Das Immunisieren von Mäusen mit diesen maßgeschneiderten Peptiden erzeugte iTabs, die krankheitsrelevante Peptid–MHC‑Komplexe erkannten und die Mehrheit der getesteten pathogenen T‑Zell‑Rezeptoren blockierten. Die Behandlung von Mäusen mit solchen iTabs oder eine Vorimmunisierung mit iTab‑induzierenden Peptiden vor Auslösung der Krankheit führte zu milderen Symptomen und verzögerter bzw. verringerter Krankheitsprogression, obwohl die gesamten Antikörperwerte gegen das Peptid ähnlich blieben.
Was das für zukünftige präzise Therapien bedeutet
Insgesamt deckt die Studie iTabs als eine natürliche, vorübergehende Ebene der Immunregulation auf: Antikörper, die T‑Zell‑Rezeptoren nachahmen, sich an genau die Peptid–MHC‑Komplexe hängen, die bestimmte Helfer‑T‑Zellen erkennen, und diese Antworten selektiv abschwächen. Durch die gezielte Auswahl von Peptiden mit passenden flankierenden Sequenzen könnte man iTabs bewusst induzieren, die nur schädliche autoreaktive T‑Zellen adressieren, während schützende Immunität erhalten bleibt. Zwar wurden diese Befunde in Mäusen gewonnen und die Übertragung auf den Menschen wird komplex sein, doch skizzieren sie einen Weg zu „Designer‑Bremsen“ für Autoimmun‑ und Allergieerkrankungen – Therapien, die nicht durch unspezifische Immunsuppression wirken, sondern die molekularen Unterhaltungen blockieren, die unerwünschte Angriffe antreiben.
Zitation: Kishida, K., Kawakami, K., Tanabe, H. et al. Immune-induced TCR-like antibodies regulate specific T cell response in mice. Nat Commun 17, 3227 (2026). https://doi.org/10.1038/s41467-026-71384-1
Schlüsselwörter: Autoimmunität, Helfer‑T‑Zellen, MHC Klasse II, regulatorische Antikörper, peptid‑flankierende Reste