Clear Sky Science · it
L’efferocitosi dei macrofagi promuove la risoluzione dell’infiammazione e accelera la guarigione delle ferite
Perché il nostro corpo fatica a chiudere ferite ostinate
Le ferite cutanee croniche, come le ulcere del piede diabetico, possono perdurare per mesi, causando dolore, infezioni e talvolta amputazioni. Questo articolo di revisione spiega perché alcune ferite si rifiutano di guarire e mette in luce un lavoro di pulizia poco noto svolto da cellule immunitarie chiamate macrofagi. Quando questa pulizia viene a mancare, l’infiammazione brucia lentamente invece di spegnersi, e la pelle non riesce a ricostruirsi correttamente. Comprendere e potenziare questo sistema naturale di smaltimento potrebbe portare a nuove terapie meno invasive per ferite difficili da guarire.
Il ritmo normale della riparazione delle ferite
La riparazione cutanea sana si svolge in quattro fasi sovrapposte: arresto del sanguinamento, pulizia del danno, crescita di nuovo tessuto e rimodellamento della cicatrice. Immediatamente dopo la lesione, i vasi sanguigni si contraggono e si forma un coagulo che funge sia da tappo sia da impalcatura. Poco dopo, un’ondata di cellule immunitarie invade l’area. I primi a intervenire, i neutrofili, uccidono i microrganismi invasori e digeriscono i detriti. A loro seguono i monociti che maturano in macrofagi, i quali adattano il loro comportamento nel tempo: inizialmente sono infiammatori e orientati all’attacco, più avanti diventano calmanti e focalizzati sulla riparazione. Quando il pericolo passa, le cellule della pelle, dei vasi sanguigni e del tessuto connettivo proliferano e migrano per chiudere il gap, mentre le fibre di collagene vengono gradualmente riorganizzate per conferire forza al nuovo tessuto.
Quando la pulizia fallisce e le ferite si bloccano
Nel diabete, nell’invecchiamento, nei danni da radiazioni e in altre condizioni croniche, le ferite spesso si arrestano nella fase infiammatoria. L’elevata glicemia, lo stress ossidativo persistente e i segnali di pericolo derivanti da molecole danneggiate alterano la maturazione e il comportamento dei macrofagi. Invece di passare a una modalità di riparazione, queste cellule restano bloccate in uno stato pro-infiammatorio e si accumulano nel sito della ferita. Allo stesso tempo si indebolisce la loro capacità di inglobare e digerire le cellule morenti. Di conseguenza, neutrofili morti e morenti si accumulano, possono rompersi e rilasciare contenuti irritanti. Ulteriori strutture a rete rilasciate dai neutrofili e un’ondata di molecole infiammatorie avvelenano ulteriormente l’ambiente locale. La ferita entra in un circolo vizioso: l’infiammazione persistente impedisce una corretta ricostruzione del tessuto, che a sua volta genera più danno cellulare e infiammazione.
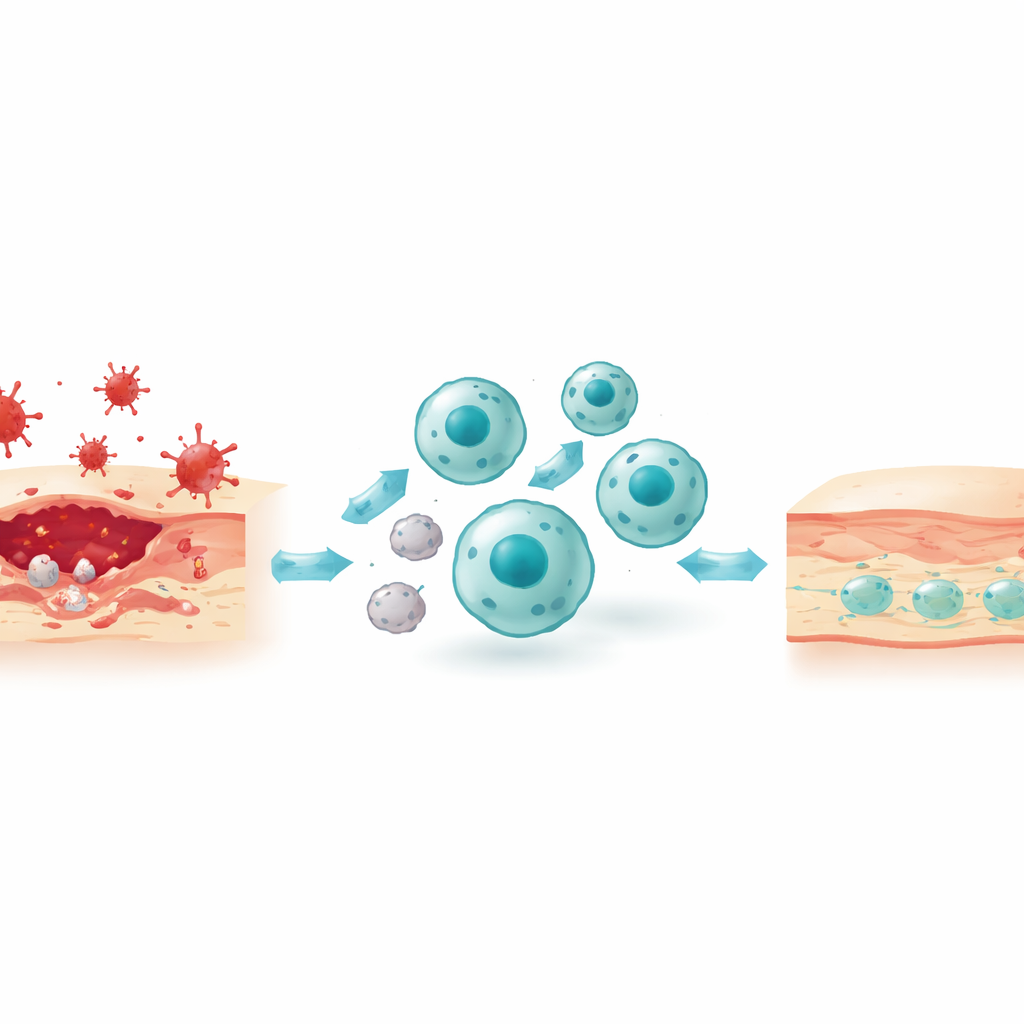
Il processo nascosto della pulizia cellulare
Un tema centrale del lavoro è l’efferocitosi, la rimozione programmata delle cellule morenti da parte dei macrofagi. Non è un semplice atto di inghiottire in un unico passaggio. Innanzitutto, le cellule apoptotiche (programmate per morire) emettono segnali «venitemi a cercare» come lipidi e nucleotidi che attirano i macrofagi. Queste cellule morenti espongono inoltre specifici lipidi sulla loro superficie esterna come segnali «mangiate-mi», riconosciuti direttamente da recettori sui macrofagi o indirettamente attraverso proteine «ponte» presenti nel fluido circostante. Poi il macrofago rimodella il suo scheletro di actina per avvolgere e internalizzare il bersaglio, formando una bolla sigillata che poi si fonde con sacchi ricchi di enzimi per la digestione. I prodotti della degradazione — lipidi, amminoacidi, nucleotidi — vengono poi riciclati o esportati e nel processo rimodellano il metabolismo del macrofago verso uno stato più calmo e pro-risolutivo che rilascia mediatori anti-infiammatori e fattori di crescita.
Come una migliore efferocitosi può salvare le ferite croniche
Gli autori passano in rassegna una vasta gamma di interruttori molecolari che possono migliorare l’efferocitosi e quindi calmare l’infiammazione cronica. Alcune strategie potenziano il riconoscimento precoce, ad esempio aumentando i segnali che attirano i macrofagi o stabilizzando i segnali «mangiate-mi» sulle cellule morenti. Altre si concentrano sul preservare o ripristinare recettori chiave dei macrofagi che spesso vengono frammentati o down-regolati nelle malattie croniche, oppure sul fornire molecole ponte che collegano le cellule morenti a questi recettori. Approcci aggiuntivi agiscono più in profondità all’interno della cellula, spingendo il sistema energetico verso la glicolisi, regolando il trattamento del colesterolo e degli amminoacidi, o migliorando la fusione delle vescicole di ingestione con i lisosomi. Mediatori lipidici specializzati derivati dagli omega-3 formano anche un circuito di retroazione positiva: vengono prodotti durante l’efferocitosi, ne aumentano ulteriormente l’efficacia e aiutano a risolvere l’infiammazione. Nel loro insieme, questi meccanismi mostrano che migliorare la pulizia cellulare non è semplicemente smaltire rifiuti; riprogramma attivamente i macrofagi per sostenere la crescita vascolare, il rimodellamento della matrice e una riparazione tissutale ordinata.
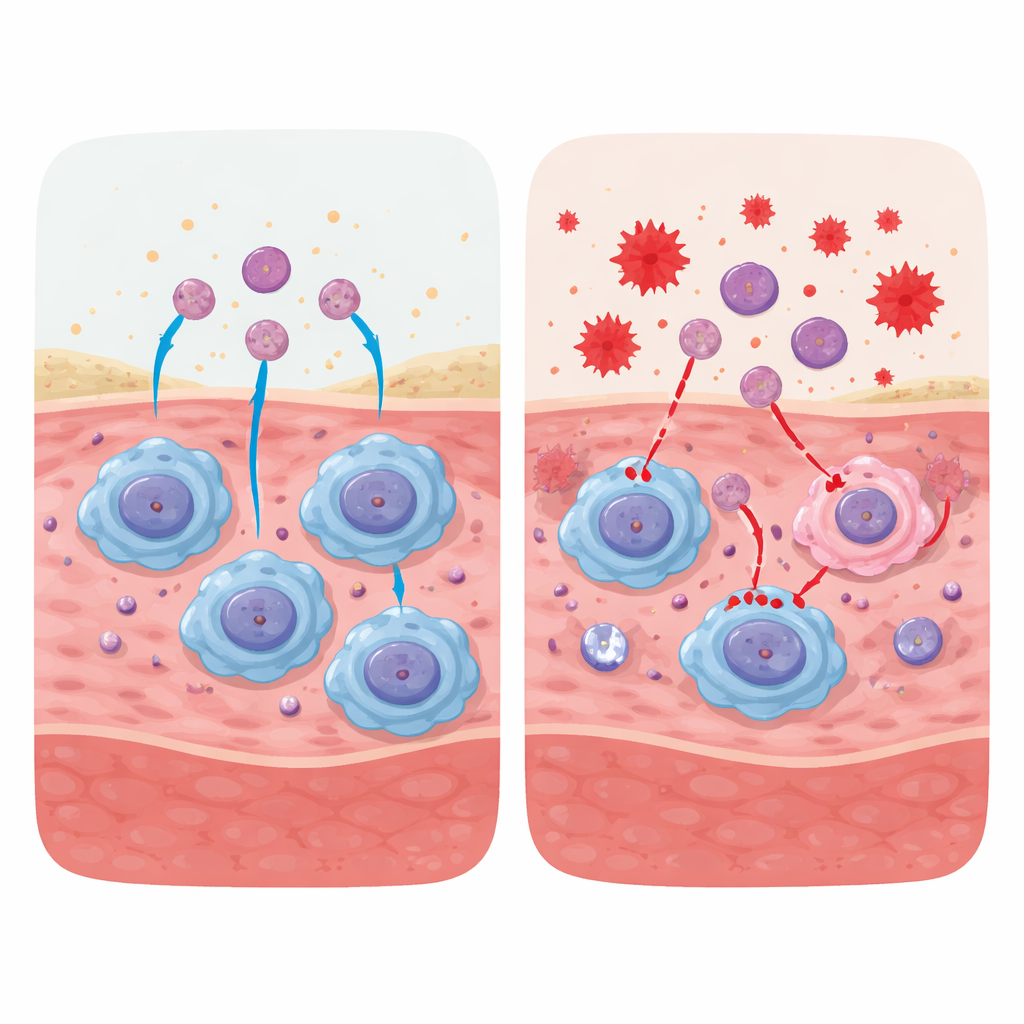
Nuove idee terapeutiche: aiutare gli aiutanti
Oltre a farmaci e biomolecole, la revisione evidenzia terapie emergenti basate su cellule e materiali. L’infusione delle cellule mononucleate del sangue periferico del paziente nelle ferite che non guariscono può rifornire monociti che maturano in macrofagi riparativi, ristabilendo l’equilibrio tra le fasi infiammatoria e di guarigione. Biomateriali intelligenti e medicazioni possono essere progettati per rilasciare segnali che potenziano l’efferocitosi, fattori di crescita o composti antiossidanti direttamente nel letto di ferita. Gli autori discutono inoltre come il targeting dei mitocondri, il controllo delle eccessive strutture neutrofiliche e la gestione della senescenza cellulare possano convergere tutti sul migliorare la funzione dei macrofagi.
Cosa significa per i pazienti con ferite difficili da guarire
L’articolo conclude che la mancata pulizia cellulare è un filo comune che collega molti tipi di ferite croniche. L’efferocitosi dei macrofagi funziona come un interruttore maestro: quando opera correttamente, l’infiammazione viene spenta al momento giusto e la ferita procede alla ricostruzione; quando fallisce, il tessuto rimane intrappolato in un limbo dannoso. Progettando terapie che ripristinino o amplifichino questa pulizia naturale — tramite molecole, cellule o materiali intelligenti — i clinici potrebbero ridurre i tempi di guarigione, diminuire le complicanze e migliorare la qualità della vita delle persone con ferite cutanee ostinate.
Citazione: Gao, J., Zhu, D., Wang, J. et al. Macrophage efferocytosis promotes inflammation resolution and accelerates wound healing. Commun Biol 9, 613 (2026). https://doi.org/10.1038/s42003-026-10107-0
Parole chiave: guarigione delle ferite, macrofagi, infiammazione, ulcere del piede diabetico, efferocitosi