Clear Sky Science · de
Die Efferozytose von Makrophagen fördert die Auflösung von Entzündungen und beschleunigt die Wundheilung
Warum unser Körper Schwierigkeiten hat, hartnäckige Wunden zu schließen
Chronische Hautwunden, etwa diabetische Fußgeschwüre, können monatelang bestehen bleiben, Schmerzen, Infektionen und sogar Amputationen verursachen. Dieser Übersichtsartikel erklärt, warum einige Wunden nicht heilen wollen, und rückt eine wenig bekannte Aufräumarbeit von Immunzellen, den Makrophagen, in den Mittelpunkt. Wenn dieses Aufräumen versagt, glimmt die Entzündung weiter, statt abzuschalten, und die Haut kann sich nicht richtig wiederaufbauen. Das Verständnis und die Stärkung dieses natürlichen Reinigungssystems könnten zu neuen, weniger invasiven Therapien für schlecht heilende Wunden führen.
Der normale Rhythmus der Wundheilung
Die gesunde Hautreparatur verläuft in vier sich überlappenden Phasen: Blutstillung, Beseitigung von Schäden, Neubildung von Gewebe und Umbau der Narbe. Unmittelbar nach der Verletzung ziehen sich Blutgefäße zusammen und ein Pfropf bildet sich, der als Verschluss und Gerüst dient. Kurz darauf strömt eine Welle von Immunzellen herbei. Ersteinsatzkräfte, die Neutrophilen, töten eindringende Mikroben und bauen Trümmer ab. Sie werden von Monozyten gefolgt, die zu Makrophagen heranreifen und ihr Verhalten im Zeitverlauf anpassen: zu Beginn sind sie kampfbeteiligt und entzündungsfördernd, später werden sie beruhigend und reparaturorientiert. Sobald die Gefahr vorüber ist, proliferieren und migrieren Haut-, Gefäß- und Bindegewebszellen, um die Lücke zu schließen, während Kollagenfasern schrittweise umorganisiert werden, damit das neue Gewebe Festigkeit erhält.
Wenn das Aufräumen scheitert und Wunden stecken bleiben
Bei Diabetes, Alter, Strahlenschäden und anderen chronischen Zuständen bleiben Wunden häufig in der entzündlichen Phase stecken. Hoher Blutzucker, anhaltender oxidativer Stress und Gefahrensignale aus beschädigten Molekülen stören, wie Makrophagen reifen und sich verhalten. Statt in einen Reparaturmodus umzuschalten, bleiben diese Zellen in einem pro-inflammatorischen Zustand gefangen und sammeln sich an der Wundstelle an. Gleichzeitig ist ihre Fähigkeit, sterbende Zellen aufzunehmen und zu verdauen, geschwächt. Infolgedessen häufen sich tote und sterbende Neutrophile an, können aufplatzen und reizende Inhalte freisetzen. Zusätzliche netzartige Strukturen von Neutrophilen und ein Strom entzündlicher Moleküle vergiften weiter die lokale Umgebung. Die Wunde gerät in einen Teufelskreis: anhaltende Entzündung verhindert einen ordnungsgemäßen Gewebeaufbau, was wiederum zu mehr Zellschäden und Entzündung führt.
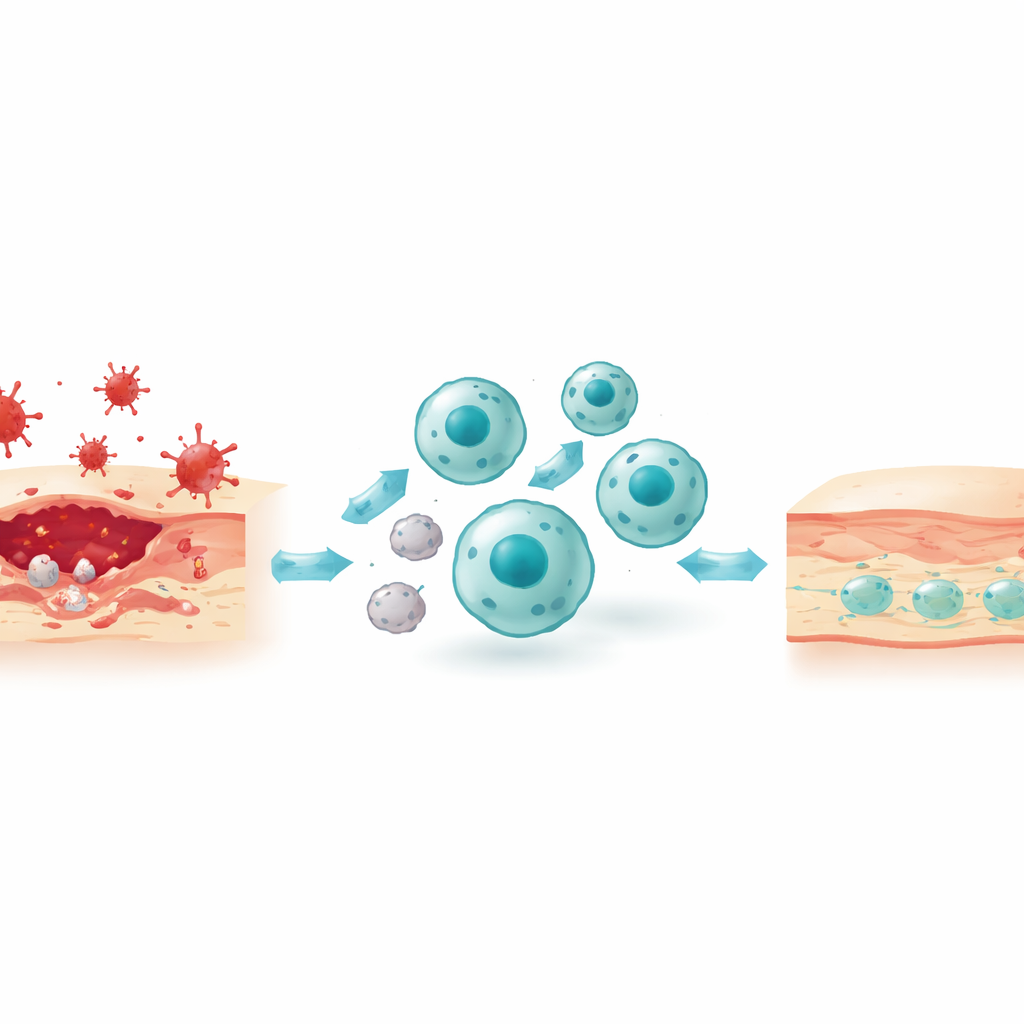
Der verborgene Prozess der zellulären Hausarbeit
Ein zentrales Thema des Papiers ist die Efferozytose, die programmierte Beseitigung sterbender Zellen durch Makrophagen. Das ist kein einfacher, einstufiger Vorgang. Zuerst senden apoptotische (programmierter Tod) Zellen „Find-me“-Signale wie Lipide und Nukleotide aus, die Makrophagen anlocken. Diese sterbenden Zellen drehen zudem bestimmte Lipide auf ihre Außenseite, um als „Eat-me“-Markierungen zu fungieren, die entweder direkt von Rezeptoren auf Makrophagen erkannt oder indirekt über „Brücken“-Proteine in der umgebenden Flüssigkeit vermittelt werden. Anschließend formt der Makrophage sein Aktin-Zytoskelett um, um das Ziel zu umschließen und zu internalisieren, wobei eine verschlossene Blase entsteht, die später mit enzymgefüllten Vesikeln zur Verdauung fusioniert. Die Abbauprodukte – Fette, Aminosäuren, Nukleotide – werden dann recycelt oder exportiert und steuern dabei den Stoffwechsel des Makrophagen in Richtung eines ruhigeren, pro-resolvierenden Zustands, der antiinflammatorische Mediatoren und Wachstumsfaktoren freisetzt.
Wie bessere Efferozytose chronische Wunden retten kann
Die Autor*innen untersuchen eine breite Palette molekularer Schalter, die die Efferozytose verbessern und damit chronische Entzündung dämpfen können. Einige Strategien verstärken die frühe Erkennung, etwa durch Erhöhung der Signale, die Makrophagen anziehen, oder durch Stabilisierung der „Eat-me“-Markierungen auf sterbenden Zellen. Andere zielen darauf ab, Schlüsselrezeptoren auf Makrophagen zu erhalten beziehungsweise wiederherzustellen, die bei chronischen Erkrankungen oft geschnitten oder herunterreguliert sind, oder Brückenmoleküle bereitzustellen, die sterbende Zellen mit diesen Rezeptoren verbinden. Weitere Ansätze wirken tiefer in der Zelle, indem sie das Energiesystem in Richtung Glykolyse lenken, den Umgang mit Cholesterin und Aminosäuren feinjustieren oder die Fusion von Aufnahmevesikeln mit Lysosomen verbessern. Spezialisierte Lipidmediatoren, abgeleitet von Omega‑3‑Fettsäuren, bilden ebenfalls eine positive Rückkopplung: Sie werden während der Efferozytose produziert, verstärken dieses Aufräumen weiter und helfen bei der Auflösung von Entzündungen. Zusammengenommen zeigen diese Mechanismen, dass die Verbesserung der Zellbeseitigung nicht nur Müllentsorgung ist; sie programmiert Makrophagen aktiv um, um Gefäßwachstum, Matrixumbau und geordnete Gewebereparatur zu unterstützen.
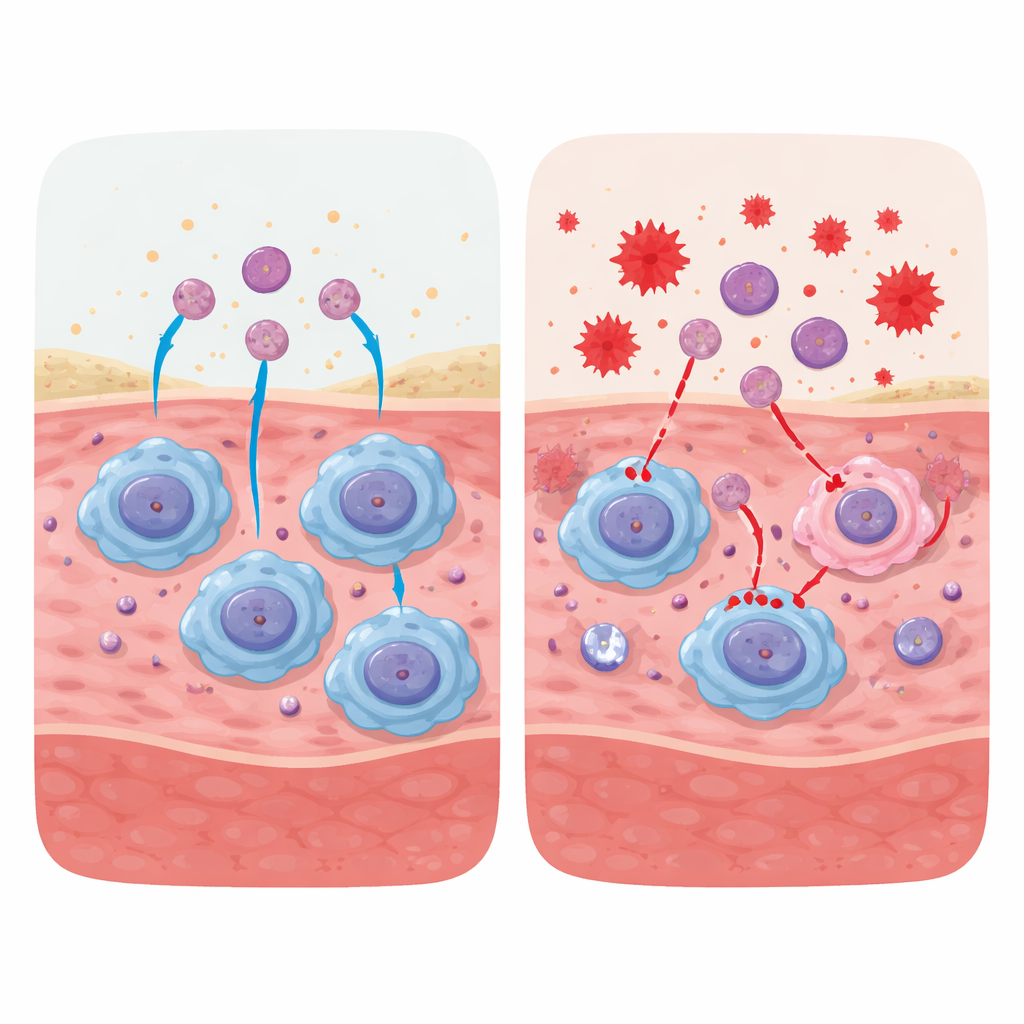
Neue Therapieideen: den Helfern helfen
Über Medikamente und Biomoleküle hinaus hebt die Übersicht aufkommende zellbasierte und materialbasierte Therapien hervor. Die Infusion eigener peripherer mononukleärer Blutzellen in nicht heilende Wunden kann Monozyten auffüllen, die zu reparativen Makrophagen heranreifen und das Gleichgewicht zwischen Entzündungs- und Heilungsphase wiederherstellen. Intelligente Biomaterialien und Verbände können so konstruiert werden, dass sie Efferozytose-fördernde Signale, Wachstumsfaktoren oder antioxidative Verbindungen direkt in das Wundbett liefern. Die Autor*innen diskutieren auch, wie das Ansteuern der Mitochondrien, das Eindämmen übermäßiger Neutrophilen‑Netzwerke und das Management zellulärer Seneszenz alle auf die Verbesserung der Makrophagenfunktion hinauslaufen können.
Was das für Patientinnen und Patienten mit schwer heilenden Wunden bedeutet
Der Artikel schließt mit der Feststellung, dass fehlgeschlagenes zelluläres Aufräumen ein gemeinsamer Faden ist, der viele Arten chronischer Wunden verbindet. Die Efferozytose der Makrophagen wirkt als Hauptschalter: Wenn sie funktioniert, wird die Entzündung zur richtigen Zeit ausgeschaltet und die Wunde gelangt in die Aufbauphase; wenn sie versagt, bleibt das Gewebe in einem schädlichen Limbus gefangen. Durch die Entwicklung von Therapien, die dieses natürliche Aufräumen wiederherstellen oder verstärken – sei es durch Moleküle, Zellen oder intelligente Materialien – könnten Kliniker die Heilungszeiten verkürzen, Komplikationen reduzieren und die Lebensqualität von Menschen mit hartnäckigen Hautwunden verbessern.
Zitation: Gao, J., Zhu, D., Wang, J. et al. Macrophage efferocytosis promotes inflammation resolution and accelerates wound healing. Commun Biol 9, 613 (2026). https://doi.org/10.1038/s42003-026-10107-0
Schlüsselwörter: Wundheilung, Makrophagen, Entzündung, diabetische Fußgeschwüre, Efferozytose