Clear Sky Science · fr
Les macrophages et l’efferocytose favorisent la résolution de l’inflammation et accélèrent la cicatrisation
Pourquoi notre corps peine à refermer des plaies rebelles
Les plaies cutanées chroniques, comme les ulcères du pied chez les personnes diabétiques, peuvent persister des mois durant, provoquant douleur, infections et parfois des amputations. Cet article de synthèse explique pourquoi certaines plaies refusent de guérir et met en lumière un rôle méconnu de nettoyage assuré par des cellules immunitaires appelées macrophages. Quand ce nettoyage fait défaut, l’inflammation couve au lieu de s’éteindre, et la peau ne peut pas se reconstruire correctement. Comprendre et renforcer ce système naturel d’élimination pourrait conduire à de nouveaux traitements moins invasifs pour les plaies difficiles à cicatriser.
Le rythme normal de la réparation des plaies
La réparation cutanée saine se déroule en quatre étapes qui se chevauchent : arrêter le saignement, nettoyer les lésions, former un nouveau tissu et remodeler la cicatrice. Immédiatement après la blessure, les vaisseaux sanguins se contractent et un caillot se forme, jouant à la fois le rôle de bouchon et d’échafaudage. Rapidement, une vague de cellules immunitaires afflue. Les neutrophiles, premiers intervenants, tuent les microbes envahisseurs et digèrent les débris. Ils sont suivis par des monocytes qui maturent en macrophages, lesquels adaptent leur comportement au fil du temps : au début, ils sont pro-inflammatoires et agressifs, puis ils deviennent apaisants et orientés vers la réparation. Quand le danger diminue, les kératinocytes, les cellules endothéliales et les cellules du tissu conjonctif prolifèrent et migrent pour refermer la lésion, tandis que les fibres de collagène sont progressivement réorganisées pour donner de la résistance au nouveau tissu.
Quand le nettoyage échoue et que les plaies s’enlisent
Dans le diabète, le vieillissement, les lésions par radiation et d’autres affections chroniques, les plaies restent souvent bloquées au stade inflammatoire. L’hyperglycémie, le stress oxydatif persistant et les signaux de danger issus de molécules endommagées perturbent la maturation et le comportement des macrophages. Au lieu de basculer vers un mode réparation, ces cellules restent figées dans un état pro-inflammatoire et s’accumulent sur le site de la plaie. Parallèlement, leur capacité à engloutir et digérer les cellules mourantes est affaiblie. En conséquence, des neutrophiles morts ou mourants s’accumulent, peuvent se rompre et répandre des contenus irritants. Des structures filamenteuses supplémentaires provenant des neutrophiles et un flot de molécules inflammatoires empoisonnent davantage l’environnement local. La plaie entre dans un cercle vicieux : l’inflammation persistante empêche la reconstitution correcte des tissus, ce qui génère à son tour davantage de dommages cellulaires et d’inflammation.
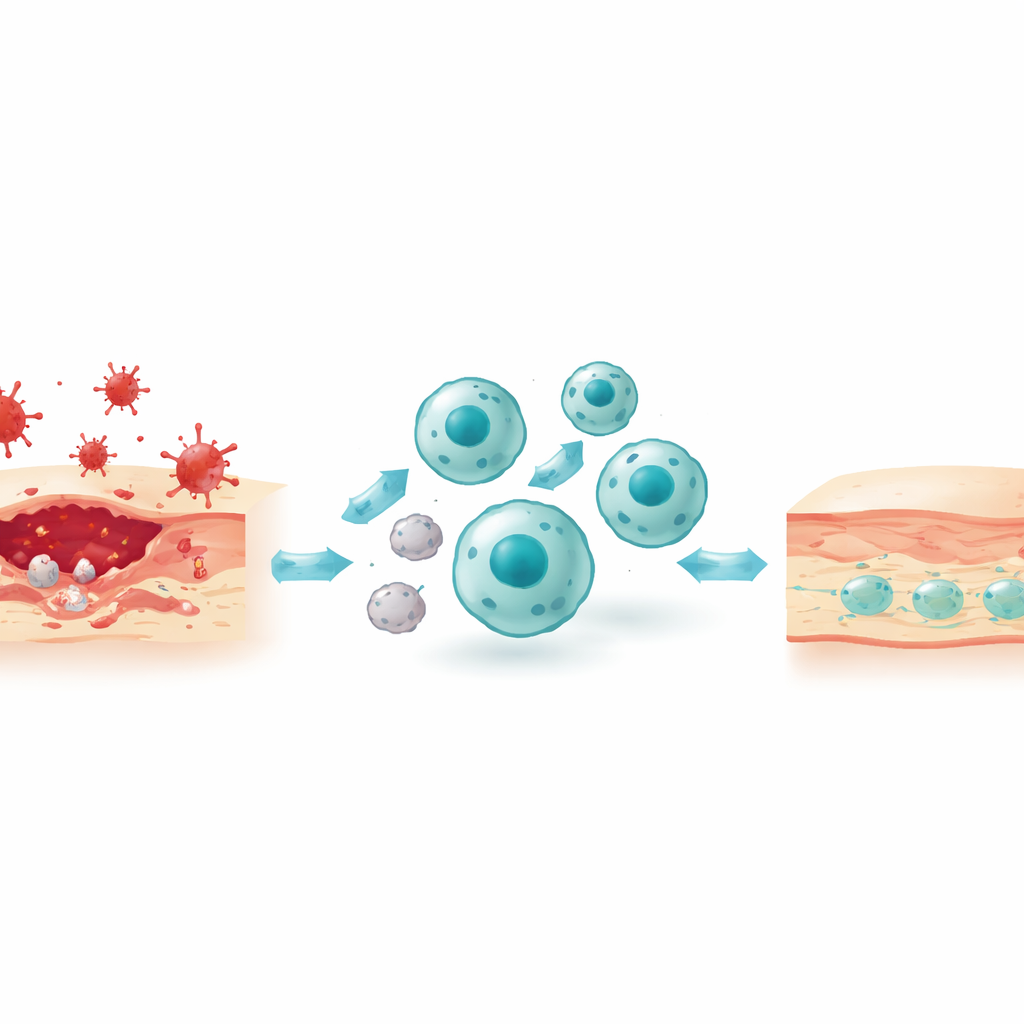
Le processus caché du nettoyage cellulaire
Un thème central de l’article est l’efferocytose, l’élimination programmée des cellules mourantes par les macrophages. Ce n’est pas une simple engloutissement en une étape. D’abord, les cellules apoptotiques (programmées pour mourir) émettent des signaux « venez-me-chercher » tels que des lipides et des nucléotides qui attirent les macrophages. Ces cellules mourantes exposent aussi certains lipides à leur surface externe pour servir de drapeaux « mangez-moi », reconnus soit directement par des récepteurs sur les macrophages, soit indirectement via des protéines « passerelles » dans le fluide environnant. Ensuite, le macrophage restructure son cytosquelette d’actine pour s’enrouler autour de la cible et l’internaliser, formant une vésicule scellée qui fusionnera ensuite avec des compartiments enzymatiques pour la digestion. Les produits de dégradation — lipides, acides aminés, nucléotides — sont ensuite recyclés ou exportés et, ce faisant, reprogramment le métabolisme du macrophage vers un état plus calme et pro-résolutionnel, qui libère des médiateurs anti-inflammatoires et des facteurs de croissance.
Comment une meilleure efferocytose peut sauver les plaies chroniques
Les auteurs passent en revue un large éventail d’interrupteurs moléculaires capables d’améliorer l’efferocytose et ainsi d’apaiser l’inflammation chronique. Certaines stratégies renforcent la reconnaissance initiale, par exemple en augmentant les signaux attirant les macrophages ou en stabilisant les drapeaux « mangez-moi » sur les cellules mourantes. D’autres visent à préserver ou restaurer des récepteurs macrophagiques clés qui sont souvent tronqués ou régulés à la baisse dans les maladies chroniques, ou à fournir des molécules passerelles qui connectent les cellules mourantes à ces récepteurs. Des approches supplémentaires agissent plus en profondeur dans la cellule, en orientant le système énergétique vers la glycolyse, en ajustant la gestion du cholestérol et des acides aminés, ou en améliorant la fusion des vésicules d’ingestion avec les lysosomes. Des médiateurs lipidiques spécialisés dérivés d’acides gras oméga‑3 forment également une boucle de rétroaction positive : ils sont produits lors de l’efferocytose, renforcent encore ce nettoyage et aident à résoudre l’inflammation. Ensemble, ces mécanismes montrent que l’amélioration de l’élimination cellulaire ne se réduit pas au simple tri des déchets ; elle reprogramme activement les macrophages pour soutenir la croissance des vaisseaux, le remodelage de la matrice et une réparation tissulaire ordonnée.
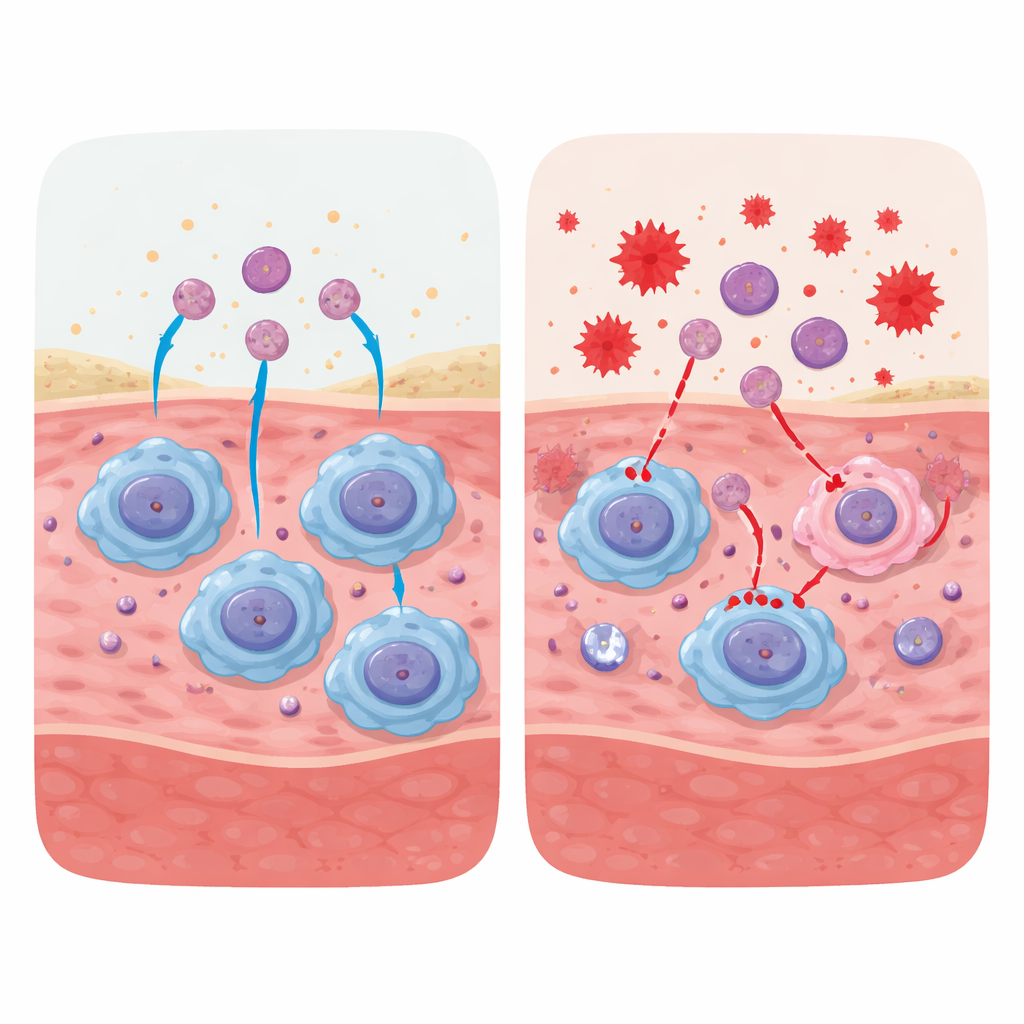
Nouvelles pistes thérapeutiques : aider les aidants
Au‑delà des médicaments et biomolécules, la revue met en avant des thérapies émergentes à base de cellules et de matériaux. L’infusion de cellules mononucléées périphériques du patient dans des plaies non cicatrisantes peut reconstituer des monocytes qui deviendront des macrophages réparateurs, restaurant l’équilibre entre phases inflammatoire et de guérison. Des biomatériaux intelligents et des pansements peuvent être conçus pour délivrer des signaux stimulant l’efferocytose, des facteurs de croissance ou des composés antioxydants directement dans le lit de la plaie. Les auteurs abordent aussi comment cibler les mitochondries, maîtriser les structures neutrophiles excessives et gérer la sénescence cellulaire peut converger pour améliorer la fonction macrophagique.
Ce que cela signifie pour les patients aux plaies difficiles à guérir
L’article conclut que l’échec du nettoyage cellulaire est un fil conducteur commun à de nombreux types de plaies chroniques. L’efferocytose des macrophages agit comme un interrupteur maître : lorsqu’elle fonctionne, l’inflammation est arrêtée au bon moment et la plaie passe à la phase de reconstruction ; lorsqu’elle faillit, le tissu reste piégé dans un limbe délétère. En concevant des thérapies qui restaurent ou amplifient ce ménage naturel — que ce soit par des molécules, des cellules ou des matériaux intelligents — les cliniciens pourraient raccourcir les temps de cicatrisation, réduire les complications et améliorer la qualité de vie des personnes vivant avec des plaies cutanées rebelles.
Citation: Gao, J., Zhu, D., Wang, J. et al. Macrophage efferocytosis promotes inflammation resolution and accelerates wound healing. Commun Biol 9, 613 (2026). https://doi.org/10.1038/s42003-026-10107-0
Mots-clés: cicatrisation, macrophages, inflammation, ulcères du pied diabétique, efferocytose