Clear Sky Science · es
La eférotosis por macrófagos promueve la resolución de la inflamación y acelera la cicatrización
Por qué nuestros cuerpos tienen problemas para cerrar heridas persistentes
Las heridas cutáneas crónicas, como las úlceras del pie diabético, pueden persistir durante meses, causando dolor, infecciones e incluso amputaciones. Este artículo de revisión explica por qué algunas heridas se niegan a sanar y pone el foco en una tarea de limpieza poco conocida realizada por células inmunitarias llamadas macrófagos. Cuando esta limpieza falla, la inflamación se mantiene en brasas en lugar de apagarse, y la piel no puede reconstruirse correctamente. Comprender y potenciar este sistema natural de eliminación podría conducir a tratamientos nuevos y menos invasivos para las heridas de difícil cicatrización.
El ritmo normal de la reparación de heridas
La reparación cutánea sana se desarrolla en cuatro etapas que se solapan: detener el sangrado, limpiar el daño, formar tejido nuevo y remodelar la cicatriz. Justo después de la lesión, los vasos sanguíneos se contraen y se forma un coágulo que actúa tanto de tapón como de andamiaje. Poco después, una oleada de células inmunitarias invade la zona. Los primeros en llegar, los neutrófilos, eliminan microbios invasores y digieren restos. Les siguen los monocitos que maduran a macrófagos, los cuales adaptan su conducta con el tiempo: al principio son inflamatorios y orientados al ataque; más tarde se vuelven calmantes y centrados en la reparación. A medida que el peligro remite, las células de la piel, de los vasos sanguíneos y del tejido conectivo proliferan y migran para cerrar la brecha, mientras las fibras de colágeno se reorganizan gradualmente para dar fuerza al tejido nuevo.
Cuando la limpieza falla y las heridas se estancan
En la diabetes, el envejecimiento, lesiones por radiación y otras condiciones crónicas, las heridas con frecuencia se quedan atrapadas en la fase inflamatoria. La hiperglucemia, el estrés oxidativo persistente y las señales de peligro procedentes de moléculas dañadas alteran cómo maduran y se comportan los macrófagos. En lugar de cambiar a un modo reparador, estas células permanecen bloqueadas en un estado proinflamatorio y se acumulan en el sitio de la herida. Al mismo tiempo, su capacidad para engullir y digerir células moribundas se ve debilitada. Como resultado, los neutrófilos muertos y moribundos se acumulan, pueden romperse y derramar contenidos irritantes. Estructuras en red adicionales procedentes de neutrófilos y una avalancha de moléculas inflamatorias envenenan aún más el entorno local. La herida entra en un ciclo vicioso: la inflamación continua impide la reconstrucción adecuada del tejido, lo que a su vez genera más daño celular e inflamación.
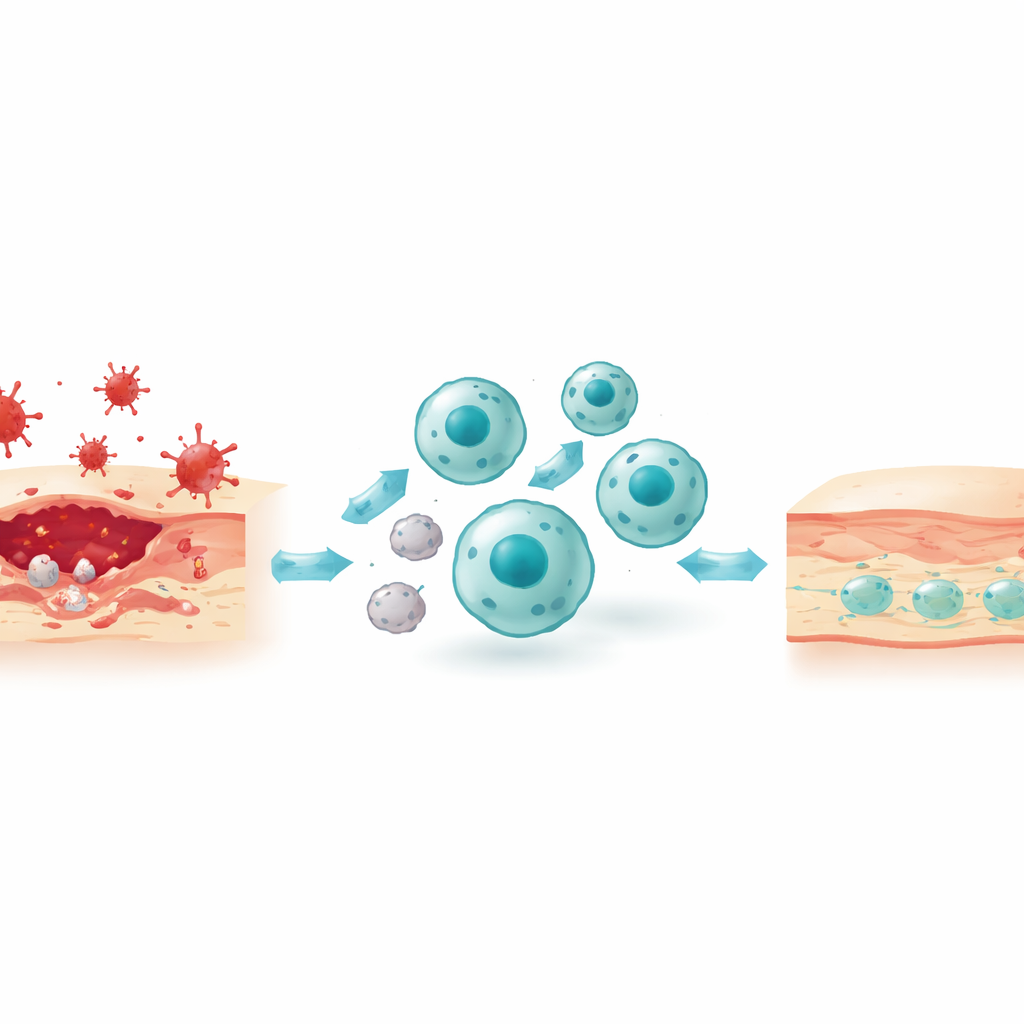
El proceso oculto de la limpieza celular
Un tema central del artículo es la eférotosis, la eliminación programada de células moribundas por macrófagos. Esto no es un simple trago de una sola vez. Primero, las células apoptóticas (programadas para morir) emiten señales «búscame» como lípidos y nucleótidos que atraen a los macrófagos hacia ellas. Estas células en proceso de muerte también desplazan ciertos lípidos a su superficie externa para actuar como banderas de «cómeme», que son reconocidas directamente por receptores en los macrófagos o indirectamente a través de proteínas puente en el fluido circundante. A continuación, el macrófago remodela su citoesqueleto de actina para envolverse e internalizar el objetivo, formando una burbuja sellada que luego se fusiona con sacos llenos de enzimas para su digestión. Los productos de la degradación—grasas, aminoácidos, nucleótidos—se reciclan o exportan, y en el proceso reconfiguran el metabolismo del macrófago hacia un estado más calmado y pro-resolutivo que libera mediadores antiinflamatorios y factores de crecimiento.
Cómo una eférotosis mejorada puede rescatar heridas crónicas
Los autores repasan una amplia variedad de interruptores moleculares que pueden mejorar la eférotosis y, con ello, calmar la inflamación crónica. Algunas estrategias potencian el reconocimiento temprano, por ejemplo aumentando señales que atraigan macrófagos o estabilizando las banderas de «cómeme» en las células moribundas. Otras se centran en preservar o restaurar receptores clave de macrófagos que con frecuencia son cortados o regulados a la baja en la enfermedad crónica, o en suministrar moléculas puente que conecten las células moribundas con esos receptores. Enfoques adicionales actúan más profundamente dentro de la célula, empujando el sistema energético hacia la glucólisis, afinando el manejo del colesterol y de los aminoácidos, o mejorando la fusión de las burbujas de ingestión con los lisosomas. Mediadores lipídicos especializados derivados de ácidos grasos omega-3 también forman un bucle de retroalimentación positiva: se producen durante la eférotosis, potencian aún más esta limpieza y ayudan a resolver la inflamación. En conjunto, estos mecanismos muestran que mejorar la eliminación celular no se trata solo de deshacerse de desechos; reprograma activamente a los macrófagos para apoyar el crecimiento de vasos sanguíneos, la remodelación de la matriz y una reparación tisular ordenada.
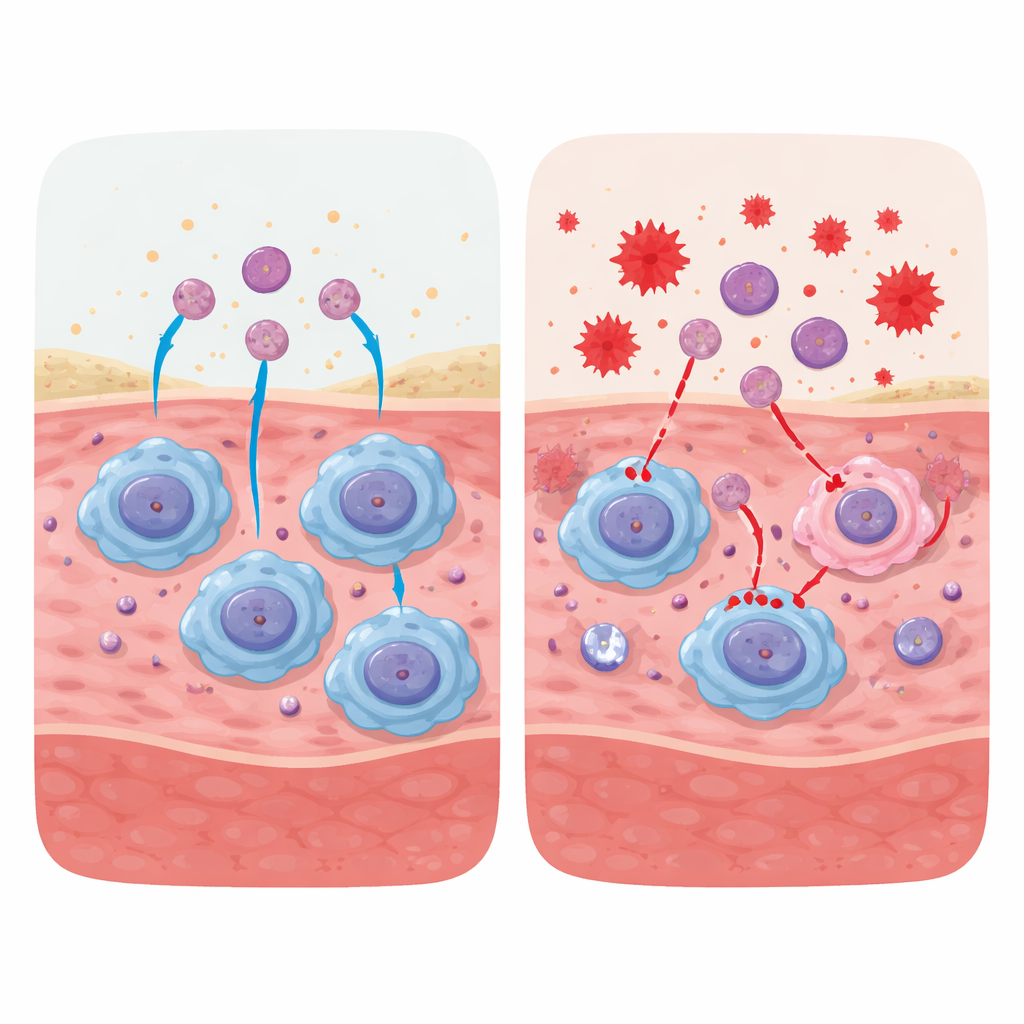
Nuevas ideas terapéuticas: ayudar a los ayudantes
Más allá de fármacos y biomoléculas, la revisión destaca terapias emergentes basadas en células y materiales. Infundir en heridas no cicatrizantes células mononucleares periféricas procedentes del propio paciente puede reponer monocitos que maduran en macrófagos reparativos, restaurando el equilibrio entre las fases inflamatoria y de curación. Biomateriales inteligentes y apósitos pueden diseñarse para liberar señales que potencien la eférotosis, factores de crecimiento o compuestos antioxidantes directamente en la cama de la herida. Los autores también discuten cómo dirigir a las mitocondrias, domar las estructuras neutrofílicas excesivas y manejar la senescencia celular pueden converger en la mejora de la función macrófaga.
Qué significa esto para pacientes con heridas de difícil cicatrización
El artículo concluye que la falla en la limpieza celular es un hilo común que une muchos tipos de heridas crónicas. La eférotosis por macrófagos actúa como un interruptor maestro: cuando funciona, la inflamación se apaga en el momento adecuado y la herida avanza hacia la reconstrucción; cuando falla, el tejido queda atrapado en un limbo dañino. Diseñando terapias que restauren o amplifiquen esta limpieza natural—ya sea mediante moléculas, células o materiales inteligentes—los clínicos podrían acortar los tiempos de curación, reducir complicaciones y mejorar la calidad de vida de las personas que conviven con heridas cutáneas persistentes.
Cita: Gao, J., Zhu, D., Wang, J. et al. Macrophage efferocytosis promotes inflammation resolution and accelerates wound healing. Commun Biol 9, 613 (2026). https://doi.org/10.1038/s42003-026-10107-0
Palabras clave: cicatrización de heridas, macrófagos, inflamación, úlceras del pie diabético, eférotosis