Clear Sky Science · it
Varianti bialleliche in RNU2-2 causano il disturbo neuroevolutivo recessivo noto più diffuso
Indizi nascosti nel DNA di famiglia
Alcune delle più gravi malattie cerebrali dell’infanzia sono rimaste a lungo inspiegate, lasciando le famiglie senza risposte o indicazioni chiare. Questo studio scopre una delle cause ereditarie più comuni di tali condizioni, non in un gene che codifica proteine ma in un minuscolo frammento di RNA che aiuta le cellule a elaborare i messaggi genetici. Comprendere questo nuovo disturbo non solo offre diagnosi attese da tempo a molte famiglie, ma apre anche opzioni pratiche per il test dei portatori, la pianificazione familiare e interventi precoci per i bambini colpiti. 
Un piccolo RNA con un grande compito
Le nostre cellule devono modificare i messaggi genetici grezzi prima che possano essere usati per produrre proteine. Questa modifica, chiamata splicing, è eseguita da una grande macchina nota come spliceosoma. Una delle sue componenti chiave è l’U2 small nuclear RNA, una breve molecola di RNA che aiuta a riconoscere dove il codice genetico deve essere tagliato e riunito. Il gene RNU2-2 codifica una versione di questo RNA U2. Fino a poco tempo fa, si sapeva che variazioni in questo e in geni RNA correlati causavano disturbi cerebrali in modo dominante—dove una sola copia difettosa è sufficiente a provocare la malattia. Il nuovo lavoro rivela che quando entrambe le copie di RNU2-2 sono danneggiate emerge una forma recessiva diversa di disturbo neuroevolutivo, e che questa è sorprendentemente comune.
Scoprire un disturbo cerebrale ereditario comune
I ricercatori hanno passato al setaccio dati genetici di decine di migliaia di persone con condizioni rare iscritte al 100,000 Genomes Project del Regno Unito e ai programmi genomici del National Health Service. Usando uno strumento statistico progettato per trovare varianti rare e patogene, hanno confrontato geni non codificanti proteine in oltre 14.000 individui con problemi neuroevolutivi con più di 50.000 senza tali diagnosi. Solo due geni sono emersi, RNU4-2 e RNU2-2, ma quando hanno cercato specificamente variazioni che agiscono in modo recessivo—dove una persona deve ereditare una copia alterata da ciascun genitore—RNU2-2 ha dato prove schiaccianti. Hanno identificato 18 famiglie ad alta confidenza in cui i bambini affetti portavano due varianti dannose di RNU2-2 su copie opposte del gene, oltre a famiglie candidate aggiuntive e altri nove casi in coorti indipendenti negli Stati Uniti, in Italia e nei Paesi Bassi. 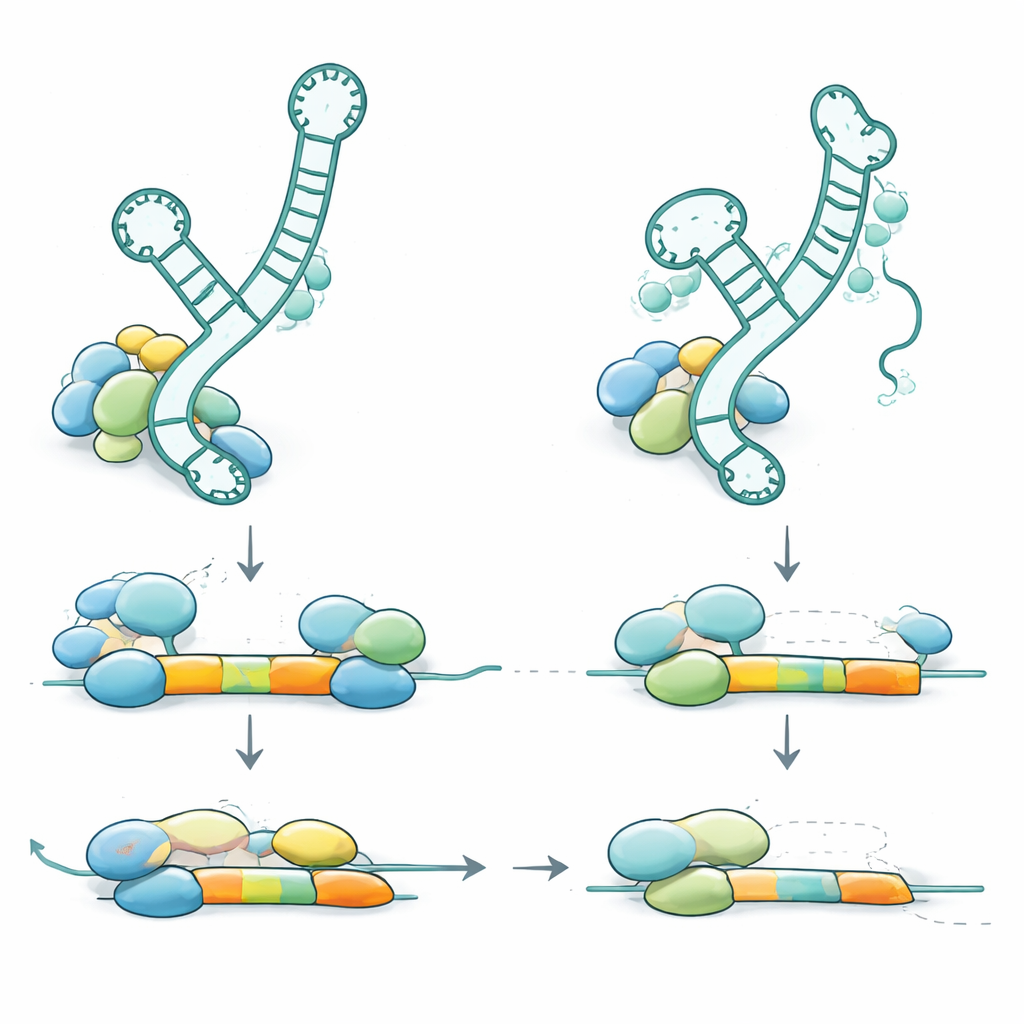
Come si manifesta la condizione nella vita reale
I bambini con questa sindrome recessiva da RNU2-2 di solito si presentano all’attenzione medica nell’infanzia o nei primi anni di vita. La maggior parte mostra ritardi nel raggiungimento delle tappe dello sviluppo, come sedersi, camminare o parlare, e molti hanno disabilità intellettive da moderate a gravi. Le crisi epilettiche sono molto comuni e possono iniziare precocemente; in alcuni bambini evolvono in sindromi epilettiche difficili da trattare. Il tono muscolare e il movimento sono spesso compromessi, con un quadro che va dall’ipotonia nell’infanzia a rigidità, posture anomale o movimenti involontari in seguito. Le immagini cerebrali possono apparire normali inizialmente ma poi mostrare perdita di tessuto cerebrale o alterazioni della sostanza bianca che collega le diverse regioni. Alcuni individui sono lievemente colpiti e rimangono relativamente stabili, mentre altri sviluppano complicazioni severe, compresi problemi respiratori, di alimentazione e, in rari casi, morte precoce.
Come le variazioni in RNU2-2 disturbano l’editing cellulare
Per capire come queste variazioni genetiche causano la malattia, il team ha esaminato dove ricadono le varianti all’interno dell’RNA U2-2 e come influenzano la sua struttura e il suo comportamento. Molte delle varianti recessive sono previste indebolire strutture a forcina—piccoli cappi nell’RNA che ne favoriscono il legame con proteine partner e altri RNA. Altre ricadono direttamente nella regione che riconosce i siti di splicing o nel sito di ancoraggio per un anello di proteine di supporto. Quando i ricercatori hanno analizzato campioni di sangue, hanno trovato che le copie difettose di RNU2-2 erano espresse a meno del 10% dei livelli normali nei soggetti affetti, indicando che l’RNA alterato è instabile e in gran parte degradato. L’organismo compensa parzialmente aumentando l’espressione di un gene U2 correlato (RNU2-1), così i livelli totali di U2 restano approssimativamente normali, ma questa compensazione non è sufficiente a prevenire la malattia. Nei portatori sani che hanno una sola copia difettosa, l’RNA danneggiato è anch’esso fortemente ridotto, tuttavia la copia normale aumenta la sua produzione, mantenendo la funzione complessiva al di sopra della soglia per i sintomi.
Perché questa scoperta è importante per le famiglie
Poiché questa sindrome segue un’ereditarietà recessiva, tende a ricomparire tra i fratelli quando entrambi i genitori sono portatori sani. Nel progetto genomico del Regno Unito, la sindrome recessiva da RNU2-2 rappresenta circa una famiglia su dieci con una diagnosi recessiva nota di disturbo neuroevolutivo, rendendola la singola causa più frequente in quella categoria e quasi comune quanto un disturbo dominante descritto in precedenza causato da un diverso gene RNA spliceosomiale. È fondamentale che gli autori dimostrino che un semplice test del RNA nel sangue può aiutare a distinguere le varianti veramente dannose da quelle innocue misurando quanto RNU2-2 viene perso e quanto il gene di riserva U2-1 viene sovraespresso. Per le famiglie, questo significa diagnosi più chiare, stime del rischio di ricorrenza più accurate e la possibilità di consulenza genetica preconcepimento o prenatale—trasformando un frammento oscuro di biologia dell’RNA in informazioni utilizzabili per decisioni mediche nel mondo reale.
Citazione: Greene, D., Mendez, R., Lees, J. et al. Biallelic variants in RNU2-2 cause the most prevalent known recessive neurodevelopmental disorder. Nat Genet 58, 774–781 (2026). https://doi.org/10.1038/s41588-026-02539-5
Parole chiave: disturbo neuroevolutivo, ereditarietà recessiva, spliceosoma, piccola RNA nucleare, sequenziamento del genoma