Clear Sky Science · de
Biallelische Varianten in RNU2-2 verursachen die bislang häufigste bekannte rezessive neuroentwicklungsstörung
Verborgene Hinweise in der Familien-DNA
Einige der schwersten kindlichen Hirnerkrankungen blieben lange unerklärt, wodurch Familien ohne klare Antworten oder Orientierung zurückgelassen wurden. Diese Studie deckt eine der häufigsten erblichen Ursachen solcher Erkrankungen auf und führt sie nicht zu einem Protein-codierenden Gen, sondern zu einem winzigen RNA-Stück, das Zellen dabei hilft, genetische Botschaften zu verarbeiten. Das Verständnis dieser neuen Erkrankung liefert vielen Familien nicht nur lang ersehnte Diagnosen, sondern eröffnet auch praktische Möglichkeiten für Trägertests, Familienplanung und frühere Betreuung betroffener Kinder. 
Eine winzige RNA mit großer Aufgabe
Unsere Zellen müssen rohe genetische Botschaften bearbeiten, bevor sie zur Proteinherstellung genutzt werden können. Diese Bearbeitung, Splicing genannt, wird von einer großen Maschine übernommen, dem Spliceosom. Einer seiner Schlüsselbestandteile ist die U2 kleine nukleäre RNA, ein kurzes RNA-Molekül, das dabei hilft, zu erkennen, wo Genabschnitte abgeschnitten und verbunden werden sollen. Das Gen RNU2-2 kodiert eine Version dieser U2-RNA. Bis vor Kurzem waren Veränderungen in diesem und verwandten RNA-Genen dafür bekannt, Hirnerkrankungen auf dominante Weise zu verursachen—ein fehlerhaftes Exemplar reicht dort aus, um Krankheit auszulösen. Die neue Arbeit zeigt, dass wenn beide Kopien von RNU2-2 geschädigt sind, eine andere, rezessive Form einer neuroentwicklungsstörung entsteht, die überraschend häufig ist.
Entdeckung einer häufigen erblichen Hirnerkrankung
Die Forschenden durchsuchten genetische Daten von Zehntausenden Menschen mit seltenen Erkrankungen, die im Rahmen des 100.000-Genom-Projekts des Vereinigten Königreichs und genomischer Programme des National Health Service erfasst wurden. Mit einem statistischen Werkzeug, das darauf ausgelegt ist, seltene krankheitsverursachende Varianten zu finden, verglichen sie nicht-protein-codierende Gene von über 14.000 Personen mit neuroentwicklungsstörungen mit mehr als 50.000 Personen ohne solche Diagnosen. Nur zwei Gene stachen hervor: RNU4-2 und RNU2-2. Als sie speziell nach Varianten suchten, die in rezessiver Weise wirken—also wenn eine Person von jedem Elternteil eine veränderte Kopie erben muss—zeigte RNU2-2 erdrückende Beweise. Sie identifizierten 18 hochzuverlässige Familien, in denen betroffene Kinder zwei schädigende RNU2-2-Varianten auf entgegengesetzten Genkopien trugen, sowie weitere Kandidatenfamilien und neun zusätzliche Fälle aus unabhängigen Kohorten in den USA, Italien und den Niederlanden. 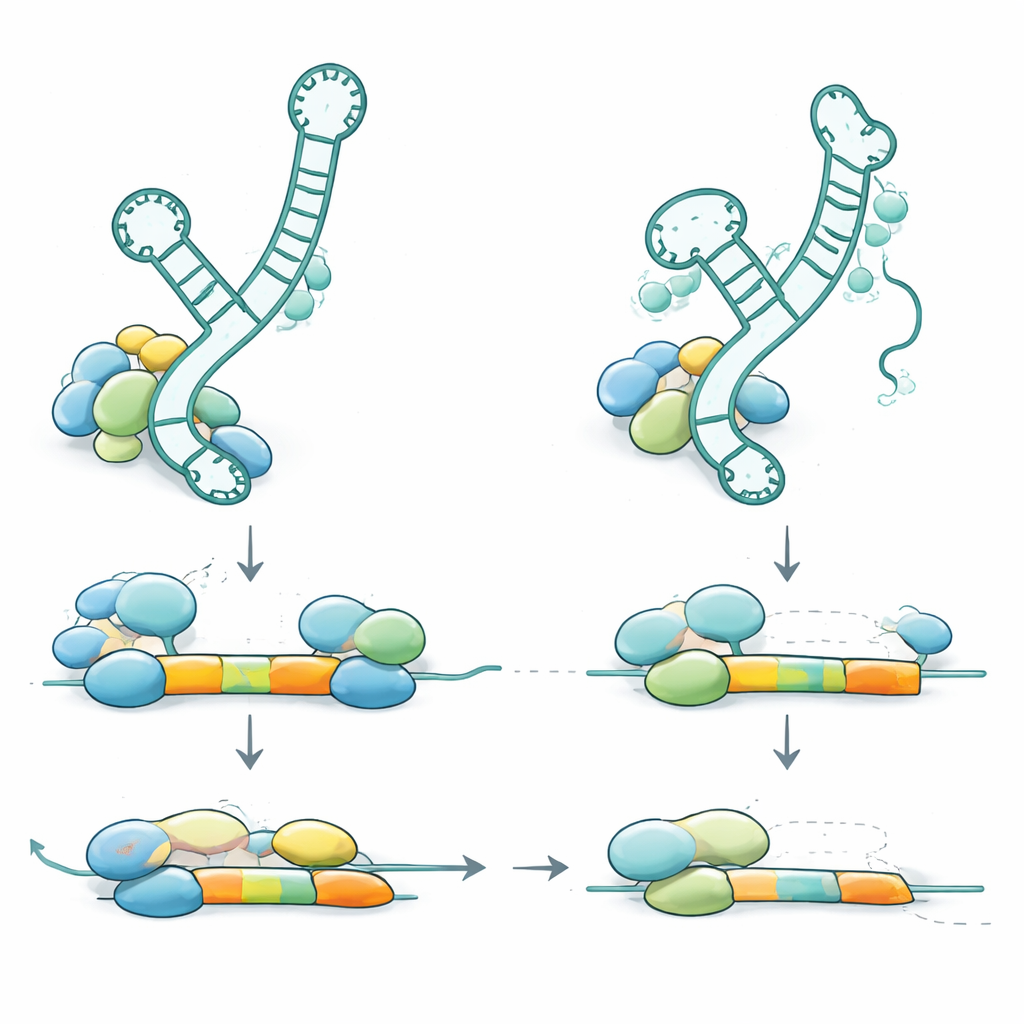
Wie sich die Erkrankung im Alltag zeigt
Kinder mit diesem rezessiven RNU2-2-Syndrom fallen typischerweise im Säuglings- oder frühen Kindesalter medizinisch auf. Die meisten haben Verzögerungen beim Erreichen entwicklungsbedingter Meilensteine wie Sitzen, Laufen oder Sprechen, und viele zeigen eine mittelschwere bis schwere geistige Behinderung. Anfälle sind sehr häufig und können früh beginnen; bei einigen Kindern entwickeln sie sich zu schwer behandelbaren epileptischen Syndromen. Muskeltonus und Bewegung sind oft betroffen und reichen von erniedrigtem Tonus im Säuglingsalter bis zu Steifheit, abnormen Haltungen oder unwillkürlichen Bewegungen im weiteren Verlauf. Hirnscans können anfangs normal erscheinen, später aber Gewebeverlust oder Veränderungen der weiße Substanz zeigen, die verschiedene Regionen verbindet. Einige Betroffene sind nur leicht beeinträchtigt und bleiben relativ stabil, während andere schwere Komplikationen entwickeln, einschließlich Atem‑ und Ernährungsproblemen und in seltenen Fällen einem frühen Tod.
Wie Veränderungen in RNU2-2 die zelluläre Bearbeitung stören
Um zu verstehen, wie diese genetischen Veränderungen Krankheit verursachen, untersuchten die Forschenden, wo die Varianten innerhalb der U2-2-RNA liegen und wie sie deren Struktur und Verhalten beeinflussen. Viele der rezessiven Varianten sollen Stamm‑Schleifen‑Strukturen schwächen—kleine Haarnadeln in der RNA, die helfen, Bindungen zu Partnerproteinen und anderen RNAs einzugehen. Andere liegen direkt in der Region, die Spleißstellen erkennt, oder in der Andockstelle für einen Ring Hilfsproteine. Als die Forschenden Blutproben untersuchten, stellten sie fest, dass fehlerhafte RNU2-2-Kopien bei Betroffenen mit weniger als 10 % der normalen Menge exprimiert wurden, was darauf hindeutet, dass die veränderte RNA instabil ist und weitgehend abgebaut wird. Der Körper kompensiert teilweise durch Hochregulation eines verwandten U2-Gens (RNU2-1), sodass die Gesamt-U2-Level ungefähr normal bleiben, doch diese Kompensation reicht nicht aus, um die Erkrankung zu verhindern. Bei gesunden Trägern mit nur einer fehlerhaften Kopie ist die geschädigte RNA ebenfalls stark reduziert, doch die verbleibende normale Kopie erhöht ihre Produktion, sodass die Gesamtfunktion über der Schwelle für Symptome bleibt.
Warum diese Entdeckung für Familien wichtig ist
Da dieses Syndrom einer rezessiven Vererbung folgt, tritt es in Familien mit gesunden Trägereltern gehäuft bei Geschwistern auf. Im britischen Genomprojekt macht das rezessive RNU2-2-Syndrom etwa eine von zehn Familien mit einer bekannten rezessiven neuroentwicklungsdiagnose aus und ist damit die häufigste einzelne Ursache in dieser Kategorie und fast ebenso häufig wie eine zuvor beschriebene dominante Erkrankung, die durch ein anderes spliceosomales RNA-Gen verursacht wird. Entscheidend ist, dass die Autoren zeigen, dass ein einfacher Blut‑RNA-Test helfen kann, wirklich schädliche Varianten von harmlosen zu unterscheiden, indem gemessen wird, wie stark RNU2-2 verloren geht und wie stark das Ersatz-U2-1 hochreguliert wird. Für Familien bedeutet das klarere Diagnosen, bessere Abschätzungen des Wiederholungsrisikos und die Möglichkeit einer genetischen Beratung vor der Zeugung oder während der Schwangerschaft—und verwandelt ein bislang obskures Stück RNA-Biologie in verwertbare Informationen für reale medizinische Entscheidungen.
Zitation: Greene, D., Mendez, R., Lees, J. et al. Biallelic variants in RNU2-2 cause the most prevalent known recessive neurodevelopmental disorder. Nat Genet 58, 774–781 (2026). https://doi.org/10.1038/s41588-026-02539-5
Schlüsselwörter: neuroentwicklungsstörung, rezessive Vererbung, Spliceosom, kleine nukleäre RNA, Genomsequenzierung